ഒരു സംയുക്തത്തിലെ ഒരു മൂലകത്തിന്റെ പിണ്ഡം. ഒരു പദാർത്ഥത്തിന്റെ ഫോർമുല അനുസരിച്ച് രാസ മൂലകങ്ങളുടെ പിണ്ഡത്തിന്റെ കണക്കുകൂട്ടൽ
മാസ് ഫ്രാക്ഷൻ പോലുള്ള ഒരു ആശയമാണ് ലേഖനം കൈകാര്യം ചെയ്യുന്നത്. അതിന്റെ കണക്കുകൂട്ടലിനുള്ള രീതികൾ നൽകിയിരിക്കുന്നു. ശബ്ദത്തിൽ സമാനവും എന്നാൽ ഭൗതിക അർത്ഥത്തിൽ വ്യത്യസ്തവുമായ അളവുകളുടെ നിർവചനങ്ങളും വിവരിച്ചിരിക്കുന്നു. മൂലകത്തിനും ഔട്ട്പുട്ടിനുമുള്ള ബഹുജന ഭിന്നസംഖ്യകളാണ് ഇവ.
ജീവന്റെ തൊട്ടിൽ - മോർട്ടാർ
നമ്മുടെ മനോഹരമായ നീല ഗ്രഹത്തിലെ ജീവന്റെ ഉറവിടം ജലമാണ്. ഈ പദപ്രയോഗം പലപ്പോഴും കാണാവുന്നതാണ്. എന്നിരുന്നാലും, സ്പെഷ്യലിസ്റ്റുകൾ ഒഴികെ കുറച്ച് ആളുകൾ ചിന്തിക്കുന്നു: വാസ്തവത്തിൽ, പദാർത്ഥങ്ങളുടെ ഒരു പരിഹാരം, രാസപരമായി ശുദ്ധമായ ജലമല്ല, ആദ്യത്തെ ജൈവ സംവിധാനങ്ങളുടെ വികസനത്തിന് അടിവസ്ത്രമായി മാറി. തീർച്ചയായും, ജനപ്രിയ സാഹിത്യത്തിലോ ഒരു പ്രോഗ്രാമിലോ, വായനക്കാരൻ "പ്രാഥമിക ചാറു" എന്ന പ്രയോഗം കണ്ടിട്ടുണ്ട്.
സങ്കീർണ്ണമായ ഓർഗാനിക് തന്മാത്രകളുടെ രൂപത്തിൽ ജീവന്റെ വികാസത്തിന് പ്രചോദനം നൽകിയ ഉറവിടങ്ങൾ ഇപ്പോഴും ചർച്ച ചെയ്യപ്പെടുന്നു. ചിലർ പ്രകൃതിദത്തവും വളരെ ഭാഗ്യകരവുമായ യാദൃശ്ചികത മാത്രമല്ല, പ്രാപഞ്ചിക ഇടപെടലും നിർദ്ദേശിക്കുന്നു. മാത്രമല്ല, നമ്മൾ സംസാരിക്കുന്നത് പുരാണ അന്യഗ്രഹജീവികളെക്കുറിച്ചല്ല, മറിച്ച് ഈ തന്മാത്രകൾ സൃഷ്ടിക്കുന്നതിനുള്ള പ്രത്യേക വ്യവസ്ഥകളെക്കുറിച്ചാണ്, അത് അന്തരീക്ഷമില്ലാത്ത ചെറിയ കോസ്മിക് ബോഡികളുടെ ഉപരിതലത്തിൽ മാത്രമേ നിലനിൽക്കൂ - ധൂമകേതുക്കളും ഛിന്നഗ്രഹങ്ങളും. അതിനാൽ, ഓർഗാനിക് തന്മാത്രകളുടെ പരിഹാരം എല്ലാ ജീവജാലങ്ങളുടെയും തൊട്ടിലാണെന്ന് പറയുന്നതായിരിക്കും കൂടുതൽ ശരി.
രാസപരമായി ശുദ്ധമായ ഒരു വസ്തുവായി വെള്ളം
വലിയ ഉപ്പിട്ട സമുദ്രങ്ങളും കടലുകളും ശുദ്ധമായ തടാകങ്ങളും നദികളും ഉണ്ടായിരുന്നിട്ടും, രാസപരമായി ശുദ്ധമായ രൂപത്തിൽ വെള്ളം വളരെ അപൂർവമാണ്, പ്രധാനമായും പ്രത്യേക ലബോറട്ടറികളിൽ. ഗാർഹിക ശാസ്ത്ര പാരമ്പര്യത്തിൽ, രാസപരമായി ശുദ്ധമായ ഒരു പദാർത്ഥം മാലിന്യങ്ങളുടെ പിണ്ഡത്തിന്റെ പത്തിൽ നിന്ന് മൈനസ് ആറാം ശക്തിയിൽ കൂടുതൽ അടങ്ങിയിട്ടില്ലാത്ത ഒരു വസ്തുവാണെന്ന് ഓർക്കുക.

വിദേശ ഘടകങ്ങളിൽ നിന്ന് തികച്ചും സ്വതന്ത്രമായ ഒരു പിണ്ഡം നേടുന്നതിന് അവിശ്വസനീയമായ ചിലവ് ആവശ്യമാണ്, മാത്രമല്ല അപൂർവ്വമായി സ്വയം ന്യായീകരിക്കുകയും ചെയ്യുന്നു. ഒരു വിദേശ ആറ്റത്തിന് പോലും പരീക്ഷണത്തെ നശിപ്പിക്കാൻ കഴിയുന്ന വ്യക്തിഗത വ്യവസായങ്ങളിൽ മാത്രമാണ് ഇത് ഉപയോഗിക്കുന്നത്. ഇന്നത്തെ മിനിയേച്ചർ സാങ്കേതികവിദ്യയുടെ (സ്മാർട്ട്ഫോണുകളും ടാബ്ലറ്റുകളും ഉൾപ്പെടെ) അടിസ്ഥാനമായ അർദ്ധചാലക ഘടകങ്ങൾ മാലിന്യങ്ങളോട് വളരെ സെൻസിറ്റീവ് ആണെന്നത് ശ്രദ്ധിക്കുക. അവയുടെ സൃഷ്ടിയിൽ, പൂർണ്ണമായും മലിനീകരിക്കപ്പെടാത്ത ലായകങ്ങൾ ആവശ്യമാണ്. എന്നിരുന്നാലും, ഗ്രഹത്തിന്റെ മുഴുവൻ ദ്രാവകവുമായി താരതമ്യപ്പെടുത്തുമ്പോൾ, ഇത് നിസ്സാരമാണ്. നമ്മുടെ ഗ്രഹത്തിൽ തുളച്ചുകയറുന്ന സാധാരണ ജലം അതിന്റെ ശുദ്ധമായ രൂപത്തിൽ വളരെ അപൂർവമായിരിക്കുന്നത് എങ്ങനെ? നമുക്ക് താഴെ വിശദീകരിക്കാം.
ഐഡിയൽ ലായനി
മുമ്പത്തെ വിഭാഗത്തിൽ ഉന്നയിച്ച ചോദ്യത്തിനുള്ള ഉത്തരം അവിശ്വസനീയമാംവിധം ലളിതമാണ്. വെള്ളത്തിന് ധ്രുവ തന്മാത്രകളുണ്ട്. ഇതിനർത്ഥം ഈ ദ്രാവകത്തിന്റെ എല്ലാ ചെറിയ കണങ്ങളിലും, പോസിറ്റീവ്, നെഗറ്റീവ് ധ്രുവങ്ങൾ കൂടുതലല്ല, മറിച്ച് വേർതിരിക്കപ്പെടുന്നു എന്നാണ്. അതേ സമയം, ദ്രാവക ജലത്തിൽ പോലും ഉണ്ടാകുന്ന ഘടനകൾ അധിക (ഹൈഡ്രജൻ എന്ന് വിളിക്കപ്പെടുന്ന) ബോണ്ടുകൾ സൃഷ്ടിക്കുന്നു. മൊത്തത്തിൽ ഇത് ഇനിപ്പറയുന്ന ഫലം നൽകുന്നു. വെള്ളത്തിലേക്ക് പ്രവേശിക്കുന്ന പദാർത്ഥം (അതിന് എന്ത് ചാർജ് ഉണ്ടെങ്കിലും) ദ്രാവകത്തിന്റെ തന്മാത്രകളാൽ വേർതിരിച്ചെടുക്കുന്നു. അലിഞ്ഞുപോയ അശുദ്ധിയുടെ ഓരോ കണികയും ജല തന്മാത്രകളുടെ നെഗറ്റീവ് അല്ലെങ്കിൽ പോസിറ്റീവ് വശങ്ങളാൽ പൊതിഞ്ഞതാണ്. അങ്ങനെ, ഈ അദ്വിതീയ ദ്രാവകം വൈവിധ്യമാർന്ന പദാർത്ഥങ്ങളെ വളരെ വലിയ അളവിൽ അലിയിക്കാൻ പ്രാപ്തമാണ്.

ലായനിയിൽ മാസ് ഫ്രാക്ഷൻ എന്ന ആശയം
തത്ഫലമായുണ്ടാകുന്ന ലായനിയിൽ "മാസ് ഫ്രാക്ഷൻ" എന്ന് വിളിക്കുന്ന ചില മാലിന്യങ്ങൾ അടങ്ങിയിരിക്കുന്നു. ഈ പദപ്രയോഗം പലപ്പോഴും കണ്ടെത്തിയില്ലെങ്കിലും. സാധാരണയായി ഉപയോഗിക്കുന്ന മറ്റൊരു പദമാണ് "ഏകാഗ്രത". ഒരു പ്രത്യേക അനുപാതത്തിലാണ് പിണ്ഡം നിർണ്ണയിക്കുന്നത്. ഞങ്ങൾ ഒരു സൂത്രവാക്യം നൽകില്ല, ഇത് വളരെ ലളിതമാണ്, ഭൗതിക അർത്ഥം ഞങ്ങൾ നന്നായി വിശദീകരിക്കും. ഇത് രണ്ട് പിണ്ഡങ്ങളുടെ അനുപാതമാണ് - പരിഹാരത്തിലേക്കുള്ള മാലിന്യങ്ങൾ. അളവില്ലാത്ത അളവാണ് മാസ് ഫ്രാക്ഷൻ. നിർദ്ദിഷ്ട ജോലികളെ ആശ്രയിച്ച് ഇത് വ്യത്യസ്ത രീതികളിൽ പ്രകടിപ്പിക്കുന്നു. അതായത്, ഒരു യൂണിറ്റിന്റെ ഭിന്നസംഖ്യകളിൽ, ഫോർമുലയിൽ പിണ്ഡത്തിന്റെ അനുപാതം മാത്രമേ അടങ്ങിയിട്ടുള്ളൂ എങ്കിൽ, ശതമാനത്തിൽ - ഫലം 100% കൊണ്ട് ഗുണിച്ചാൽ.
ദ്രവത്വം
H 2 O കൂടാതെ, മറ്റ് ലായകങ്ങളും ഉപയോഗിക്കുന്നു. കൂടാതെ, അടിസ്ഥാനപരമായി ജലത്തിന്റെ തന്മാത്രകൾ ഉപേക്ഷിക്കാത്ത പദാർത്ഥങ്ങളുണ്ട്. എന്നാൽ അവർ എളുപ്പത്തിൽ ഗ്യാസോലിൻ അല്ലെങ്കിൽ ചൂടുള്ള സൾഫ്യൂറിക് ആസിഡിൽ ലയിക്കുന്നു.

ദ്രാവകത്തിൽ ഒരു പ്രത്യേക മെറ്റീരിയൽ എത്രത്തോളം നിലനിൽക്കുമെന്ന് കാണിക്കുന്ന പ്രത്യേക പട്ടികകൾ ഉണ്ട്. ഈ സൂചകത്തെ സോളിബിലിറ്റി എന്ന് വിളിക്കുന്നു, ഇത് താപനിലയെ ആശ്രയിച്ചിരിക്കുന്നു. അത് ഉയർന്നതനുസരിച്ച്, ലായകത്തിന്റെ ആറ്റങ്ങളോ തന്മാത്രകളോ കൂടുതൽ സജീവമായി നീങ്ങുന്നു, കൂടുതൽ മാലിന്യങ്ങൾ ആഗിരണം ചെയ്യാൻ കഴിയും.
ഒരു ലായനിയിൽ ഒരു ലായനിയുടെ അനുപാതം നിർണ്ണയിക്കുന്നതിനുള്ള ഓപ്ഷനുകൾ
രസതന്ത്രജ്ഞരുടെയും സാങ്കേതിക വിദഗ്ധരുടെയും എഞ്ചിനീയർമാരുടെയും ഭൗതികശാസ്ത്രജ്ഞരുടെയും ചുമതലകൾ വ്യത്യസ്തമായിരിക്കുമെന്നതിനാൽ, വെള്ളത്തിൽ ലയിച്ച പദാർത്ഥത്തിന്റെ ഭാഗം വ്യത്യസ്ത രീതികളിൽ നിർവചിക്കപ്പെടുന്നു. വോളിയം അംശം പരിഹാരത്തിന്റെ മൊത്തം വോള്യത്തിലേക്കുള്ള അശുദ്ധിയുടെ അളവ് കണക്കാക്കുന്നു. മറ്റൊരു പാരാമീറ്റർ ഉപയോഗിക്കുന്നു, പക്ഷേ തത്വം അതേപടി തുടരുന്നു.
വോളിയം ഭിന്നസംഖ്യ ഒരു യൂണിറ്റിന്റെ ഭിന്നസംഖ്യകളിലോ ശതമാനത്തിലോ പ്രകടിപ്പിക്കുന്ന അളവില്ലായ്മ നിലനിർത്തുന്നു. മോളാരിറ്റി ("മോളാർ വോളിയം കോൺസൺട്രേഷൻ" എന്നും അറിയപ്പെടുന്നു) എന്നത് ഒരു നിശ്ചിത അളവിലുള്ള ലായനിയിലെ ഒരു ലായനിയുടെ മോളുകളുടെ എണ്ണമാണ്. ഈ നിർവചനം ഇതിനകം ഒരു സിസ്റ്റത്തിന്റെ രണ്ട് വ്യത്യസ്ത പാരാമീറ്ററുകൾ ഉൾക്കൊള്ളുന്നു, ഈ അളവിന്റെ അളവ് വ്യത്യസ്തമാണ്. ഒരു ലിറ്ററിന് മോളുകളിൽ ഇത് പ്രകടിപ്പിക്കുന്നു. തന്മാത്രകളുടെയോ ആറ്റങ്ങളുടെയോ പത്ത് മുതൽ ഇരുപത്തിമൂന്നാം ഡിഗ്രി വരെ അടങ്ങിയിരിക്കുന്ന ഒരു പദാർത്ഥത്തിന്റെ അളവാണ് മോൾ എന്ന് ഞങ്ങൾ ഓർക്കുന്നു.
ഒരു മൂലകത്തിന്റെ പിണ്ഡം എന്ന ആശയം
ഈ മൂല്യം പരിഹാരങ്ങളുമായി പരോക്ഷമായി ബന്ധപ്പെട്ടിരിക്കുന്നു. ഒരു മൂലകത്തിന്റെ പിണ്ഡം മുകളിൽ ചർച്ച ചെയ്ത ആശയത്തിൽ നിന്ന് വ്യത്യസ്തമാണ്. ഏതൊരു സങ്കീർണ്ണ രാസ സംയുക്തവും രണ്ടോ അതിലധികമോ മൂലകങ്ങൾ ഉൾക്കൊള്ളുന്നു. ഓരോന്നിനും അതിന്റേതായ ആപേക്ഷിക ഭാരം ഉണ്ട്. ഈ മൂല്യം മെൻഡലീവിന്റെ രാസവ്യവസ്ഥയിൽ കാണാം. അവിടെ ഇത് പൂർണ്ണസംഖ്യകളല്ലാത്ത സംഖ്യകളിൽ സൂചിപ്പിച്ചിരിക്കുന്നു, എന്നാൽ ഏകദേശ ടാസ്ക്കുകൾക്ക് മൂല്യം റൗണ്ട് ഓഫ് ചെയ്യാം. ഒരു സങ്കീർണ്ണ പദാർത്ഥത്തിന്റെ ഘടനയിൽ ഓരോ തരത്തിലുമുള്ള ഒരു നിശ്ചിത എണ്ണം ആറ്റങ്ങൾ ഉൾപ്പെടുന്നു. ഉദാഹരണത്തിന്, വെള്ളത്തിൽ (H 2 O) രണ്ട് ഹൈഡ്രജൻ ആറ്റങ്ങളും ഒരു ഓക്സിജനും ഉണ്ട്. മുഴുവൻ പദാർത്ഥത്തിന്റെയും ആപേക്ഷിക പിണ്ഡവും ശതമാനത്തിൽ നൽകിയിരിക്കുന്ന മൂലകവും തമ്മിലുള്ള അനുപാതം മൂലകത്തിന്റെ പിണ്ഡത്തിന്റെ അംശമായിരിക്കും.

അനുഭവപരിചയമില്ലാത്ത വായനക്കാർക്ക്, ഈ രണ്ട് ആശയങ്ങളും അടുത്തതായി തോന്നാം. പലപ്പോഴും അവർ പരസ്പരം ആശയക്കുഴപ്പത്തിലാകുന്നു. വിളവിന്റെ ബഹുജന ഭിന്നസംഖ്യ പരിഹാരങ്ങളെയല്ല, പ്രതികരണങ്ങളെയാണ് സൂചിപ്പിക്കുന്നത്. ഏതൊരു രാസപ്രക്രിയയും എല്ലായ്പ്പോഴും നിർദ്ദിഷ്ട ഉൽപ്പന്നങ്ങളുടെ രസീതിയിൽ തുടരുന്നു. റിയാക്ടന്റുകളേയും പ്രോസസ്സ് അവസ്ഥകളേയും ആശ്രയിച്ച് സൂത്രവാക്യങ്ങൾ ഉപയോഗിച്ചാണ് അവയുടെ വിളവ് കണക്കാക്കുന്നത്. കേവലം പിണ്ഡത്തിന്റെ ഭിന്നസംഖ്യയിൽ നിന്ന് വ്യത്യസ്തമായി, ഈ മൂല്യം നിർണ്ണയിക്കുന്നത് അത്ര എളുപ്പമല്ല. സൈദ്ധാന്തിക കണക്കുകൂട്ടലുകൾ പ്രതിപ്രവർത്തന ഉൽപ്പന്നത്തിന്റെ പദാർത്ഥത്തിന്റെ പരമാവധി അളവ് നിർദ്ദേശിക്കുന്നു. എന്നിരുന്നാലും, പരിശീലനം എല്ലായ്പ്പോഴും അല്പം കുറഞ്ഞ മൂല്യം നൽകുന്നു. ഈ പൊരുത്തക്കേടിന്റെ കാരണങ്ങൾ വളരെ ചൂടായ തന്മാത്രകൾക്കിടയിൽ പോലും ഊർജ്ജത്തിന്റെ വിതരണത്തിലാണ്.

അങ്ങനെ, ഒരു പ്രതിപ്രവർത്തനത്തിലേക്ക് പ്രവേശിക്കാനും അവയുടെ യഥാർത്ഥ അവസ്ഥയിൽ തുടരാനും കഴിയാത്ത "തണുത്ത" കണങ്ങൾ എല്ലായ്പ്പോഴും ഉണ്ടായിരിക്കും. സൈദ്ധാന്തികമായി കണക്കാക്കിയതിൽ നിന്ന് യഥാർത്ഥത്തിൽ ലഭിച്ച പദാർത്ഥത്തിന്റെ ശതമാനമാണ് വിളവിന്റെ ബഹുജന ഭിന്നസംഖ്യയുടെ ഭൗതിക അർത്ഥം. ഫോർമുല അവിശ്വസനീയമാംവിധം ലളിതമാണ്. പ്രായോഗികമായി ലഭിച്ച ഉൽപ്പന്നത്തിന്റെ പിണ്ഡം പ്രായോഗികമായി കണക്കാക്കിയ ഒന്നിന്റെ പിണ്ഡം കൊണ്ട് ഹരിക്കുന്നു, മുഴുവൻ പദപ്രയോഗവും നൂറു ശതമാനം കൊണ്ട് ഗുണിക്കുന്നു. വിളവിന്റെ പിണ്ഡം നിർണ്ണയിക്കുന്നത് പ്രതിപ്രവർത്തനത്തിന്റെ മോളുകളുടെ എണ്ണം അനുസരിച്ചാണ്. അതിനെക്കുറിച്ച് മറക്കരുത്. ഒരു പദാർത്ഥത്തിന്റെ ഒരു മോൾ അതിന്റെ ആറ്റങ്ങളുടെ അല്ലെങ്കിൽ തന്മാത്രകളുടെ ഒരു നിശ്ചിത സംഖ്യയാണ് എന്നതാണ് വസ്തുത. ദ്രവ്യത്തിന്റെ സംരക്ഷണ നിയമം അനുസരിച്ച്, ഇരുപത് ജല തന്മാത്രകൾക്ക് സൾഫ്യൂറിക് ആസിഡിന്റെ മുപ്പത് തന്മാത്രകൾ ഉണ്ടാക്കാൻ കഴിയില്ല, അതിനാൽ പ്രശ്നങ്ങൾ ഈ രീതിയിൽ കണക്കാക്കുന്നു. പ്രാരംഭ ഘടകത്തിന്റെ മോളുകളുടെ എണ്ണത്തിൽ നിന്ന്, പിണ്ഡം ഉരുത്തിരിഞ്ഞതാണ്, ഇത് ഫലത്തിന് സൈദ്ധാന്തികമായി സാധ്യമാണ്. അപ്പോൾ, പ്രതികരണ ഉൽപ്പന്നത്തിന്റെ യഥാർത്ഥത്തിൽ എത്രമാത്രം ലഭിച്ചുവെന്ന് അറിയുമ്പോൾ, മുകളിൽ വിവരിച്ച ഫോർമുല ഉപയോഗിച്ച് വിളവിന്റെ പിണ്ഡം നിർണ്ണയിക്കപ്പെടുന്നു.
1. വാക്യങ്ങളിലെ വിടവുകൾ പൂരിപ്പിക്കുക.
a) ഗണിതശാസ്ത്രത്തിൽ, "പങ്കിടൽ" എന്നത് ഒരു ഭാഗത്തിന്റെ മൊത്തത്തിലുള്ള അനുപാതമാണ്. ഒരു മൂലകത്തിന്റെ പിണ്ഡം കണക്കാക്കാൻ, സൂത്രവാക്യത്തിൽ നൽകിയിരിക്കുന്ന മൂലകത്തിന്റെ ആറ്റങ്ങളുടെ എണ്ണം കൊണ്ട് അതിന്റെ ആപേക്ഷിക ആറ്റോമിക പിണ്ഡത്തെ ഗുണിച്ച് പദാർത്ഥത്തിന്റെ ആപേക്ഷിക തന്മാത്രാ പിണ്ഡം കൊണ്ട് ഹരിക്കുക.
b) പദാർത്ഥം നിർമ്മിക്കുന്ന എല്ലാ മൂലകങ്ങളുടെയും പിണ്ഡം ഭിന്നസംഖ്യകളുടെ ആകെത്തുക 1 അല്ലെങ്കിൽ 100% ആണ്.
2. ഇനിപ്പറയുന്നവയാണെങ്കിൽ മൂലകങ്ങളുടെ പിണ്ഡം കണ്ടെത്തുന്നതിനുള്ള ഗണിത സൂത്രവാക്യങ്ങൾ എഴുതുക:
a) പദാർത്ഥത്തിന്റെ ഫോർമുല P 2 O 5, M r \u003d 2 * 31 + 5 * 16 \u003d 142 ആണ്
w(P) = 2*31/132 *100% = 44%
w(O) = 5*16/142*100% = 56% അല്ലെങ്കിൽ w(O) = 100-44=56.
b) പദാർത്ഥത്തിന്റെ ഫോർമുല - A x B y
w(A) = Ar(A)*x/Mr(AxBy) * 100%
w(B) = Ar(B)*y / Mr(AxBy) *100%
3. മൂലകങ്ങളുടെ പിണ്ഡ ഭിന്നസംഖ്യകൾ കണക്കാക്കുക:
a) മീഥേനിൽ (CH 4)

ബി) സോഡിയം കാർബണേറ്റിൽ (Na 2 CO 3)

4. പദാർത്ഥങ്ങളിൽ സൂചിപ്പിച്ചിരിക്കുന്ന മൂലകങ്ങളുടെ പിണ്ഡം താരതമ്യം ചെയ്ത് ഒരു അടയാളം ഇടുക<, >അല്ലെങ്കിൽ =:

5. ഹൈഡ്രജനുമായി സിലിക്കണിന്റെ സംയോജനത്തിൽ, സിലിക്കണിന്റെ പിണ്ഡം 87.5%, ഹൈഡ്രജൻ 12.5% ആണ്. പദാർത്ഥത്തിന്റെ ആപേക്ഷിക തന്മാത്രാ ഭാരം 32 ആണ്. ഈ സംയുക്തത്തിന്റെ ഫോർമുല നിർണ്ണയിക്കുക.

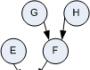
6. സംയുക്തത്തിലെ മൂലകങ്ങളുടെ ബഹുജന ഭിന്നസംഖ്യകൾ ഡയഗ്രാമിൽ കാണിച്ചിരിക്കുന്നു:

ഈ പദാർത്ഥത്തിന്റെ ആപേക്ഷിക തന്മാത്രാ ഭാരം 100 ആണെന്ന് അറിയാമെങ്കിൽ അതിന്റെ ഫോർമുല നിർണ്ണയിക്കുക.

7. എഥിലീൻ ഒരു സ്വാഭാവിക ഫലം കായ്ക്കുന്ന ഉത്തേജകമാണ്: പഴങ്ങളിൽ ഇത് അടിഞ്ഞുകൂടുന്നത് അവയുടെ പഴുക്കലിനെ ത്വരിതപ്പെടുത്തുന്നു. നേരത്തെ എഥിലീൻ ശേഖരണം ആരംഭിക്കുന്നു, നേരത്തെ പഴങ്ങൾ പാകമാകും. അതിനാൽ, പഴങ്ങൾ പാകമാകുന്നത് കൃത്രിമമായി വേഗത്തിലാക്കാൻ എഥിലീൻ ഉപയോഗിക്കുന്നു. കാർബണിന്റെ പിണ്ഡം 85.7% ആണെന്നും ഹൈഡ്രജന്റെ പിണ്ഡം -14.3% ആണെന്നും അറിയാമെങ്കിൽ എഥിലീൻ ഫോർമുല കണ്ടെത്തുക. ഈ പദാർത്ഥത്തിന്റെ ആപേക്ഷിക തന്മാത്രാ ഭാരം 28 ആണ്.

8. പദാർത്ഥത്തിന്റെ കെമിക്കൽ ഫോർമുല, അത് അറിയാമെങ്കിൽ കണ്ടെത്തുക
a) w(Ca) = 36%, w(Cl) = 64%

b) w(Na) 29.1%, w(S) = 40.5%, w(O) = 30.4%.

9. ലാപിസിന് ആന്റിമൈക്രോബയൽ ഗുണങ്ങളുണ്ട്. മുമ്പ്, അരിമ്പാറയെ നശിപ്പിക്കാൻ ഇത് ഉപയോഗിച്ചിരുന്നു. ചെറിയ സാന്ദ്രതയിൽ, ഇത് ഒരു ആൻറി-ഇൻഫ്ലമേറ്ററി, രേതസ് ആയി പ്രവർത്തിക്കുന്നു, പക്ഷേ പൊള്ളലേറ്റേക്കാം. 63.53% വെള്ളിയും 8.24% നൈട്രജനും 28.23% ഓക്സിജനും അടങ്ങിയിട്ടുണ്ടെന്ന് അറിയാമെങ്കിൽ ലാപിസിന്റെ ഫോർമുല കണ്ടെത്തുക.
പരിഹാരംരണ്ടോ അതിലധികമോ ഘടകങ്ങളുടെ ഏകതാനമായ മിശ്രിതത്തെ വിളിക്കുന്നു.
ഒരു ലായനി രൂപപ്പെടുത്തുന്നതിന് മിശ്രിതമായ പദാർത്ഥങ്ങളെ വിളിക്കുന്നു ഘടകങ്ങൾ.
പരിഹാരത്തിന്റെ ഘടകങ്ങൾ ലായനി, ഒന്നിൽ കൂടുതൽ ആയിരിക്കാം, കൂടാതെ ലായക. ഉദാഹരണത്തിന്, വെള്ളത്തിലെ പഞ്ചസാരയുടെ ലായനിയിൽ, പഞ്ചസാര ലായകവും ജലം ലായകവുമാണ്.
ചിലപ്പോൾ ലായകമെന്ന ആശയം ഏതെങ്കിലും ഘടകങ്ങളിൽ തുല്യമായി പ്രയോഗിക്കാവുന്നതാണ്. ഉദാഹരണത്തിന്, പരസ്പരം നന്നായി ലയിക്കുന്ന രണ്ടോ അതിലധികമോ ദ്രാവകങ്ങൾ കലർത്തി ലഭിക്കുന്ന പരിഹാരങ്ങൾക്ക് ഇത് ബാധകമാണ്. അതിനാൽ, പ്രത്യേകിച്ച്, മദ്യവും വെള്ളവും അടങ്ങിയ ഒരു ലായനിയിൽ, മദ്യവും വെള്ളവും ഒരു ലായകമെന്ന് വിളിക്കാം. എന്നിരുന്നാലും, മിക്കപ്പോഴും ജലം അടങ്ങിയ ലായനികളുമായി ബന്ധപ്പെട്ട്, പരമ്പരാഗതമായി ജലത്തെ ഒരു ലായകവും രണ്ടാമത്തെ ഘടകത്തെ ലായനിയും എന്ന് വിളിക്കുന്നത് പതിവാണ്.
പരിഹാരത്തിന്റെ ഘടനയുടെ അളവ് സ്വഭാവം എന്ന നിലയിൽ, അത്തരമൊരു ആശയം മിക്കപ്പോഴും ഉപയോഗിക്കുന്നു ബഹുജന ഭിന്നസംഖ്യലായനിയിലെ പദാർത്ഥങ്ങൾ. ഒരു പദാർത്ഥത്തിന്റെ പിണ്ഡത്തിന്റെ പിണ്ഡവും അതിൽ അടങ്ങിയിരിക്കുന്ന ലായനിയുടെ പിണ്ഡവും തമ്മിലുള്ള അനുപാതമാണ് ഒരു പദാർത്ഥത്തിന്റെ പിണ്ഡം:
എവിടെ ω (ഇൻ-വ) - ലായനിയിൽ അടങ്ങിയിരിക്കുന്ന പദാർത്ഥത്തിന്റെ പിണ്ഡം (ഗ്രാം), എം(v-va) - ലായനിയിൽ അടങ്ങിയിരിക്കുന്ന പദാർത്ഥത്തിന്റെ പിണ്ഡം (g), m (p-ra) - ലായനിയുടെ പിണ്ഡം (g).
(1) ഫോർമുലയിൽ നിന്ന്, പിണ്ഡത്തിന്റെ ഭിന്നസംഖ്യയ്ക്ക് 0 മുതൽ 1 വരെയുള്ള മൂല്യങ്ങൾ എടുക്കാൻ കഴിയും, അതായത്, ഇത് ഒരു യൂണിറ്റിന്റെ ഭിന്നസംഖ്യയാണ്. ഇക്കാര്യത്തിൽ, ബഹുജന ഭിന്നസംഖ്യയെ ഒരു ശതമാനമായും (%) പ്രകടിപ്പിക്കാം, ഈ ഫോർമാറ്റിലാണ് മിക്കവാറും എല്ലാ പ്രശ്നങ്ങളിലും ഇത് ദൃശ്യമാകുന്നത്. ഒരു ശതമാനമായി പ്രകടിപ്പിക്കുന്ന പിണ്ഡം, ഫോർമുല (1) ന് സമാനമായ ഒരു ഫോർമുല ഉപയോഗിച്ചാണ് കണക്കാക്കുന്നത്, ഒരേയൊരു വ്യത്യാസത്തിൽ ലായനിയുടെ പിണ്ഡത്തിന്റെയും മുഴുവൻ ലായനിയുടെയും പിണ്ഡത്തിന്റെ അനുപാതം 100% കൊണ്ട് ഗുണിക്കുന്നു:
രണ്ട് ഘടകങ്ങൾ മാത്രമുള്ള ഒരു ലായനിക്ക്, ലായകത്തിന്റെ ω(r.v.) പിണ്ഡത്തിന്റെ പിണ്ഡവും ω(ലായകത്തിന്റെ) പിണ്ഡത്തിന്റെ അംശവും യഥാക്രമം കണക്കാക്കാം.
ഒരു ലായനിയുടെ പിണ്ഡം എന്നും വിളിക്കപ്പെടുന്നു പരിഹാരം ഏകാഗ്രത.
രണ്ട് ഘടക പരിഹാരത്തിന്, അതിന്റെ പിണ്ഡം ലായകത്തിന്റെയും ലായകത്തിന്റെയും പിണ്ഡത്തിന്റെ ആകെത്തുകയാണ്:
രണ്ട് ഘടകങ്ങളുള്ള ലായനിയുടെ കാര്യത്തിൽ, ലായകത്തിന്റെയും ലായകത്തിന്റെയും പിണ്ഡത്തിന്റെ അംശങ്ങളുടെ ആകെത്തുക എല്ലായ്പ്പോഴും 100% ആണ്:
വ്യക്തമായും, മുകളിൽ എഴുതിയ സൂത്രവാക്യങ്ങൾക്ക് പുറമേ, ഗണിതശാസ്ത്രപരമായി അവയിൽ നിന്ന് നേരിട്ട് ഉരുത്തിരിഞ്ഞ എല്ലാ സൂത്രവാക്യങ്ങളും ഒരാൾ അറിഞ്ഞിരിക്കണം. ഉദാഹരണത്തിന്:
ഒരു പദാർത്ഥത്തിന്റെ പിണ്ഡം, അളവ്, സാന്ദ്രത എന്നിവയുമായി ബന്ധപ്പെട്ട സൂത്രവാക്യം ഓർമ്മിക്കേണ്ടത് ആവശ്യമാണ്:
m = ρ∙ വി
ജലത്തിന്റെ സാന്ദ്രത 1 ഗ്രാം / മില്ലി ആണെന്നും നിങ്ങൾ അറിയേണ്ടതുണ്ട്. ഇക്കാരണത്താൽ, മില്ലിലിറ്ററിലെ ജലത്തിന്റെ അളവ് ഗ്രാമിലെ ജലത്തിന്റെ പിണ്ഡത്തിന് സംഖ്യാപരമായി തുല്യമാണ്. ഉദാഹരണത്തിന്, 10 മില്ലി വെള്ളത്തിന് 10 ഗ്രാം, 200 മില്ലി - 200 ഗ്രാം മുതലായവ പിണ്ഡമുണ്ട്.
പ്രശ്നങ്ങൾ വിജയകരമായി പരിഹരിക്കുന്നതിന്, മുകളിലുള്ള ഫോർമുലകൾ അറിയുന്നതിനു പുറമേ, അവരുടെ ആപ്ലിക്കേഷന്റെ കഴിവുകൾ യാന്ത്രികതയിലേക്ക് കൊണ്ടുവരുന്നത് വളരെ പ്രധാനമാണ്. നിരവധി വ്യത്യസ്ത ജോലികൾ പരിഹരിക്കുന്നതിലൂടെ മാത്രമേ ഇത് നേടാനാകൂ. "" ലായനിയിലെ ഒരു പദാർത്ഥത്തിന്റെ പിണ്ഡം എന്ന ആശയം ഉപയോഗിച്ചുള്ള കണക്കുകൂട്ടലുകൾ "" എന്ന വിഷയത്തെക്കുറിച്ചുള്ള യഥാർത്ഥ USE പരീക്ഷകളിൽ നിന്നുള്ള ടാസ്ക്കുകൾ പരിഹരിക്കാൻ കഴിയും.
പരിഹാരങ്ങൾക്കായുള്ള ജോലികളുടെ ഉദാഹരണങ്ങൾ
ഉദാഹരണം 1
5 ഗ്രാം ഉപ്പും 20 ഗ്രാം വെള്ളവും കലർത്തി ലഭിക്കുന്ന ലായനിയിൽ പൊട്ടാസ്യം നൈട്രേറ്റിന്റെ പിണ്ഡം കണക്കാക്കുക.
തീരുമാനം:
നമ്മുടെ കാര്യത്തിൽ ലായനി പൊട്ടാസ്യം നൈട്രേറ്റ് ആണ്, ലായകമാണ് വെള്ളം. അതിനാൽ, സൂത്രവാക്യങ്ങൾ (2), (3) എന്നിവ യഥാക്രമം ഇങ്ങനെ എഴുതാം:
m (KNO 3) \u003d 5 g, m (H 2 O) \u003d 20 g എന്നീ അവസ്ഥയിൽ നിന്ന്, അതിനാൽ:
ഉദാഹരണം 2
10% ഗ്ലൂക്കോസ് ലായനി ലഭിക്കാൻ 20 ഗ്രാം ഗ്ലൂക്കോസിൽ എന്ത് പിണ്ഡം വെള്ളം ചേർക്കണം.
തീരുമാനം:
ലായനി ഗ്ലൂക്കോസ് ആണെന്നും ലായകം വെള്ളമാണെന്നും പ്രശ്നത്തിന്റെ അവസ്ഥയിൽ നിന്ന് ഇത് പിന്തുടരുന്നു. അപ്പോൾ ഫോർമുല (4) ഞങ്ങളുടെ കാര്യത്തിൽ ഇനിപ്പറയുന്ന രീതിയിൽ എഴുതാം:
അവസ്ഥയിൽ നിന്ന്, ഗ്ലൂക്കോസിന്റെ പിണ്ഡവും (കോൺസൺട്രേഷൻ) ഗ്ലൂക്കോസിന്റെ പിണ്ഡവും നമുക്ക് അറിയാം. ജലത്തിന്റെ പിണ്ഡത്തെ x g ആയി സൂചിപ്പിക്കുന്നു, മുകളിലുള്ള ഫോർമുലയെ അടിസ്ഥാനമാക്കി നമുക്ക് ഇനിപ്പറയുന്ന തുല്യമായ സമവാക്യം എഴുതാം:
ഈ സമവാക്യം പരിഹരിക്കുമ്പോൾ നമ്മൾ x കണ്ടെത്തുന്നു:
ആ. m(H 2 O) \u003d x g \u003d 180 g
ഉത്തരം: m (H 2 O) \u003d 180 ഗ്രാം
ഉദാഹരണം 3
15% സോഡിയം ക്ലോറൈഡ് ലായനിയിൽ 150 ഗ്രാം അതേ ഉപ്പ് 20% ലായനിയിൽ 100 ഗ്രാം കലർത്തി. തത്ഫലമായുണ്ടാകുന്ന ലായനിയിൽ ഉപ്പിന്റെ പിണ്ഡം എത്രയാണ്? നിങ്ങളുടെ ഉത്തരം ഏറ്റവും അടുത്തുള്ള പൂർണ്ണസംഖ്യയ്ക്ക് നൽകുക.
തീരുമാനം:
പരിഹാരങ്ങൾ തയ്യാറാക്കുന്നതിനുള്ള പ്രശ്നങ്ങൾ പരിഹരിക്കുന്നതിന്, ഇനിപ്പറയുന്ന പട്ടിക ഉപയോഗിക്കുന്നത് സൗകര്യപ്രദമാണ്:
1st പരിഹാരം |
രണ്ടാമത്തെ പരിഹാരം |
മൂന്നാമത്തെ പരിഹാരം |
|
എം ആർ.വി. |
|||
മീറ്റർ പരിഹാരം |
|||
ω ആർ.വി. |
എവിടെ എം ആർ.വി. , m r-ra, ω r.v. ഓരോ ലായനികൾക്കും യഥാക്രമം ലയിച്ച പദാർത്ഥത്തിന്റെ പിണ്ഡം, ലായനിയുടെ പിണ്ഡം, അലിഞ്ഞുപോയ പദാർത്ഥത്തിന്റെ പിണ്ഡം എന്നിവയുടെ മൂല്യങ്ങൾ വ്യക്തിഗതമാണ്.
വ്യവസ്ഥയിൽ നിന്ന് നമുക്ക് അറിയാം:
m (1) പരിഹാരം = 150 ഗ്രാം,
ω (1) ആർ.വി. = 15%,
m (2) പരിഹാരം = 100 ഗ്രാം,
ω (1) ആർ.വി. = 20%,
ഈ മൂല്യങ്ങളെല്ലാം പട്ടികയിലേക്ക് തിരുകുമ്പോൾ, നമുക്ക് ലഭിക്കുന്നത്:
കണക്കുകൂട്ടലുകൾക്ക് ആവശ്യമായ ഇനിപ്പറയുന്ന ഫോർമുലകൾ ഞങ്ങൾ ഓർക്കണം:
ω ആർ.വി. = 100% ∙ എം ആർ.വി. / m പരിഹാരം, m r.v. = m r-ra ∙ ω r.v. / 100%, m പരിഹാരം = 100% ∙ m r.v. /ω ആർ.വി.
നമുക്ക് പട്ടിക പൂരിപ്പിക്കാൻ തുടങ്ങാം.
ഒരു വരിയിലോ നിരയിലോ ഒരു മൂല്യം മാത്രം ഇല്ലെങ്കിൽ, അത് കണക്കാക്കാം. ഒഴിവാക്കൽ ω r.v ഉള്ള വരിയാണ്., അതിന്റെ രണ്ട് സെല്ലുകളിലെ മൂല്യങ്ങൾ അറിയുമ്പോൾ, മൂന്നാമത്തേതിന്റെ മൂല്യം കണക്കാക്കാൻ കഴിയില്ല.
ആദ്യ നിരയിൽ ഒരു സെല്ലിൽ മാത്രം ഒരു മൂല്യം കാണുന്നില്ല. അതിനാൽ നമുക്ക് ഇത് കണക്കാക്കാം:
m (1) ആർ.വി. = m (1) r-ra ∙ ω (1) r.v. /100% = 150 ഗ്രാം ∙ 15%/100% = 22.5 ഗ്രാം
അതുപോലെ, രണ്ടാമത്തെ നിരയിലെ രണ്ട് സെല്ലുകളിലെ മൂല്യങ്ങൾ നമുക്കറിയാം, അതായത്:
m (2) ആർ.വി. = m (2) r-ra ∙ ω (2) r.v. /100% = 100 ഗ്രാം ∙ 20%/100% = 20 ഗ്രാം
പട്ടികയിൽ കണക്കാക്കിയ മൂല്യങ്ങൾ നൽകാം:
ഇപ്പോൾ നമുക്ക് ആദ്യ വരിയിൽ രണ്ട് മൂല്യങ്ങളും രണ്ടാമത്തെ വരിയിൽ രണ്ട് മൂല്യങ്ങളും ഉണ്ട്. അതിനാൽ നമുക്ക് നഷ്ടപ്പെട്ട മൂല്യങ്ങൾ കണക്കാക്കാം (m (3) r.v., m (3) r-ra):
m (3) ആർ.വി. = എം (1) ആർ.വി. + m (2)r.v. = 22.5 ഗ്രാം + 20 ഗ്രാം = 42.5 ഗ്രാം
m (3) പരിഹാരം = m (1) പരിഹാരം + m (2) പരിഹാരം = 150 g + 100 g = 250 g.
പട്ടികയിൽ കണക്കാക്കിയ മൂല്യങ്ങൾ നൽകാം, നമുക്ക് ലഭിക്കുന്നു:
ഇപ്പോൾ നമ്മൾ ആവശ്യമുള്ള മൂല്യം ω (3) r.v കണക്കാക്കുന്നതിനുള്ള അടുത്തെത്തിയിരിക്കുന്നു. . അത് സ്ഥിതിചെയ്യുന്ന നിരയിൽ, മറ്റ് രണ്ട് സെല്ലുകളുടെ ഉള്ളടക്കം അറിയപ്പെടുന്നു, അതിനാൽ നമുക്ക് ഇത് കണക്കാക്കാം:
ω (3) ആർ.വി. = 100% ∙ മീറ്റർ (3) ആർ.വി. / m (3) പരിഹാരം = 100% ∙ 42.5 g / 250 g = 17%
ഉദാഹരണം 4
200 ഗ്രാം 15% സോഡിയം ക്ലോറൈഡ് ലായനിയിൽ 50 മില്ലി വെള്ളം ചേർത്തു. തത്ഫലമായുണ്ടാകുന്ന ലായനിയിൽ ഉപ്പിന്റെ പിണ്ഡം എന്താണ്. നിങ്ങളുടെ ഉത്തരം അടുത്തുള്ള നൂറിലൊന്ന് _______% ലേക്ക് നൽകുക
തീരുമാനം:
ഒന്നാമതായി, ചേർത്ത വെള്ളത്തിന്റെ പിണ്ഡത്തിനുപകരം, അതിന്റെ അളവ് ഞങ്ങൾക്ക് നൽകിയിരിക്കുന്നു എന്ന വസ്തുത നിങ്ങൾ ശ്രദ്ധിക്കണം. ജലത്തിന്റെ സാന്ദ്രത 1 ഗ്രാം / മില്ലി ആണെന്ന് അറിഞ്ഞുകൊണ്ട് ഞങ്ങൾ അതിന്റെ പിണ്ഡം കണക്കാക്കുന്നു:
m ext. (H 2 O) = V ext. (H 2 O) ∙ ρ (H2O) = 50 മില്ലി ∙ 1 ഗ്രാം/മില്ലി = 50 ഗ്രാം
യഥാക്രമം 0 ഗ്രാം സോഡിയം ക്ലോറൈഡ് അടങ്ങിയ 0% സോഡിയം ക്ലോറൈഡ് ലായനിയായി ഞങ്ങൾ ജലത്തെ പരിഗണിക്കുകയാണെങ്കിൽ, മുകളിലുള്ള ഉദാഹരണത്തിലെ അതേ പട്ടിക ഉപയോഗിച്ച് പ്രശ്നം പരിഹരിക്കാനാകും. നമുക്ക് അത്തരമൊരു പട്ടിക വരച്ച് അതിൽ നമുക്കറിയാവുന്ന മൂല്യങ്ങൾ തിരുകാം:
ആദ്യ നിരയിൽ, രണ്ട് മൂല്യങ്ങൾ അറിയാം, അതിനാൽ നമുക്ക് മൂന്നാമത്തേത് കണക്കാക്കാം:
m (1) ആർ.വി. = m (1) r-ra ∙ ω (1) r.v. /100% = 200 ഗ്രാം ∙ 15%/100% = 30 ഗ്രാം,
രണ്ടാമത്തെ വരിയിൽ, രണ്ട് മൂല്യങ്ങളും അറിയപ്പെടുന്നു, അതിനാൽ നമുക്ക് മൂന്നാമത്തേത് കണക്കാക്കാം:
m (3) പരിഹാരം = m (1) പരിഹാരം + m (2) പരിഹാരം = 200 g + 50 g = 250 g,
ഉചിതമായ സെല്ലുകളിൽ കണക്കാക്കിയ മൂല്യങ്ങൾ നൽകുക:
ഇപ്പോൾ ആദ്യ വരിയിലെ രണ്ട് മൂല്യങ്ങൾ അറിയപ്പെടുന്നു, അതായത് m (3) r.v യുടെ മൂല്യം നമുക്ക് കണക്കാക്കാം. മൂന്നാമത്തെ സെല്ലിൽ:
m (3) ആർ.വി. = എം (1) ആർ.വി. + m (2)r.v. = 30 ഗ്രാം + 0 ഗ്രാം = 30 ഗ്രാം
ω (3) ആർ.വി. = 30/250 ∙ 100% = 12%.
രാസ സൂത്രവാക്യം അറിയുന്നതിലൂടെ, ഒരു പദാർത്ഥത്തിലെ രാസ മൂലകങ്ങളുടെ പിണ്ഡം നിങ്ങൾക്ക് കണക്കാക്കാം. പദാർത്ഥങ്ങളിലെ മൂലകത്തെ ഗ്രീക്ക് സൂചിപ്പിക്കുന്നു. "ഒമേഗ" - ω E / V എന്ന അക്ഷരം ഫോർമുല ഉപയോഗിച്ച് കണക്കാക്കുന്നു:
ഇവിടെ k എന്നത് തന്മാത്രയിലെ ഈ മൂലകത്തിന്റെ ആറ്റങ്ങളുടെ എണ്ണമാണ്.
ജലത്തിലെ ഹൈഡ്രജന്റെയും ഓക്സിജന്റെയും പിണ്ഡം എത്രയാണ് (H 2 O)?
തീരുമാനം:
M r (H 2 O) \u003d 2 * A r (H) + 1 * A r (O) \u003d 2 * 1 + 1 * 16 \u003d 18
2) ജലത്തിലെ ഹൈഡ്രജന്റെ പിണ്ഡം കണക്കാക്കുക:
3) വെള്ളത്തിൽ ഓക്സിജന്റെ പിണ്ഡം കണക്കാക്കുക. ജലത്തിന്റെ ഘടനയിൽ രണ്ട് രാസ മൂലകങ്ങളുടെ ആറ്റങ്ങൾ മാത്രമുള്ളതിനാൽ, ഓക്സിജന്റെ പിണ്ഡം ഇതിന് തുല്യമായിരിക്കും:

അരി. 1. പ്രശ്നത്തിന്റെ പരിഹാരത്തിന്റെ രൂപീകരണം 1
H 3 PO 4 എന്ന പദാർത്ഥത്തിലെ മൂലകങ്ങളുടെ പിണ്ഡം കണക്കാക്കുക.
1) പദാർത്ഥത്തിന്റെ ആപേക്ഷിക തന്മാത്രാ ഭാരം കണക്കാക്കുക:
M r (H 3 RO 4) \u003d 3 * A r (H) + 1 * A r (P) + 4 * A r (O) \u003d 3 * 1 + 1 * 31 + 4 * 16 \u003d 98
2) പദാർത്ഥത്തിലെ ഹൈഡ്രജന്റെ പിണ്ഡം ഞങ്ങൾ കണക്കാക്കുന്നു:
3) പദാർത്ഥത്തിലെ ഫോസ്ഫറസിന്റെ പിണ്ഡം കണക്കാക്കുക:
4) പദാർത്ഥത്തിലെ ഓക്സിജന്റെ പിണ്ഡം കണക്കാക്കുക:
1. രസതന്ത്രത്തിലെ ജോലികളുടെയും വ്യായാമങ്ങളുടെയും ശേഖരണം: 8-ാം ഗ്രേഡ്: പാഠപുസ്തകത്തിലേക്ക് പി.എ. ഒർഷെക്കോവ്സ്കിയും മറ്റുള്ളവരും. "കെമിസ്ട്രി, ഗ്രേഡ് 8" / പി.എ. ഒർഷെക്കോവ്സ്കി, എൻ.എ. ടിറ്റോവ്, എഫ്.എഫ്. ഹെഗൽ. - എം.: AST: ആസ്ട്രൽ, 2006.
2. ഉഷകോവ ഒ.വി. കെമിസ്ട്രി വർക്ക്ബുക്ക്: എട്ടാം ക്ലാസ്: പാഠപുസ്തകത്തിലേക്ക് പി.എ. ഒർഷെക്കോവ്സ്കിയും മറ്റുള്ളവരും. "രസതന്ത്രം. ഗ്രേഡ് 8" / ഒ.വി. ഉഷക്കോവ, പി.ഐ. ബെസ്പലോവ്, പി.എ. ഒർഷെക്കോവ്സ്കി; കീഴിൽ. ed. പ്രൊഫ. പി.എ. Orzhekovsky - M .: AST: Astrel: Profizdat, 2006. (p. 34-36)
3. രസതന്ത്രം: എട്ടാം ക്ലാസ്: പാഠപുസ്തകം. ജനറൽ വേണ്ടി സ്ഥാപനങ്ങൾ / പി.എ. ഒർഷെക്കോവ്സ്കി, എൽ.എം. മെഷ്ചെര്യാക്കോവ, എൽ.എസ്. പോണ്ടക്. എം.: AST: Astrel, 2005.(§15)
4. കുട്ടികൾക്കുള്ള എൻസൈക്ലോപീഡിയ. വാല്യം 17. രസതന്ത്രം / അധ്യായം. എഡിറ്റ് ചെയ്തത് വി.എ. വോലോഡിൻ, നേതൃത്വം. ശാസ്ത്രീയമായ ed. I. ലീൻസൺ. - എം.: അവന്ത +, 2003.
1. ഡിജിറ്റൽ വിദ്യാഭ്യാസ വിഭവങ്ങളുടെ ഒരൊറ്റ ശേഖരം ().
2. ജേർണലിന്റെ ഇലക്ട്രോണിക് പതിപ്പ് "കെമിസ്ട്രി ആൻഡ് ലൈഫ്" ().
4. "ഒരു പദാർത്ഥത്തിലെ രാസ മൂലകത്തിന്റെ മാസ് ഫ്രാക്ഷൻ" () എന്ന വിഷയത്തെക്കുറിച്ചുള്ള വീഡിയോ പാഠം.
ഹോംവർക്ക്
1. പേജ്.78 നമ്പർ 2"രസതന്ത്രം: എട്ടാം ഗ്രേഡ്" എന്ന പാഠപുസ്തകത്തിൽ നിന്ന് (പി.എ. ഒർഷെക്കോവ്സ്കി, എൽ.എം. മെഷ്ചെറിയാക്കോവ, എൽ.എസ്. പോണ്ടക്. എം.: എഎസ്ടി: ആസ്ട്രൽ, 2005).
2. കൂടെ. 34-36 നമ്പർ 3.5രസതന്ത്രത്തിലെ വർക്ക്ബുക്കിൽ നിന്ന്: എട്ടാം ക്ലാസ്: പി.എയുടെ പാഠപുസ്തകത്തിലേക്ക്. ഒർഷെക്കോവ്സ്കിയും മറ്റുള്ളവരും. "രസതന്ത്രം. ഗ്രേഡ് 8" / ഒ.വി. ഉഷക്കോവ, പി.ഐ. ബെസ്പലോവ്, പി.എ. ഒർഷെക്കോവ്സ്കി; കീഴിൽ. ed. പ്രൊഫ. പി.എ. Orzhekovsky - M.: AST: Astrel: Profizdat, 2006.
ചില പദാർത്ഥങ്ങളിലെ ഒരു പ്രത്യേക മൂലകത്തിന്റെ ഉള്ളടക്കമാണ് പിണ്ഡത്തിന്റെ ഭിന്നസംഖ്യയെന്ന് രസതന്ത്രത്തിന്റെ ഗതിയിൽ നിന്ന് അറിയാം. ഒരു സാധാരണ വേനൽക്കാല താമസക്കാരന് അത്തരം അറിവ് ഉപയോഗപ്രദമല്ലെന്ന് തോന്നുന്നു. എന്നാൽ പേജ് അടയ്ക്കാൻ തിരക്കുകൂട്ടരുത്, കാരണം ഒരു തോട്ടക്കാരന് പിണ്ഡം കണക്കാക്കാനുള്ള കഴിവ് വളരെ ഉപയോഗപ്രദമാകും. എന്നിരുന്നാലും, ആശയക്കുഴപ്പത്തിലാകാതിരിക്കാൻ, എല്ലാം ക്രമത്തിൽ സംസാരിക്കാം."പിണ്ഡത്തിന്റെ ഭിന്നസംഖ്യ" എന്ന ആശയത്തിന്റെ അർത്ഥമെന്താണ്?
പിണ്ഡത്തിന്റെ അംശം ഒരു ശതമാനമായി അല്ലെങ്കിൽ പത്തിലൊന്നിൽ അളക്കുന്നു. കുറച്ചുകൂടി ഉയരത്തിൽ, ഞങ്ങൾ ക്ലാസിക് നിർവചനത്തെക്കുറിച്ച് സംസാരിച്ചു, അത് റഫറൻസ് പുസ്തകങ്ങളിലോ വിജ്ഞാനകോശങ്ങളിലോ സ്കൂൾ കെമിസ്ട്രി പാഠപുസ്തകങ്ങളിലോ കാണാം. എന്നാൽ പറഞ്ഞതിന്റെ സാരാംശം മനസ്സിലാക്കുക അത്ര ലളിതമല്ല. അതിനാൽ, നമുക്ക് 500 ഗ്രാം ചില സങ്കീർണ്ണ പദാർത്ഥങ്ങൾ ഉണ്ടെന്ന് കരുതുക. ഈ കേസിൽ കോംപ്ലക്സ് അർത്ഥമാക്കുന്നത് അത് രചനയിൽ ഏകതാനമല്ല എന്നാണ്. വലിയതോതിൽ, നമ്മൾ ഉപയോഗിക്കുന്ന ഏതൊരു പദാർത്ഥവും സങ്കീർണ്ണമാണ്, ലളിതമായ ടേബിൾ ഉപ്പ് പോലും, അതിന്റെ ഫോർമുല NaCl ആണ്, അതായത് അതിൽ സോഡിയം, ക്ലോറിൻ തന്മാത്രകൾ അടങ്ങിയിരിക്കുന്നു. ടേബിൾ ഉപ്പിന്റെ ഉദാഹരണത്തിൽ ഞങ്ങൾ ന്യായവാദം തുടരുകയാണെങ്കിൽ, 500 ഗ്രാം ഉപ്പിൽ 400 ഗ്രാം സോഡിയം അടങ്ങിയിട്ടുണ്ടെന്ന് നമുക്ക് അനുമാനിക്കാം. അപ്പോൾ അതിന്റെ പിണ്ഡം 80% അല്ലെങ്കിൽ 0.8 ആയിരിക്കും.
ഒരു തോട്ടക്കാരന് ഇത് ആവശ്യമായി വരുന്നത് എന്തുകൊണ്ട്?
ഈ ചോദ്യത്തിനുള്ള ഉത്തരം നിങ്ങൾക്ക് ഇതിനകം അറിയാമെന്ന് ഞാൻ കരുതുന്നു. എല്ലാത്തരം പരിഹാരങ്ങളും മിശ്രിതങ്ങളും മറ്റും തയ്യാറാക്കുന്നത് ഏതൊരു തോട്ടക്കാരന്റെയും സാമ്പത്തിക പ്രവർത്തനത്തിന്റെ അവിഭാജ്യ ഘടകമാണ്. പരിഹാരങ്ങൾ, വളങ്ങൾ, വിവിധ പോഷക മിശ്രിതങ്ങൾ, മറ്റ് തയ്യാറെടുപ്പുകൾ എന്നിവയുടെ രൂപത്തിൽ ഉപയോഗിക്കുന്നു, ഉദാഹരണത്തിന്, വളർച്ചാ ഉത്തേജകങ്ങളായ "എപിൻ", "കോർനെവിൻ" മുതലായവ. കൂടാതെ, സിമൻറ്, മണൽ, മറ്റ് ഘടകങ്ങൾ എന്നിവ പോലുള്ള ഉണങ്ങിയ പദാർത്ഥങ്ങൾ അല്ലെങ്കിൽ സാധാരണ പൂന്തോട്ട മണ്ണ് വാങ്ങിയ കെ.ഇ. അതേ സമയം, മിക്ക നിർദ്ദേശങ്ങളിലും തയ്യാറാക്കിയ ലായനികളിലോ മിശ്രിതങ്ങളിലോ ഈ ഏജന്റുമാരുടെയും തയ്യാറെടുപ്പുകളുടെയും ശുപാർശ ചെയ്യുന്ന ഏകാഗ്രത ബഹുജന ഭിന്നസംഖ്യകളിൽ നൽകിയിരിക്കുന്നു.
അതിനാൽ, ഒരു പദാർത്ഥത്തിലെ ഒരു മൂലകത്തിന്റെ പിണ്ഡം എങ്ങനെ കണക്കാക്കാമെന്ന് അറിയുന്നത് വേനൽക്കാല നിവാസികൾക്ക് ആവശ്യമായ വളം അല്ലെങ്കിൽ പോഷക മിശ്രിതം ശരിയായി തയ്യാറാക്കാൻ സഹായിക്കും, ഇത് ഭാവിയിലെ വിളവെടുപ്പിനെ ബാധിക്കും.
കണക്കുകൂട്ടൽ അൽഗോരിതം
അതിനാൽ, ഒരു വ്യക്തിഗത ഘടകത്തിന്റെ പിണ്ഡത്തിന്റെ പിണ്ഡത്തിന്റെ അനുപാതം ഒരു ലായനി അല്ലെങ്കിൽ പദാർത്ഥത്തിന്റെ ആകെ പിണ്ഡത്തിലേക്കുള്ള അനുപാതമാണ്. ലഭിച്ച ഫലം ഒരു ശതമാനമായി പരിവർത്തനം ചെയ്യണമെങ്കിൽ, അത് 100 കൊണ്ട് ഗുണിക്കണം. അതിനാൽ, പിണ്ഡത്തിന്റെ ഭിന്നസംഖ്യ കണക്കാക്കുന്നതിനുള്ള സൂത്രവാക്യം ഇനിപ്പറയുന്ന രീതിയിൽ എഴുതാം:
W = പദാർത്ഥത്തിന്റെ പിണ്ഡം / ലായനിയുടെ പിണ്ഡം
W = (ദ്രവ്യത്തിന്റെ പിണ്ഡം / ലായനിയുടെ പിണ്ഡം) x 100%.
ബഹുജന ഭിന്നസംഖ്യ നിർണ്ണയിക്കുന്നതിനുള്ള ഒരു ഉദാഹരണം
നമുക്ക് ഒരു പരിഹാരമുണ്ടെന്ന് കരുതുക, തയ്യാറാക്കുന്നതിനായി 5 ഗ്രാം NaCl 100 മില്ലി വെള്ളത്തിൽ ചേർത്തു, ഇപ്പോൾ ടേബിൾ ഉപ്പിന്റെ സാന്ദ്രത കണക്കാക്കേണ്ടത് ആവശ്യമാണ്, അതായത്, അതിന്റെ പിണ്ഡം. പദാർത്ഥത്തിന്റെ പിണ്ഡം നമുക്കറിയാം, തത്ഫലമായുണ്ടാകുന്ന ലായനിയുടെ പിണ്ഡം രണ്ട് പിണ്ഡങ്ങളുടെ ആകെത്തുകയാണ് - ഉപ്പും വെള്ളവും 105 ഗ്രാം തുല്യമാണ്. അങ്ങനെ, ഞങ്ങൾ 5 ഗ്രാം 105 ഗ്രാം കൊണ്ട് ഹരിച്ച് ഫലം 100 കൊണ്ട് ഗുണിച്ച് ആവശ്യമുള്ള മൂല്യം നേടുക. 4.7%. ഉപ്പുവെള്ള ലായനിയിൽ ഉണ്ടാകുന്ന ഏകാഗ്രത ഇതാണ്.
കൂടുതൽ പ്രായോഗിക ചുമതല
പ്രായോഗികമായി, വേനൽ റസിഡന്റ് പലപ്പോഴും വ്യത്യസ്ത തരത്തിലുള്ള ജോലികൾ കൈകാര്യം ചെയ്യേണ്ടതുണ്ട്. ഉദാഹരണത്തിന്, ഒരു രാസവളത്തിന്റെ ജലീയ ലായനി തയ്യാറാക്കേണ്ടത് ആവശ്യമാണ്, അതിന്റെ സാന്ദ്രത ഭാരം 10% ആയിരിക്കണം. ശുപാർശ ചെയ്യുന്ന അനുപാതങ്ങൾ കൃത്യമായി നിരീക്ഷിക്കുന്നതിന്, പദാർത്ഥത്തിന്റെ അളവ് എത്രയാണെന്നും അത് ഏത് അളവിൽ വെള്ളത്തിൽ ലയിപ്പിക്കണമെന്നും നിങ്ങൾ നിർണ്ണയിക്കേണ്ടതുണ്ട്.
പ്രശ്നത്തിന്റെ പരിഹാരം വിപരീത ക്രമത്തിൽ ആരംഭിക്കുന്നു. ആദ്യം, നിങ്ങൾ ഒരു ശതമാനമായി പ്രകടിപ്പിക്കുന്ന പിണ്ഡത്തെ 100 കൊണ്ട് ഹരിക്കണം. തൽഫലമായി, നമുക്ക് W \u003d 0.1 ലഭിക്കുന്നു - ഇത് യൂണിറ്റുകളിലെ പദാർത്ഥത്തിന്റെ പിണ്ഡത്തിന്റെ അംശമാണ്. ഇനി നമുക്ക് പദാർത്ഥത്തിന്റെ അളവ് x ആയി സൂചിപ്പിക്കാം, ലായനിയുടെ അന്തിമ പിണ്ഡം - M. ഈ സാഹചര്യത്തിൽ, അവസാന മൂല്യം രണ്ട് പദങ്ങളാൽ നിർമ്മിതമാണ് - ജലത്തിന്റെ പിണ്ഡവും വളത്തിന്റെ പിണ്ഡവും. അതായത്, M = Mv + x. അങ്ങനെ, നമുക്ക് ഒരു ലളിതമായ സമവാക്യം ലഭിക്കും:
W = x / (Mv + x)
x-നായി ഇത് പരിഹരിക്കുമ്പോൾ, നമുക്ക് ലഭിക്കുന്നത്:
x \u003d W x Mv / (1 - W)
ലഭ്യമായ ഡാറ്റയ്ക്ക് പകരമായി, ഞങ്ങൾക്ക് ഇനിപ്പറയുന്ന ആശ്രിതത്വം ലഭിക്കും:
x \u003d 0.1 x Mv / 0.9
അതിനാൽ, ലായനി തയ്യാറാക്കാൻ ഞങ്ങൾ 1 ലിറ്റർ (അതായത്, 1000 ഗ്രാം) വെള്ളം എടുക്കുകയാണെങ്കിൽ, ആവശ്യമുള്ള സാന്ദ്രതയുടെ പരിഹാരം തയ്യാറാക്കാൻ ഏകദേശം 111-112 ഗ്രാം വളം ആവശ്യമാണ്.
നേർപ്പിക്കുകയോ കൂട്ടിച്ചേർക്കുകയോ ചെയ്യുന്നതിലൂടെ പ്രശ്നങ്ങൾ പരിഹരിക്കുന്നു
നമുക്ക് 10 ലിറ്റർ (10,000 ഗ്രാം) റെഡിമെയ്ഡ് ജലീയ ലായനി ഉണ്ടെന്ന് കരുതുക, അതിൽ ഒരു നിശ്ചിത പദാർത്ഥത്തിന്റെ സാന്ദ്രത W1 = 30% അല്ലെങ്കിൽ 0.3 ആണ്. സാന്ദ്രത W2 = 15% അല്ലെങ്കിൽ 0.15 ആയി കുറയുന്നതിന് അതിൽ എത്ര വെള്ളം ചേർക്കേണ്ടതുണ്ട്? ഈ സാഹചര്യത്തിൽ, ഫോർമുല സഹായിക്കും:
Mv \u003d (W1x M1 / W2) - M1
പ്രാരംഭ ഡാറ്റയ്ക്ക് പകരമായി, ചേർത്ത വെള്ളത്തിന്റെ അളവ് ഇതായിരിക്കണം:
Mv \u003d (0.3 x 10,000 / 0.15) - 10,000 \u003d 10,000 ഗ്രാം
അതായത്, നിങ്ങൾ അതേ 10 ലിറ്റർ ചേർക്കേണ്ടതുണ്ട്.
ഇപ്പോൾ വിപരീത പ്രശ്നം സങ്കൽപ്പിക്കുക - W1 = 10% അല്ലെങ്കിൽ 0.1 എന്ന സാന്ദ്രതയിൽ 10 ലിറ്റർ ജലീയ ലായനി (M1 = 10,000 ഗ്രാം) ഉണ്ട്. വളം W2 = 20% അല്ലെങ്കിൽ 0.2 ന്റെ പിണ്ഡം ഉപയോഗിച്ച് ഒരു പരിഹാരം നേടേണ്ടത് ആവശ്യമാണ്. എത്ര പ്രാരംഭ മെറ്റീരിയൽ ചേർക്കണം? ഇത് ചെയ്യുന്നതിന്, നിങ്ങൾ ഫോർമുല ഉപയോഗിക്കേണ്ടതുണ്ട്:
x \u003d M1 x (W2 - W1) / (1 - W2)
യഥാർത്ഥ മൂല്യത്തിന് പകരമായി, നമുക്ക് x \u003d 1 125 ഗ്രാം ലഭിക്കും.
അതിനാൽ, സ്കൂൾ രസതന്ത്രത്തിന്റെ ഏറ്റവും ലളിതമായ അടിസ്ഥാനങ്ങളെക്കുറിച്ചുള്ള അറിവ് വളം പരിഹാരങ്ങൾ, നിരവധി ഘടകങ്ങളിൽ നിന്നുള്ള പോഷക അടിവസ്ത്രങ്ങൾ അല്ലെങ്കിൽ നിർമ്മാണ പ്രവർത്തനങ്ങൾക്ക് മിശ്രിതങ്ങൾ എന്നിവ ശരിയായി തയ്യാറാക്കാൻ തോട്ടക്കാരനെ സഹായിക്കും.