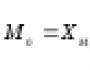Lomonosovin suosikkitiede on kemia. "Kemia levittää kätensä inhimillisissä asioissa... Minne katsomme, minne katsomme, minne käännymme
Aivorengas kemiassa
"Kemia ojentaa kätensä miesten asioihin."
Laajenna tietämystä kemiasta, herätä kiinnostusta tieteeseen
Kehitä luovia kykyjä
Kehitä parityöskentelykykyä
Osallistujat: 9-10 luokkien opiskelijat
1. Opettajan johdantopuhe.
Hei kaverit! Kutsuimme sinut tänään todistamaan kilpailua kekseliäisyydestä, iloisuudesta ja myös kemian aineen tuntemuksesta 9. ja 10. luokkien joukkueiden välillä.
Ja siksi haluan muistuttaa, että tänään pidämme 6 kierroksen "BRAIN RINGiä".
Hyvät fanit, tänään voit kysyä, antaa itsenäisiä vastauksia ja voit osallistua 6. kierrokseen, taistella tulevien voittajien kanssa.
Aivorenkaamme seuraa JURYmme:…….
Ryhmätervehdyksiä arvioidaan viiden pisteen järjestelmässä
Joten, annetaan nyt puheenvuoro joukkueillemme.
I. KIERROS "Hienot kemistit"
1. Lue kemiallisten yhdisteiden koostumuksen pysyvyyden laki ja nimeä ranskalainen tiedemies, joka löysi tämän lain. (Vastaus: Proust Joseph Louis)
2. Lisää numero 3. ryhmän kemiallisten alkuaineiden nimeen saadaksesi venäläisen tiedemiehen - kemistin ja säveltäjän - nimen.
(Vastaus: Bor-one \u003d Borodin Alexander Porfiryevich 12. 11. 1833–27. 02. 87)
3. Pietari Suuri sanoi: "Näen aavistuksen, että venäläiset jonakin päivänä ja ehkä jopa meidän elinaikanamme häpeävät valistuneimpia kansoja tieteiden menestyksellä, väsymättömyydellä työnteossa sekä lujan ja äänekkään kunnian majesteettisuudella."
Kysymys. Nyt sinun on päätettävä kenelle nämä säkeet kuuluvat ja kerrottava hyvin lyhyesti, millainen henkilö tämä on.
"Oi sinä, joka odotat
Isänmaa sisimmästään
Ja haluaa nähdä ne
jota hän kutsuu vieraiden leireistä,
Oi, päiväsi ovat siunattuja!
Uskalla nyt rohkaista,
Näytä huolellasi
Mikä voi omistaa Platoksen
Ja Newtonien nopea mieli
Venäjän maa synnyttää. Vastaus. M. V. Lomonosov
5. A. A. Voskresensky työskenteli Pietarin Main Pedagogical Institutessa, luennoi Institute of Communicationsissa, Corps of Pagesissa ja Engineering Academyssa. Vuosina 1838-1867 opetti Pietarin yliopistossa.
Kysymys. Mikä on hänen kuuluisimman oppilaansa nimi? Kiitollinen oppilas kutsui opettajaansa "venäläisen kemian isoisäksi".
Vastaus: D. I. Mendelejev.
6. Anna suosikkisanosi A. A. Voskresenskyltä, jonka D. I. Mendelejev toisti usein.
Vastaus: "Jumalat eivät polta ruukkuja eivätkä tee tiiliä."
7. Kuka ja milloin ehdotti yksinkertaista ja ymmärrettävää aakkosmerkkijärjestelmää kemiallisten yhdisteiden atomikoostumuksen ilmaisemiseksi. Kuinka monta vuotta kemiallisia symboleja on käytetty.
Vastaus: 1814 ruotsalainen tiedemies Jan Berzelius. Kyltit ovat olleet käytössä 194 vuotta.
Tuomariston sana
II KIERROS "Hapot"
1. Mikä happo ja sen suolat palvelivat sodan ja tuhon aihetta useiden vuosisatojen ajan.
Vastaus: Typpihappo.
2. Nimeä vähintään 5 happoa, joita ihminen syö.
Vastaus: Askorbiini, sitruuna, etikka, maitohappo, omena, valeriaani, oksaali ...
3. Mikä on "vitrioli"?
Vastaus: rikkihappoa (pl. 1, 84, 96, 5 % öljyisen ulkonäön vuoksi saatiin rautasulfaatista (1700-luvun puoliväliin asti).)
4. On olemassa happosateen käsite. Onko mahdollista hapanlunta, sumua tai kastetta? Selitä tämä ilmiö.
Soitamme ensin kissalle
Toinen on vesipatsaan mittaaminen,
Unioni kolmannelle menee meille
Ja tulla kokonaiseksi
Vastaus. Acid
"Mustanmeren salaisuus" Yu. Kuznetsov.
Ravistelee Krimiä kahdentenakymmenentenäkahdeksantena vuonna,
Ja meri nousi
Antaen kansojen kauhun,
Tuliset rikkipilarit.
Kaikki on mennyt. Taas vaahto kävelee,
Mutta siitä lähtien kaikki on korkeampaa, kaikki on tiheämpää
Synkkä rikkigehenna
Lähestyy laivojen pohjaa.
(!?) Kirjoita kaavioita tässä jaksossa tapahtuvasta mahdollisesta OVR:stä.
Vastaus: 2H2S+O2=2H20+2S+Q
S+O2=SO2
2H2+3O2=H2O+302+Q
III. PYÖRISTÄ (P, S, O, N,)
1. "Kyllä! Se oli koira, valtava, musta kuin piki. Mutta kukaan meistä kuolevaisista ei ollut koskaan nähnyt sellaista koiraa. Sen avoimesta suusta leimahti liekkejä, sen silmistä lensi kipinöitä, sen kuonolle levisi välkkyvä tuli ja niska. tulehtuneilla aivoilla ei voisi olla kauheampaa, inhottavampaa näkemystä kuin tämä helvetinen olento, joka hyppäsi sumusta meille... Kauhea koira, nuoren leijonan kokoinen. Sen valtava suu hehkui edelleen sinertävällä liekillä , syvälle asettuneet silmät kosketin tätä valoisaa päätä ja oten käteni pois, näin, että myös sormeni hehkuivat pimeydessä.
Oppinut? Arthur Conan Doyle "Baskervillen koira"
(!?) Mikä elementti tähän huonoon tarinaan liittyy? Anna lyhyt kuvaus tästä elementistä.
Vastaus: PSHE.1669:n sijainnin mukaan alkemisti Brand löysi valkoisen fosforin. Sen kyvystä hehkua pimeässä hän kutsui sitä "kylmäksi tuleksi".
2. Kuinka poistaa nitraatit vihanneksista? Ehdota vähintään kolmea tapaa.
Vastaus: 1. Nitraatit liukenevat veteen, vihannekset voidaan liottaa veteen.2. Kuumennettaessa nitraatit hajoavat, joten vihannekset on kypsennettävä.
3. Mitä Venäjän kaupunkia kutsutaan kiviraaka-aineeksi fosfaattilannoitteiden valmistukseen?
Vastaus: Apatity, Murmanskin alue.
4. Kuten tiedät, antiikin erinomainen luonnontieteilijä Plinius Vanhin kuoli vuonna 79 jKr. tulivuorenpurkauksen aikana. Hänen veljenpoikansa kirjoitti kirjeessään historioitsija Tacitukselle "...Yhtäkkiä jyrisi ukkonen ja mustia rikkihöyryjä vierivät alas vuoren liekistä. Kaikki pakenivat. Plinius nousi ylös ja nojaten kahteen orjaan, ajatteli myös lähteä; mutta tappava höyry ympäröi häntä joka puolelta, hänen polvensa vääntyivät, hän kaatui jälleen ja tukehtui.
Kysymys. Mitkä olivat ne rikkihöyryt, jotka tappoivat Pliniusin?
Vastaus: 1) 0,01 % rikkivetyä ilmassa tappaa ihmisen melkein välittömästi. 2) rikkioksidi (IV).
5. Haluatpa sitten valkaista katot, kuparoida esineen tai tappaa tuholaisia puutarhassasi, tummansiniset kiteet ovat välttämättömiä.
Kysymys. Anna yhdisteen kaava, joka muodostaa nämä kiteet.
Vastaus. Kuparivitrioli. CuSO4 * 5 H2O.
Tuomariston sana
IV. ROUND - kysymys - vastaus
Mikä elementti on aina onnellinen? (radon)
Mitkä alkuaineet väittävät "voi synnyttää muita aineita" (hiili, vety, happi)
Millainen on ympäristö, kun natriumkarbonaatti liuotetaan veteen? (emäksinen)
Mikä on positiivisesti varautuneen hiukkasen nimi, joka muodostuu, kun virta johdetaan elektrolyyttiliuoksen (kationin) läpi?
Mikä kemiallinen alkuaine on osa rakennetta, jonka Tom Sawyer joutui maalaamaan (aita - boori)
Minkä metallin nimi kantaa taikuria (magnesiumtaikuri)
V. PYÖRÄS (As , Sb ,Bi )
1. Rikoslainsäädäntö on aina nostanut myrkytyksen muiden murhien joukosta erityisen vakavana rikoksena. Rooman laki näki myrkytyksen murhan ja petoksen yhdistelmänä. Kanonin laki asetti myrkytyksen noituuden rinnalle. XIV vuosisadan koodeissa. Myrkytyksestä määrättiin erityisen pelottava kuolemanrangaistus - miehille pyöräily ja naisille hukkuminen alustavaan kidutukseen.
Se toimii eri aikoina, eri olosuhteissa, eri muodoissa myrkkynä ja ainutlaatuisena parantavana aineena, haitallisena ja vaarallisena jätetuotteena, hyödyllisimpien, korvaamattomien aineiden komponenttina.
Kysymys. Mistä kemiallisesta alkuaineesta puhumme, mikä on sarjanumero ja sen suhteellinen atomimassa.
Vastaus. Arseeni. Ar = 34.
2. Mistä kroonisesta sairaudesta tina kärsii? Mikä metalli pystyy parantamaan taudin?
Vastaus. Tina muuttuu jauheeksi matalissa lämpötiloissa – "tinarutto". Vismutti (antimoni ja lyijy) atomit, kun niitä lisätään tinaan, sementoivat sen kidehilan pysäyttäen "tinaruton".
3. Mitä kemiallista alkuainetta alkemistit kuvasivat vääntelevänä käärmeenä?
Vastaus. Keskiajalla vääntelevän käärmeen avulla arseenia kuvattiin, mikä korosti sen myrkyllisyyttä.
5. Mitä kemiallista alkuainetta alkemistit kuvasivat sudena suu auki?
Vastaus. Antimonia kuvattiin suden muodossa, jolla on avoin suu. Hän sai tämän symbolin kyvystään liuottaa metalleja ja erityisesti kultaa.
6. Yhdistämällä mitä kemikaalia esim. Myrkytettiinkö Napoleon?
Vastaus. Arseeni.
VI. ROUND (Kemia jokapäiväisessä elämässä)
1. Mitä ilman et voi leipoa hapan omenapiirakkaa?
Vastaus. Ei soodaa.
2. Ilman mitä ainetta on mahdotonta silittää ylikuivuneita tavaroita?
Vastaus. Ilman vettä.
3. Nimeä metalli, joka on huoneenlämmössä nestemäisessä tilassa.
Vastaus. Merkurius.
4. Mitä ainetta käytetään liian happaman maaperän käsittelyyn?
Vastaus. Lime.
5. Palaako sokeri? Kokeile.
Vastaus. Kaikki aineet palavat. Mutta sokerin sytyttämiseen tarvitset katalyytin - savukkeen tuhkaa.
6. Muinaisista ajoista lähtien ihmiskunta on käyttänyt säilöntäaineita ruoan säilöntään. Nimeä tärkeimmät säilöntäaineet.
Vastaus. Suola, savu, hunaja, öljy, etikka.
Sillä aikaa kun JURY laskee kilpailujen tuloksia ja julkistaa voittajan, esitän faneille kysymyksiä:
Millaista maitoa ei juota? (kalkkikivi)
Mikä elementti on elottoman luonnon perusta? (vety)
Mikä vesi liuottaa kultaa? (aqua regia)
Mistä elementistä yksinkertaisen aineen muodossa he maksavat joskus enemmän kuin kullasta, sitten päinvastoin he maksavat päästäkseen eroon siitä? (elohopea)
Mikä on allotropia? Antaa esimerkkejä.
Mikä on jäähappo? (etikka)
Mikä alkoholi ei pala? (ammoniakki)
Mikä on valkokulta? (kullan ja platinan, nikkelin tai hopean seos)
JURYn sana.
Voittajan palkintojenjakotilaisuus

Bensiinin puhdistus vedestä.
Kaadoin bensaa tölkkiin, sitten unohdin sen ja menin kotiin. Kanisteri jätettiin auki. Sade on tulossa.
Seuraavana päivänä halusin ajaa mönkijällä ja muistin kaasukanisterin. Kun lähestyin sitä, tajusin, että siinä oleva bensiini oli sekoittunut veteen, koska eilen siinä oli selvästi vähemmän nestettä. Minun piti erottaa vesi ja bensiini. Ymmärsin, että vesi jäätyy korkeammassa lämpötilassa kuin bensiini, laitoin bensiinipurkin jääkaappiin. Jääkaapissa bensiinin lämpötila on -10 celsiusastetta. Hetken kuluttua otin kanisterin jääkaapista. Kanisteri sisälsi jäätä ja bensiiniä. Kaadoin bensaa verkon läpi toiseen kanisteriin. Näin ollen kaikki jää jäi ensimmäiseen kanisteriin. Nyt voisin kaataa jalostettua bensiiniä ATV:n bensatankkiin ja lopulta ajaa sillä. Jäätyessään (eri lämpötiloissa) tapahtui aineiden erottuminen.
Kulgashov Maxim.
Nykymaailmassa ihmisen elämää ei voida kuvitella ilman kemiallisia prosesseja. Jopa esimerkiksi Pietari Suuren aikana oli kemiaa.
Jos ihmiset eivät oppisi sekoittamaan erilaisia kemiallisia alkuaineita, ei olisi kosmetiikkaa. Monet tytöt eivät ole niin kauniita kuin miltä näyttävät. Lapset eivät pystyisi veistämään muovailuvahasta. Muovisia leluja ei olisi. Autot eivät kulje ilman bensaa. Asioiden peseminen on paljon vaikeampaa ilman pesujauhetta.
Jokainen kemiallinen alkuaine esiintyy kolmessa muodossa: atomeina, yksinkertaisina aineina ja monimutkaisina aineina. Kemian rooli ihmisen elämässä on valtava. Kemistit uuttavat monia upeita aineita mineraali-, eläin- ja kasviraaka-aineista. Ihminen saa kemian avulla aineita, joilla on ennalta määrätyt ominaisuudet, ja niistä puolestaan tuotetaan vaatteita, kenkiä, laitteita, nykyaikaisia viestintävälineitä ja paljon muuta.
Kuten koskaan ennen, M.V. Lomonosov: "Kemia ojentaa kätensä inhimillisiin asioihin..."
Tällaisten kemianteollisuuden tuotteiden, kuten metallien, muovien, soodan jne., tuotanto saastuttaa ympäristöä erilaisilla haitallisilla aineilla.
Saavutukset kemiassa eivät ole pelkästään hyviä. Nykyajan ihmisen on tärkeää käyttää niitä oikein.
Makarova Katya.
Voinko elää ilman kemiallisia prosesseja?
Kemiallisia prosesseja on kaikkialla. He ympäröivät meitä. Joskus emme edes huomaa heidän läsnäoloaan jokapäiväisessä elämässämme. Pidämme niitä itsestäänselvyytenä ajattelematta tapahtuvien reaktioiden todellista luonnetta.
Joka hetki maailmassa tapahtuu lukemattomia prosesseja, joita kutsutaan kemiallisiksi reaktioiksi.
Kahden tai useamman aineen vuorovaikutuksessa toistensa kanssa muodostuu uusia aineita. On olemassa kemiallisia reaktioita, jotka ovat hyvin hitaita ja erittäin nopeita. Räjähdys on esimerkki nopeasta reaktiosta: hetkessä kiinteät tai nestemäiset aineet hajoavat vapauttaen suuren määrän kaasuja.
Teräslevy säilyttää kiiltonsa pitkään, mutta siihen ilmestyy vähitellen punertavia ruostekuvioita. Tätä prosessia kutsutaan korroosioksi. Korroosio on esimerkki hitaasta mutta erittäin salakavalasta kemiallisesta reaktiosta.
Hyvin usein, erityisesti teollisuudessa, on tarpeen nopeuttaa tiettyä reaktiota, jotta haluttu tuote saadaan nopeammin. Sitten käytetään katalyyttejä. Nämä aineet eivät itse osallistu reaktioon, mutta nopeuttavat sitä merkittävästi.
Mikä tahansa kasvi imee hiilidioksidia ilmasta ja vapauttaa happea. Samalla vihreässä lehdessä syntyy monia arvokkaita aineita. Tämä prosessi tapahtuu - fotosynteesi heidän laboratorioissaan.
Planeettojen ja koko maailmankaikkeuden evoluutio alkoi kemiallisista reaktioista.
Belialova Julia.
Sokeri
Sokeri on sakkaroosin yleinen nimi. Sokeria on monenlaista. Näitä ovat esimerkiksi glukoosi - rypälesokeri, fruktoosi - hedelmäsokeri, ruokosokeri, juurikassokeri (yleisin kidesokeri).
Aluksi sokeria saatiin vain ruo'osta. Sen uskotaan ilmestyneen alun perin Intiassa, Bengalissa. Ison-Britannian ja Ranskan välisten konfliktien vuoksi ruokosokerista tuli kuitenkin erittäin kallista, ja monet kemistit alkoivat miettiä, kuinka saada sitä jostain muusta. Ensimmäinen, joka teki tämän, oli saksalainen kemisti Andreas Marggraf 1700-luvun alussa. Hän huomasi, että joidenkin kasvien kuivatuissa mukuloissa on makea maku, ja mikroskoopilla katsottuna niissä näkyy valkoisia kiteitä, jotka ovat ulkonäöltään hyvin samanlaisia kuin sokeri. Marggraf ei kuitenkaan kyennyt toteuttamaan tietojaan ja havaintojaan, ja sokerin massatuotanto aloitettiin vasta vuonna 1801, kun Marggrafin oppilas Franz Karl Arhard osti Kunernin kartanon ja aloitti ensimmäisen sokerijuurikastehtaan rakentamisen. Voittojen lisäämiseksi hän tutki erilaisia juurikaslajikkeita ja selvitti syitä, miksi niiden mukulat saivat korkean sokeripitoisuuden. 1880-luvulla sokerintuotanto alkoi tuottaa suurta voittoa, mutta Archard ei nähnyt sitä.
Nyt juurikassokeri louhitaan seuraavasti. Punajuuret puhdistetaan ja murskataan, mehu uutetaan siitä puristimen avulla, sitten mehu puhdistetaan ei-sokerisista epäpuhtauksista ja haihdutetaan. Saadaan siirappia, keitetään, kunnes muodostuu sokerikiteitä. Ruokosokerin kanssa asiat ovat monimutkaisempia. Sokeriruoko murskataan myös, mehu uutetaan, se puhdistetaan epäpuhtauksista ja keitetään, kunnes siirappiin ilmestyy kiteitä. Tässä tapauksessa saadaan kuitenkin vain raakasokeria, josta sitten valmistetaan sokeria. Tämä raakasokeri puhdistetaan poistamalla ylimääräinen ja väriaine, ja siirappia keitetään uudelleen, kunnes se kiteytyy. Sokerille ei sinänsä ole kaavaa: kemiassa sokeri on makea, liukoinen hiilihydraatti.
Umanski Kirill.
Suola
Suola - elintarviketuote. Jauhettuna se on pieniä valkoisia kiteitä. Luonnollisen alkuperän ruokasuolassa on lähes aina muiden mineraalisuolojen epäpuhtauksia, jotka voivat antaa sille eri värisävyjä (yleensä harmaata). Sitä valmistetaan eri muodoissa: puhdistettu ja puhdistamaton (kivisuola), karkea ja hienojauhettu, puhdas ja jodittu, merisuola jne.
Muinaisina aikoina suolaa saatiin polttamalla tiettyjä kasveja tulessa; saatua tuhkaa käytettiin mausteena. Suolasaannon lisäämiseksi ne kasteltiin lisäksi suolaisella merivedellä. Ainakin kaksituhatta vuotta sitten ruokasuolan uuttaminen alettiin suorittaa haihduttamalla merivettä. Tämä menetelmä ilmestyi ensimmäisen kerran maissa, joissa ilmasto on kuiva ja kuuma, jossa veden haihtuminen tapahtui luonnollisesti; kun se levisi, vettä alettiin lämmittää keinotekoisesti. Pohjoisilla alueilla, erityisesti Valkoisenmeren rannoilla, menetelmää on parannettu: kuten tiedätte, makea vesi jäätyy aikaisemmin kuin suolainen vesi, ja jäljellä olevan liuoksen suolapitoisuus kasvaa vastaavasti. Siten merivedestä saatiin samanaikaisesti tuoretta ja tiivistettyä suolavettä, joka sitten haihdutettiin pienemmillä energiakustannuksilla.
Ruokasuola on tärkeä raaka-aine kemianteollisuudelle. Sitä käytetään soodan, kloorin, suolahapon, natriumhydroksidin ja natriummetallin valmistukseen.
Suolaliuos vedessä jäätyy alle 0 °C:n lämpötiloissa. Sekoittuessaan puhtaan vesijään kanssa (myös lumen muodossa), suola saa sen sulamaan, koska lämpöenergia valitaan ympäristöstä. Tätä ilmiötä käytetään teiden puhdistamiseen lumesta.
Chumakova Julia
Venäjän tieteen menneisyyden loistavien nimien joukossa on yksi meille erityisen läheinen ja rakas - Mihail Vasilyevich Lomonosovin nimi. Hänestä tuli Venäjän tieteen elävä ruumiillistuma. Hän valitsi työnsä pääsuunnaksi kemian. Lomonosov oli aikansa merkittävin tiedemies. Hänen työnsä vaati näkyviä tuloksia. Tämä selittää sinnikkyyden, jolla hän saavutti menestystä.
Esityksen aihe:"Kemia ojentaa kätensä miesten asioihin." Tämä on esitys M.V.:n toiminnasta. Lomonosov kemian alalla.
Tämä aihe on tärkeä, koska M.V. Lomonosov on yksi suurista tiedemiehistä, joka voidaan epäilemättä asettaa ykkössijalle ihmiskunnan monipuolisten lahjakkaiden joukossa. Hänen saavutuksensa tieteen alalla ovat hämmästyttäviä. Kaikella, mitä Lomonosov puhui, oli syvän ammattimaisuuden luonne. Siksi hänen työnsä on tällä hetkellä suurta mielenkiintoa ja kunnioitusta.
Työ tehtiin kemian (raportti) ja tietojenkäsittelytieteen (esitys) opettajan ohjauksessa
Ladata:
Esikatselu:
Raportti "Kemia ojentaa kätensä ihmisasioissa" VI opiskelijatieteellisessä ja käytännön konferenssissa "Ja heijastuksesi palaa vielä nytkin..."
Kaikista tieteistä, joita tietosanakirjailija Lomonosov harjoitti, ensimmäinen paikka kuuluu objektiivisesti kemialle: 25. heinäkuuta 1745 Lomonosoville myönnettiin erityisellä asetuksella kemian professorin arvo (mitä nykyään kutsutaan akateemioksi - sitten siellä). ei yksinkertaisesti ollut sellaista otsikkoa).
Lomonosov korosti, että kemiassa "se, mitä sanottiin, on todistettava", joten hän halusi antaa asetuksen Venäjän ensimmäisen kemian laboratorion rakentamisesta, joka valmistui vuonna 1748. Venäjän tiedeakatemian ensimmäinen kemian laboratorio on toiminnassaan laadullisesti uusi taso: siinä otettiin ensimmäistä kertaa käyttöön tieteen ja käytännön integraation periaate. Laboratorion avajaisissa puhuessaan Lomonosov sanoi: "Kemian tutkimuksella on kaksi tarkoitusta: yksi on luonnontieteiden parantaminen. Toinen on elämän siunausten lisääntyminen.
Laboratoriossa suoritettujen lukuisten tutkimusten joukossa erityinen paikka oli Lomonosovin kemiallisella ja teknisellä lasi- ja posliinityöllä. Hän suoritti yli kolme tuhatta koetta, jotka tarjosivat runsaasti kokeellista materiaalia "todellisen väriteorian" perustelemiseksi. Lomonosov itse sanoi useammin kuin kerran, että kemia on hänen "pääammattinsa".
Lomonosov luennoi opiskelijoille laboratoriossa, opetti heille kokeellisia taitoja. Itse asiassa se oli ensimmäinen opiskelijapaja. Laboratoriokokeita edelsi teoreettiset seminaarit.
Jo yhdessä ensimmäisistä teoksistaan - "Matemaattisen kemian elementit" (1741) Lomonosov totesi: "Tosi kemistin on oltava teoreetikko ja harjoittaja sekä filosofi." Tuolloin kemiaa tulkittiin taiteena kuvata eri aineiden ominaisuuksia ja niiden eristämistä ja puhdistamista. Ei kumpikaan
tutkimusmenetelmät, kemiallisten toimintojen kuvausmenetelmät tai silloisten kemistien ajattelutyyli eivät tyydyttäneet Lomonosovia, joten hän siirtyi pois vanhasta ja hahmotteli suurenmoisen ohjelman kemian taiteen muuttamiseksi tieteeksi.
Vuonna 1751 Tiedeakatemian julkisessa kokouksessa Lomonosov piti kuuluisan "Sarmon kemian eduista", jossa hän esitti näkemyksensä, jotka poikkesivat vallitsevista. Se, mitä Lomonosov aikoi saavuttaa, oli suurenmoista innovatiivisessa suunnittelussaan: hän halusi tehdä kaikesta kemiasta fysikaalista ja kemiallista tiedettä ja nosti ensimmäistä kertaa esiin uuden kemiallisen tietämyksen alueen - fysikaalisen kemian. Hän kirjoitti: "En vain nähnyt eri kirjoittajissa, vaan olen myös vakuuttunut omasta taiteestani, että kemialliset kokeet yhdistettynä fyysisiin kokeisiin osoittavat erityisiä toimintoja." Ensimmäistä kertaa hän alkoi antaa opiskelijoille kurssia "todellisesta fysikaalisesta kemiasta" seuraten häntä esittelykokeissa.
Vuonna 1756 Lomonosov suoritti kemiallisessa laboratoriossa sarjan kokeita metallien kalsinointia (kalsinointia) varten, josta hän kirjoitti: "... tiiviisti sulatetuissa lasiastioissa tehtiin kokeita sen selvittämiseksi, tuleeko paino puhtaasta lämmöstä; Näillä kokeilla todettiin, että loistavan Robert Boylen mielipide on väärä, koska ilman ulkoilman kulkua palaneen metallin paino pysyy yhdellä mitalla ... ". Tämän seurauksena Lomonosov, käyttämällä erityistä esimerkkiä yleisen säilymislain soveltamisesta, todisti aineen kokonaismassan muuttumattomuuden kemiallisten muutosten aikana ja löysi kemian tieteen peruslain - aineen massan pysyvyyden lain. Joten Lomonosov oli ensimmäinen Venäjällä ja myöhemmin Lavoisier Ranskassa, joka lopulta muutti kemian tiukasti kvantitatiiviseksi tieteeksi.
Lukuisat kokeet ja materialistinen näkemys luonnonilmiöistä johtivat Lomonosovin ajatukseen "universaalista luonnonlakista". Kirjeessään Eulerille vuonna 1748 hän kirjoitti: "Kaikki luonnossa tapahtuvat muutokset tapahtuvat siten, että jos jotain lisätään johonkin, se otetaan pois jostakin muusta.
Siten niin paljon ainetta lisätään yhteen kappaleeseen, sama määrä häviää toisesta. Koska tämä on universaali luonnonlaki, se ulottuu myös liikkeen sääntöihin: keho, joka kiihottaa toisen liikkeelle vauhtillaan, menettää liikkeestään yhtä paljon kuin se kommunikoi liikuttamansa kanssa. Kymmenen vuotta myöhemmin hän esitteli tämän lain Tiedeakatemian kokouksessa ja julkaisi sen vuonna 1760 painettuna. Edellä mainitussa kirjeessä Eulerille Lomonosov ilmoitti hänelle, että jotkut Akatemian jäsenet kyseenalaistavat tämän ilmeisen luonnonlain. Kun akateemisen toimiston johtaja Schumacher lähetti ilman sopimusta Lomonosovin kanssa useita julkaistavaksi jätettyjä Lomonosovin papereita Eulerille tarkastettavaksi, suuren matemaatikon vastaus oli innostunut: "Kaikki nämä teokset eivät ole vain hyviä, vaan myös erinomaisia." Euler kirjoitti: "Koska hän (Lomonosov) selittää fyysisiä asioita, kaikkein tarpeellisimpia ja vaikeimpia, jotka olivat täysin tuntemattomia ja nerokkaimmille tiedemiehille mahdottomia tulkita, niin perusteellisesti, että olen täysin varma hänen todisteidensa oikeellisuudesta. Tässä tapauksessa minun on tehtävä oikeutta herra Lomonosoville, että hän on lahjakkain älykkyys fysikaalisten ja kemiallisten ilmiöiden selittämiseen. On tarpeen toivoa, että kaikki muut Akatemiat pystyisivät näyttämään sellaisia keksintöjä kuin herra Lomonosov osoitti.
Sivu 7/8
Kemia leviää laajasti...

Lisää timantista
Raaka, raakatimantti on "kaikkien mineraalien, materiaalien ja muiden" mestari kovuuden suhteen. Moderni tekniikka ilman timantteja olisi vaikeaa.
Valmis, kiillotettu timantti muuttuu timantiksi, eikä sillä ole vertaa jalokivien joukossa.
Jalokivikauppiaat arvostavat erityisesti sinisiä timantteja. Ne ovat luonteeltaan järjettömän harvinaisia, ja siksi he maksavat niistä aivan hullua rahaa.
Mutta Jumala siunatkoon heitä timanttikoruilla. Olkoon tavallisia timantteja enemmän, jotta sinun ei tarvitse vapista jokaisen pienen kristallin yli.
Valitettavasti maapallolla on vain muutamia timanttiesiintymiä ja vielä vähemmän rikkaita. Yksi niistä on Etelä-Afrikassa. Ja se tuottaa edelleen jopa 90 prosenttia maailman timantituotannosta. Paitsi Neuvostoliitto. Kymmenen vuotta sitten löysimme Jakutian suurimman timanttialueen. Nyt siellä on meneillään teollinen timanttien louhinta.
Luonnontimanttien muodostuminen vaati poikkeuksellisia olosuhteita. Valtavat lämpötilat ja paineet. Timantit syntyivät maan paksuuden syvyyksissä. Paikoin timanttipitoisia sulatteita purskahti pintaan ja kiinteytyi. Mutta tämä tapahtui erittäin harvoin.
Onko mahdollista tulla toimeen ilman luonnon palveluita? Voiko ihminen luoda timantteja itse?
Tieteen historiassa on kirjattu yli tusina yritystä saada keinotekoisia timantteja. (Muuten, yksi ensimmäisistä "onnen etsijistä" oli Henri Moissan, joka eristi vapaata fluoria.) Jokainen yksittäinen epäonnistui. Joko menetelmä oli pohjimmiltaan väärä tai kokeilijoilla ei ollut laitteita, jotka kestäisivät korkeimpien lämpötilojen ja paineiden yhdistelmän.
Vasta 1950-luvun puolivälissä viimeisin teknologia löysi vihdoin avaimet keinotekoisten timanttien ongelman ratkaisemiseen. Raaka-aineena oli odotetusti grafiittia. Häneen kohdistui samanaikaisesti 100 000 ilmakehän paine ja noin 3 000 asteen lämpötila. Nyt timantteja valmistetaan monissa maailman maissa.
Mutta kemistit täällä voivat vain iloita yhdessä kaikkien kanssa. Heidän roolinsa ei ole niin suuri: fysiikka otti pääosan.
Mutta kemistit ovat onnistuneet toisessa. Ne auttoivat merkittävästi parantamaan timanttia.
Miten parantaa näin? Onko mitään täydellisempää kuin timantti? Sen kristallirakenne on kristallimaailman täydellisyyttä. Timanttikiteissä olevien hiiliatomien ihanteellisen geometrisen järjestelyn ansiosta jälkimmäiset ovat niin kovia.
Et voi tehdä timantista kovempaa kuin se on. Mutta aineesta on mahdollista tehdä timanttia kovempaa. Ja kemistit ovat luoneet raaka-aineita tätä varten.
On boorin kemiallinen yhdiste typen kanssa - boorinitridi. Ulkoisesti se on merkityksetön, mutta yksi sen ominaisuuksista on hälyttävä: sen kiderakenne on sama kuin grafiitilla. "Valkoinen grafiitti" - tämä nimi on pitkään liitetty boorinitridille. Totta, kukaan ei yrittänyt tehdä siitä lyijykynän johtoja ...
Kemistit ovat löytäneet halvan tavan syntetisoida boorinitridi. Fyysikot tekivät hänelle julmia kokeita: satoja tuhansia ilmakehyksiä, tuhansia asteita... Heidän toimiensa logiikka oli äärimmäisen yksinkertainen. Koska "musta" grafiitti on muutettu timantiksi, voidaanko "valkoisesta" grafiitista saada timantin kaltaista ainetta?
Ja he saivat niin sanotun boratsonin, joka ylittää timantin kovuudessaan. Se jättää naarmuja sileisiin timanttireunoihin. Ja se kestää korkeampia lämpötiloja - et voi vain polttaa boratsonia.
Borazon on edelleen kallis. On paljon työtä tehtävänä, jotta se tulee halvemmaksi. Mutta tärkein asia on jo tehty. Ihminen osoittautui jälleen kykeneväksi luontoon.
…Ja tässä on toinen viesti, joka tuli hiljattain Tokiosta. Japanilaiset tutkijat ovat onnistuneet valmistamaan aineen, joka on paljon vahvempi kuin timantti kovuudeltaan. He altistivat magnesiumsilikaatin (magnesiumista, piistä ja hapesta koostuva yhdiste) 150 tonnin paineeseen neliösenttimetriä kohti. Ilmeisistä syistä synteesin yksityiskohtia ei mainosteta. Vastasyntyneellä "kovuuden kuninkaalla" ei ole vielä nimeä. Mutta sillä ei ole väliä. Toinen asia on tärkeämpi: ei ole epäilystäkään siitä, että lähitulevaisuudessa timantti, joka oli vuosisatojen ajan kovimpien aineiden luettelon kärjessä, ei ole tämän luettelon ensimmäisellä sijalla.
Loputtomat molekyylit
Kumi on kaikkien tiedossa. Nämä ovat palloja ja galosseja. Se on jääkiekkokiekko ja kirurgin hanskat. Lopuksi nämä ovat autonrenkaat ja lämmitystyynyt, vedenpitävät sadetakit ja vesiletkut.
Nyt kumia ja siitä valmistettuja tuotteita valmistetaan sadoissa tehtaissa ja tehtaissa. Ja muutama vuosikymmen sitten luonnonkumia käytettiin kaikkialla maailmassa kumin valmistukseen. Sana "kumi" tulee intiaanien sanasta "kao-chao", joka tarkoittaa "hevean kyyneleitä". Ja hevea on puu. Keräämällä ja käsittelemällä sen maitomaista mehua tietyllä tavalla ihmiset saivat kumia.
Kumista voidaan valmistaa monia hyödyllisiä asioita, mutta on sääli, että sen louhinta on erittäin työlästä ja hevea kasvaa vain tropiikissa. Ja teollisuuden tarpeita oli mahdotonta täyttää luonnollisilla raaka-aineilla.
Tässä kemia tulee apuun. Ensinnäkin kemistit esittivät itselleen kysymyksen: miksi kumi on niin joustavaa? Heidän piti pitkään tutkia "Hevean kyyneleitä", ja lopulta he löysivät vihjeen. Kävi ilmi, että kumimolekyylit rakennetaan hyvin omituisella tavalla. Ne koostuvat suuresta määrästä toistuvia identtisiä lenkkejä ja muodostavat jättimäisiä ketjuja. Tietenkin tällainen "pitkä" molekyyli, joka sisältää noin viisitoista tuhatta linkkiä, pystyy taipumaan kaikkiin suuntiin, ja sillä on myös elastisuutta. Tämän ketjun linkki osoittautui hiileksi, isopreeni C5H8, ja sen rakennekaava voidaan esittää seuraavasti:

Olisi oikein sanoa, että isopreeni edustaa alkuperäistä luonnollista monomeeriä. Polymerointiprosessissa isopreenimolekyyli muuttuu jonkin verran: hiiliatomien väliset kaksoissidokset katkeavat. Tällaisten vapautuneiden sidosten ansiosta yksittäiset linkit yhdistyvät jättimäiseksi kumimolekyyliksi.
Keinotekoisen kumin saannin ongelma on huolestuttanut tutkijoita ja insinöörejä pitkään.
Vaikuttaa siltä, että asia ei ole niin kuuma, mikä hankala. Hanki ensin isopreeni. Laita se sitten polymeroitumaan. Sido yksittäiset isopreeniyksiköt pitkiksi ja taipuisiksi tekokumiketjuiksi.

Se näytti yhdeltä, se osoittautui toiseksi. Kemistit syntetisoivat isopreeniä ilman vaikeuksia, mutta heti kun se tuli polymerointiin, kumi ei toiminut. Linkit yhdistettiin toisiinsa, mutta sattumanvaraisesti, eivätkä missään tietyssä järjestyksessä. Ja keinotekoisia tuotteita luotiin, hieman samanlaisia kuin kumi, mutta monin tavoin erilaisia kuin se.
Ja kemistien oli keksittävä tapoja saada isopreeniyksiköt kiertymään ketjuksi oikeaan suuntaan.
Maailman ensimmäinen teollinen tekokumi hankittiin Neuvostoliitossa. Akateemikko Sergei Vasilyevich Lebedev valitsi tähän toisen aineen - butadieeni:

Koostumukseltaan ja rakenteeltaan hyvin samanlainen kuin isopreenin, mutta butadieenin polymeroitumista on helpompi hallita.
Nykyään tunnetaan melko suuri määrä keinokumeja (toisin kuin luonnonkumeja, niitä kutsutaan nykyään usein elastomeereiksi).
Itse luonnonkumilla ja siitä valmistetuilla tuotteilla on merkittäviä haittoja. Siten se turpoaa voimakkaasti öljyissä ja rasvoissa, eikä kestä monien hapettimien, erityisesti otsonin, vaikutusta, jonka jäämiä on aina ilmassa. Luonnonkumista valmistettujen tuotteiden valmistuksessa se on vulkanoitava, eli altistettava korkealle lämpötilalle rikin läsnä ollessa. Näin kumi muuttuu kumiksi tai eboniittiksi. Luonnonkumituotteiden (esim. autonrenkaat) käytön aikana vapautuu huomattava määrä lämpöä, mikä johtaa niiden ikääntymiseen ja nopeaan kulumiseen.
Siksi tutkijoiden oli huolehdittava uusien synteettisten kumien luomisesta, joilla olisi kehittyneempiä ominaisuuksia. On olemassa esimerkiksi kumiperhe nimeltä "buna". Se tulee kahden sanan alkukirjaimista: "butadieeni" ja "natrium". (Natriumilla on polymerointikatalyytin rooli.) Eräät tämän perheen elastomeerit ovat osoittautuneet erinomaisiksi. Ne menivät pääasiassa autonrenkaiden valmistukseen.

Erityisen tärkeä on ns. butyylikumi, jota saadaan isobuteenin ja isopreenin yhteispolymeroimalla. Ensinnäkin se osoittautui halvimmaksi. Ja toiseksi, toisin kuin luonnonkumi, otsoni ei juuri vaikuta siihen. Lisäksi butyylikumivulkanisaatit, joita nykyään käytetään laajalti kammioiden valmistuksessa, ovat kymmenen kertaa ilmatiiviisempiä kuin luonnontuotevulkanisaatit.
Niin sanotut polyuretaanikumit ovat hyvin omituisia. Niillä on korkea veto- ja vetolujuus, joten ne eivät melkein ole alttiina ikääntymiselle. Valmistele polyuretaanielastomereista ns. vaahtokumi, joka soveltuu istuinten verhoiluun.
Viimeisen vuosikymmenen aikana on kehitetty kumia, joita tiedemiehet eivät olleet aiemmin ajatelleet. Ja ennen kaikkea organopii- ja fluorihiiliyhdisteisiin perustuvat elastomeerit. Näille elastomeereille on ominaista korkean lämpötilan kestävyys, kaksi kertaa luonnonkumiin verrattuna. Ne kestävät otsonia, ja fluorihiiliyhdisteisiin perustuva kumi ei pelkää edes savuavaa rikki- ja typpihappoa.
Mutta siinä ei vielä kaikki. Viime aikoina on saatu ns. karboksyylipitoisia kumeja, butadieenin ja orgaanisten happojen kopolymeerejä. He osoittautuivat jännityksessä poikkeuksellisen vahvoiksi.
Voidaan sanoa, että myös luonto on menettänyt ensisijaisuutensa ihmisen luomiin materiaaleihin nähden.
Timanttisydän ja sarvikuonon iho
Orgaanisessa kemiassa on luokka yhdisteitä, joita kutsutaan hiilivedyiksi. Nämä ovat todella hiilivetyjä - niiden molekyyleissä, paitsi hiili- ja vetyatomeissa, ei ole mitään muuta. Tyypillinen niiden tunnetuimmista edustajista on metaani (se muodostaa noin 95 prosenttia maakaasusta) ja nestemäisistä hiilivedyistä - öljy, josta saadaan erilaisia bensiinilaatuja, voiteluöljyjä ja monia muita arvokkaita tuotteita.
Otetaan yksinkertaisin hiilivety, metaani CH 4 . Mitä tapahtuu, jos metaanin vetyatomit korvataan happiatomeilla? Hiilidioksidi CO 2 . Ja jos rikkiatomeissa? Erittäin haihtuva myrkyllinen neste, hiilisulfidi CS 2 . Entä jos korvaamme kaikki vetyatomit klooriatomeilla? Saamme myös hyvin tunnetun aineen: hiilitetrakloridin. Ja jos otat fluoria kloorin sijaan?
Kolme vuosikymmentä sitten harvat pystyivät vastaamaan tähän kysymykseen mitään ymmärrettävää. Kuitenkin meidän aikanamme fluorihiiliyhdisteet ovat jo itsenäinen kemian ala.
Fysikaalisten ominaisuuksiensa mukaan fluorihiilivedyt ovat lähes täydellisiä hiilivetyjen analogeja. Mutta tähän heidän yhteiset ominaisuudet päättyvät. Fluorihiilivedyt, toisin kuin hiilivedyt, osoittautuivat erittäin reaktiivisiksi aineiksi. Lisäksi ne ovat erittäin lämmönkestäviä. Ei ihme, että niitä kutsutaan joskus aineiksi, joilla on "timanttisydän ja sarvikuonon iho".

Niiden stabiilisuuden kemiallinen olemus verrattuna hiilivetyihin (ja muihin orgaanisten yhdisteiden luokkiin) on suhteellisen yksinkertainen. Fluoriatomit ovat paljon suurempia kuin vedyn atomit, ja siksi ne "sulkevat" tiukasti muiden reaktiivisten atomien pääsyn niitä ympäröiviin hiiliatomeihin.
Toisaalta ioneiksi muuttuneiden fluoriatomien on äärimmäisen vaikea luopua elektronistaan ja "eivät halua" reagoida muiden atomien kanssa. Loppujen lopuksi fluori on aktiivisin ei-metalleista, eikä käytännössä mikään muu ei-metalli voi hapettaa ioniaan (ottaa elektronin pois ionistaan). Kyllä, ja hiili-hiili-sidos on sinänsä vakaa (muista timantti).
Fluorihiilivedyt ovat löytäneet laajimman sovelluksen juuri niiden inerttisyyden vuoksi. Esimerkiksi fluorihiilivetymuovi, niin kutsuttu teflon, on vakaa 300 asteeseen kuumennettaessa, rikki-, typpi-, kloorivety- ja muut hapot eivät vaikuta siihen. Kiehuvat alkalit eivät vaikuta siihen, se ei liukene kaikkiin tunnettuihin orgaanisiin ja epäorgaanisiin liuottimiin.
Ei turhaan, että fluoroplastia kutsutaan joskus "orgaaniseksi platinaksi", koska se on hämmästyttävä materiaali lasitavaroiden valmistukseen kemian laboratorioihin, erilaisiin teollisuuskemiallisiin laitteisiin ja putkiin eri tarkoituksiin. Uskokaa minua, monet asiat maailmassa olisi tehty platinasta, jos se ei olisi niin kallista. Fluoroplasti on suhteellisen halpaa.
Kaikista maailmassa tunnetuista aineista fluoroplasti on liukkain. Pöydälle heitetty fluoroplastikalvo kirjaimellisesti "virtaa" lattialle. PTFE-laakerit eivät käytännössä tarvitse voitelua. Lopuksi fluoroplasti on ihana eriste ja lisäksi erittäin lämmönkestävä. Fluoroplastinen eristys kestää kuumennuksen jopa 400 asteeseen (lyijyn sulamispisteen yläpuolella!).
Sellainen on fluoroplasti - yksi upeimmista ihmisen luomista keinotekoisista materiaaleista.
Nestemäiset fluorihiilivedyt ovat syttymättömiä eivätkä jäädy kovin alhaisiin lämpötiloihin.
Hiilen ja piin liitto
Kaksi luonnon elementtiä voivat vaatia erityisasemaa. Ensinnäkin hiili. Hän on kaiken elävän perusta. Ja ennen kaikkea siksi, että hiiliatomit pystyvät liittymään tiukasti toisiinsa muodostaen ketjumaisia yhdisteitä:

Toiseksi pii. Hän on kaiken epäorgaanisen luonnon perusta. Mutta piiatomit eivät voi muodostaa niin pitkiä ketjuja kuin hiiliatomit, ja siksi luonnossa on vähemmän piiyhdisteitä kuin hiiliyhdisteitä, vaikkakin paljon enemmän kuin muiden kemiallisten alkuaineiden yhdisteitä.
Tiedemiehet päättivät "korjata" tämän piin puutteen. Itse asiassa pii on yhtä neliarvoinen kuin hiili. Totta, hiiliatomien välinen sidos on paljon vahvempi kuin piiatomien välinen sidos. Mutta pii ei ole niin aktiivinen elementti.
Ja jos hänen osallistumisellaan olisi mahdollista saada orgaanisten yhdisteiden kaltaisia yhdisteitä, mitä hämmästyttäviä ominaisuuksia niillä voisi olla!
Aluksi tiedemiehet eivät olleet onnekkaita. On totta, että pii voi muodostaa yhdisteitä, joissa sen atomit vuorottelevat happiatomien kanssa:

Ne osoittautuivat kuitenkin epävakaiksi.
Menestys tuli, kun piiatomit päättivät yhdistyä hiiliatomien kanssa. Tällaisilla yhdisteillä, joita kutsutaan organopiiksi tai silikoneiksi, on useita ainutlaatuisia ominaisuuksia. Niiden perusteella luotiin erilaisia hartseja, joiden avulla on mahdollista saada muovimassoja, jotka kestävät korkeita lämpötiloja pitkään.
Organopiipolymeerien pohjalta valmistetuilla kumeilla on arvokkaimmat ominaisuudet, kuten lämmönkestävyys. Jotkut silikonikumin laadut kestävät jopa 350 astetta. Kuvittele sellaisesta kumista valmistettu autonrengas.
Silikonikumit eivät turpoa lainkaan orgaanisissa liuottimissa. Niistä alkoi tuottaa erilaisia putkia polttoaineen pumppaamiseen.
Jotkut silikoninesteet ja -hartsit eivät juurikaan muuta viskositeettiaan laajalla lämpötila-alueella. Tämä tasoitti tietä niiden käytölle voiteluaineina. Alhaisen haihtuvuuden ja korkean kiehumispisteensä vuoksi silikoninesteitä käytetään laajalti suurtyhjiöpumpuissa.
Silikoniyhdisteillä on vettä hylkiviä ominaisuuksia, ja tämä arvokas laatu on otettu huomioon. Niitä alettiin käyttää vettä hylkivän kankaan valmistukseen. Mutta kyse ei ole vain kankaista. On tunnettu sananlasku "vesi kuluttaa kiven". Tärkeiden rakenteiden rakentamisessa testattiin rakennusmateriaalien suojausta erilaisilla organopiinesteillä. Kokeilut onnistuivat.
Silikoneista on äskettäin luotu vahvoja lämpöä kestäviä emaleja. Tällaisilla emaleilla päällystetyt kupari- tai rautalevyt kestävät kuumennuksen jopa 800 asteeseen useita tunteja.
Ja tämä on vasta alkua eräänlaiselle hiilen ja piin liitolle. Mutta tällainen "kaksoisliitto" ei enää tyydytä kemistejä. He asettivat tehtäväksi lisätä muita alkuaineita organopiiyhdisteiden molekyyleihin, kuten esimerkiksi alumiinia, titaania ja booria. Tiedemiehet ovat onnistuneesti ratkaisseet ongelman. Näin syntyi täysin uusi aineluokka - polyorganometallosiloksaanit. Tällaisten polymeerien ketjuissa voi olla erilaisia linkkejä: pii - happi - alumiini, pii - happi - titaani, pii - happi - boori ja muut. Tällaiset aineet sulavat 500-600 asteen lämpötiloissa ja kilpailevat tässä mielessä monien metallien ja metalliseosten kanssa.
Kirjallisuudessa jotenkin välähti viesti, että japanilaisten tiedemiesten väitetään onnistuneen luomaan polymeerimateriaalin, joka kestää jopa 2000 asteen kuumennuksen. Ehkä tämä on virhe, mutta virhe, joka ei ole liian kaukana totuudesta. Termi "lämmönkestävät polymeerit" pitäisi pian sisällyttää pitkälle listalle uusia modernin tekniikan materiaaleja.
Upeat seulat
Nämä seulat on järjestetty melko alkuperäisellä tavalla. Ne ovat jättimäisiä orgaanisia molekyylejä, joilla on useita mielenkiintoisia ominaisuuksia.
Ensinnäkin, kuten monet muovit, ne ovat liukenemattomia veteen ja orgaanisiin liuottimiin. Ja toiseksi, ne sisältävät niin sanotut ionogeeniset ryhmät, toisin sanoen ryhmät, jotka liuottimessa (erityisesti vedessä) voivat antaa yhden tai toisen ionin. Näin ollen nämä yhdisteet kuuluvat elektrolyyttien luokkaan.
Niissä oleva vetyioni voidaan korvata jollain metallilla. Näin ionit vaihtuvat.
Näitä erikoisia yhdisteitä kutsutaan ioninvaihtimiksi. Niitä, jotka pystyvät olemaan vuorovaikutuksessa kationien (positiivisesti varautuneiden ionien) kanssa, kutsutaan kationinvaihtimiksi, ja niitä, jotka ovat vuorovaikutuksessa negatiivisesti varautuneiden ionien kanssa, kutsutaan anioninvaihtimiksi. Ensimmäiset orgaaniset ioninvaihtimet syntetisoitiin 1930-luvun puolivälissä. Ja voitti heti laajimman tunnustuksen. Kyllä, tämä ei ole yllättävää. Itse asiassa ioninvaihtimien avulla on mahdollista muuttaa kova vesi pehmeäksi, suolaiseksi - tuoreeksi.

Kuvittele kaksi kolonnia - yksi niistä on täytetty kationinvaihtohartsilla, toinen anioninvaihtohartsilla. Oletetaan, että ryhdymme puhdistamaan tavallista ruokasuolaa sisältävää vettä. Kuljetamme vettä ensin kationinvaihtimen läpi. Siinä kaikki natriumionit "vaihdetaan" vetyioneiksi, ja natriumkloridin sijaan vedessämme on jo suolahappoa. Sitten vedämme veden anionihartsin läpi. Jos se on hydroksyylimuodossaan (eli sen vaihdettavat anionit ovat hydroksyyli-ioneja), kaikki kloridi-ionit korvataan liuoksessa hydroksyyli-ioneilla. No, hydroksyyli-ionit vapaiden vetyionien kanssa muodostavat välittömästi vesimolekyylejä. Siten vesi, joka alun perin sisälsi natriumkloridia, muuttui ioninvaihtokolonnien läpi kulkemisen jälkeen täysin suolattomaksi. Ominaisuuksiltaan se voi kilpailla parhaan tislatun veden kanssa.
Mutta ei vain veden suolanpoisto toi laajaa suosiota ioninvaihtimille. Kävi ilmi, että ioninvaihtajat pitävät ioneja eri tavoin, eri vahvuuksin. Litium-ionit ovat vahvempia kuin vetyionit, kalium-ionit ovat vahvempia kuin natrium, rubidium-ionit ovat vahvempia kuin kalium ja niin edelleen. Ioninvaihtimien avulla tuli mahdolliseksi suorittaa erilaisten metallien erottaminen erittäin helposti. Ioninvaihtimilla on nyt tärkeä rooli useilla teollisuudenaloilla. Esimerkiksi valokuvatehtaissa ei pitkään aikaan ollut sopivaa tapaa vangita arvokasta hopeaa. Ioninvaihtimet ratkaisivat tämän tärkeän ongelman.
Voiko ihminen koskaan käyttää ioninvaihtimia arvokkaiden metallien erottamiseen merivedestä? Tähän kysymykseen on vastattava myöntävästi. Ja vaikka merivesi sisältää valtavan määrän erilaisia suoloja, näyttää siltä, että jalometallien saaminen siitä on lähitulevaisuudessa.
Nyt vaikeus on se, että kun merivettä johdetaan kationinvaihtimen läpi, sen sisältämät suolat eivät itse asiassa salli pienten arvometallien epäpuhtauksien laskeutumista kationinvaihtimeen. Viime aikoina on kuitenkin syntetisoitu niin kutsuttuja elektroninvaihtohartseja. Ne eivät ainoastaan vaihta ionejaan metalli-ioneiksi liuoksesta, vaan ne pystyvät myös pelkistämään tämän metallin luovuttamalla sille elektroneja. Viimeaikaiset kokeet tällaisilla hartseilla ovat osoittaneet, että jos hopeaa sisältävä liuos johdetaan niiden läpi, hartsille ei nopeasti kerrostu hopeaioneja, vaan metallihopeaa, ja hartsi säilyttää ominaisuutensa pitkään. Siten, jos suolojen seos johdetaan elektroninvaihtimen läpi, helpoimmin pelkistyvät ionit voivat muuttua puhtaiksi metalliatomeiksi.
Kemialliset pihdit
Kuten vanha vitsi kuuluu, leijonien pyydystäminen autiomaassa on helppoa. Koska autiomaa on tehty hiekasta ja leijonasta, on otettava seula ja seulottava autiomaa. Hiekka kulkee reikien läpi ja leijonat jäävät arinalle.
Mutta entä jos jokin arvokas kemiallinen alkuaine sekoitetaan valtavaan määrään sellaisia, jotka eivät edusta mitään arvoa sinulle? Tai on tarpeen puhdistaa aine haitallisesta epäpuhtaudesta, joka sisältää hyvin pieniä määriä.
Tätä tapahtuu melko usein. Ydinreaktorien suunnittelussa käytettävässä zirkoniumissa hafniumin lisäys ei saisi ylittää muutamaa kymmentä tuhannesosaa ja tavallisessa zirkoniumissa noin kaksi kymmenesosaa.

Nämä elementit ovat kemiallisilta ominaisuuksiltaan hyvin samankaltaisia, ja tavalliset menetelmät täällä, kuten sanotaan, eivät toimi. Jopa hämmästyttävä kemiallinen seula. Samaan aikaan tarvitaan poikkeuksellisen korkean puhtausasteen zirkoniumia ...
Kemistit seurasivat vuosisatojen ajan yksinkertaista reseptiä: "Like liuottaa kaltaista". Epäorgaaniset aineet liukenevat hyvin epäorgaanisiin liuottimiin, orgaaniset - orgaanisiin. Monet mineraalihappojen suolat liukenevat hyvin veteen, vedettömään fluorivetyhappoon, nestemäiseen syaanivetyhappoon (syaanivetyhappo). Hyvin monet orgaaniset aineet ovat melko liukoisia orgaanisiin liuottimiin - bentseeni, asetoni, kloroformi, hiilisulfidi jne., jne.
Ja miten aine käyttäytyy, joka on jotain orgaanisten ja epäorgaanisten yhdisteiden välissä? Itse asiassa kemistit tunsivat jossain määrin tällaiset yhdisteet. Joten klorofylli (vihreän lehden väriaine) on orgaaninen yhdiste, joka sisältää magnesiumatomeja. Se liukenee hyvin moniin orgaanisiin liuottimiin. Luonnolle tuntemattomia keinotekoisesti syntetisoituja organometallisia yhdisteitä on valtava määrä. Monet niistä pystyvät liukenemaan orgaanisiin liuottimiin, ja tämä kyky riippuu metallin luonteesta.
Tässä kemistit päättivät pelata.
Ydinreaktorien toiminnan aikana tulee aika ajoin tarpeen vaihtaa käytettyjä uraanilohkoja, vaikka niissä olevien epäpuhtauksien (uraanin fissiopalasten) määrä ei yleensä ylitä prosentin tuhannesosaa. Ensin lohkot liuotetaan typpihappoon. Kaikki uraani (ja muut ydinmuunnosten seurauksena syntyneet metallit) muuttuu nitraattisuoloiksi. Tässä tapauksessa jotkut epäpuhtaudet, kuten ksenon, jodi, poistuvat automaattisesti kaasujen tai höyryjen muodossa, kun taas toiset, kuten tina, jäävät sedimenttiin.
Mutta saatu liuos sisältää uraanin lisäksi monien metallien, erityisesti plutoniumin, neptuniumin, harvinaisten maametallien, teknetiumin ja joidenkin muiden epäpuhtauksia. Täällä tulee sisään orgaaninen aine. Uraanin ja epäpuhtauksien liuos typpihapossa sekoitetaan orgaanisen aineen - tributyylifosfaatin - liuokseen. Tässä tapauksessa lähes kaikki uraani siirtyy orgaaniseen faasiin, kun taas epäpuhtaudet jäävät typpihappoliuokseen.
Tätä prosessia kutsutaan uuttamiseksi. Kahden uuton jälkeen uraani on lähes epäpuhtaudeton ja sitä voidaan käyttää uudelleen uraanilohkojen valmistukseen. Ja loput epäpuhtaudet menevät edelleen erotukseen. Niistä erotetaan tärkeimmät osat: plutonium, joitain radioaktiivisia isotooppeja.
Samoin zirkonium ja hafnium voidaan erottaa.
Uuttoprosesseja käytetään nykyään laajalti tekniikassa. Heidän avullaan he eivät ainoastaan puhdista epäorgaanisia yhdisteitä, vaan myös monia orgaanisia aineita - vitamiineja, rasvoja, alkaloideja.
Kemia valkoisessa takissa
Hän kantoi soinnoivaa nimeä - Johann Bombast Theophrastus Paracelsus von Hohenheim. Paracelsus ei ole sukunimi, vaan eräänlainen titteli. Käännetty venäjäksi, se tarkoittaa "super-suuria". Paracelsus oli erinomainen kemisti, ja suosittu huhu kutsui häntä ihmeparantajaksi. Koska hän ei ollut vain kemisti, vaan myös lääkäri.
Keskiajalla kemian ja lääketieteen liitto vahvistui. Kemia ei ollut vielä ansainnut oikeutta kutsua sitä tieteeksi. Hänen näkemyksensä olivat liian epämääräisiä, ja hänen voimansa hajaantuivat turhaan pahamaineisen viisasten kiven etsimiseen.
Mutta mystiikan verkoissa höperöllä kemia oppi parantamaan ihmisiä vakavista sairauksista. Näin syntyi iatrokemia. Tai lääketieteellinen kemia. Ja monia kemistejä 1500-, 1700- ja 1700-luvuilla kutsuttiin farmaseuteiksi, proviisoreiksi. Vaikka he harjoittivat puhdasta kemiaa, he valmistivat erilaisia parantavia juomia. Totta, he olivat sokeita. Eikä aina näistä "lääkkeistä" ole ollut hyötyä ihmiselle.
"Apteekkarien" joukossa Paracelsus oli yksi näkyvimmistä. Hänen lääkkeiden luetteloon kuuluivat elohopea- ja rikkivoiteet (muuten niitä käytetään edelleen ihosairauksien hoitoon), rauta- ja antimonisuolat sekä erilaiset kasvismehut.

Aluksi kemia pystyi antamaan lääkäreille vain luonnossa olevia aineita. Ja sitä on erittäin rajoitettu määrä. Mutta lääke ei riittänyt.
Jos selaamme nykyaikaisia reseptioppaita, huomaamme, että 25 prosenttia lääkkeistä on niin sanotusti luonnollisia valmisteita. Niiden joukossa on eri kasveista valmistettuja uutteita, tinktuuroita ja keitteitä. Kaikki muu on keinotekoisesti syntetisoituja, luonnolle tuntemattomia lääkeaineita. Kemian voimalla luodut aineet.
Ensimmäinen lääkeaineen synteesi tehtiin noin 100 vuotta sitten. Salisyylihapon parantava vaikutus reumaan on tiedetty pitkään. Mutta sen uuttaminen kasviraaka-aineista oli sekä vaikeaa että kallista. Vasta vuonna 1874 oli mahdollista kehittää yksinkertainen menetelmä salisyylihapon saamiseksi fenolista.
Tämä happo muodosti perustan monille lääkkeille. Esimerkiksi aspiriini. Pääsääntöisesti lääkkeiden "elämän" aika on lyhyt: vanhat korvataan uusilla, edistyneemmillä, kehittyneemmillä taistelussa erilaisia vaivoja vastaan. Aspiriini on poikkeus tässä suhteessa. Joka vuosi se paljastaa uusia, aiemmin tuntemattomia hämmästyttäviä ominaisuuksia. Osoittautuu, että aspiriini ei ole vain kuumetta alentava ja kipulääke, vaan sen käyttöalue on paljon laajempi.
Hyvin "vanha" lääke on tunnettu pyramidoni (hänen syntymävuosi on 1896).
Nyt yhden päivän sisällä kemistit syntetisoivat useita uusia lääkkeitä. Monilla ominaisuuksilla, monenlaisia sairauksia vastaan. Kipua torjuvista lääkkeistä mielisairautta parantaviin lääkkeisiin.
Parantaa ihmisiä - kemistillä ei ole jalompaa tehtävää. Mutta vaikeampaa tehtävää ei ole.
Saksalainen kemisti Paul Ehrlich yritti useiden vuosien ajan syntetisoida lääkettä kauheaa sairautta - unihäiriötä - vastaan. Jokaisessa synteesissä jotain onnistui, mutta joka kerta Ehrlich pysyi tyytymättömänä. Vain 606. yrityksellä oli mahdollista saada tehokas lääke - salvarsan, ja kymmenet tuhannet ihmiset pystyivät toipumaan paitsi nukkumisesta myös toisesta salakavalasta taudista - kupasta. Ja 914. yrityksellä Erlich sai vielä tehokkaamman lääkkeen - neosalvarsanin.
Lääkkeen tie kemikaalipullosta apteekin tiskille on pitkä. Tämä on lääketieteen laki: ennen kuin lääkettä on testattu perusteellisesti, sitä ei voida suositella käytettäväksi. Ja kun tätä sääntöä ei noudateta, tapahtuu traagisia virheitä. Ei niin kauan sitten länsisaksalaiset lääkeyritykset mainostivat uutta unilääkettä - tolidomidia. Pieni valkoinen pilleri syöksyi nopeaan ja syvään uneen jatkuvasta unettomuudesta kärsivän henkilön. Ylistystä laulettiin tolidomidia, ja hän osoittautui hirvittäväksi viholliseksi vauvoille, jotka eivät olleet vielä syntyneet. Kymmeniä tuhansia syntyneitä friikkejä - ihmiset maksoivat sellaisen hinnan siitä, että he kiirehtivät laittamaan riittämättömästi testatun lääkkeen myyntiin.
Ja siksi kemistien ja lääkäreiden on tärkeää tietää paitsi, että tällainen ja sellainen lääke parantaa menestyksekkäästi sellaista ja sellaista sairautta. Heidän on ymmärrettävä huolellisesti, miten se toimii, mikä on sen taudin torjunnan hienovarainen kemiallinen mekanismi.

Tässä pieni esimerkki. Nyt niin sanottujen barbituurihappojen johdannaisia käytetään usein unilääkkeinä. Nämä yhdisteet sisältävät hiili-, vety-, typpi- ja happiatomeja. Lisäksi yhteen hiiliatomeista on kiinnittynyt kaksi niin kutsuttua alkyyliryhmää, eli hiilivetymolekyyliä, joissa ei ole yhtä vetyatomia. Ja tähän kemistit tulivat. Vain silloin barbituurihapolla on hypnoottinen vaikutus, kun alkyyliryhmien hiiliatomien summa on vähintään neljä. Ja mitä suurempi tämä määrä, sitä pidempään ja nopeammin lääke vaikuttaa.
Mitä syvemmälle tiedemiehet tunkeutuvat sairauksien luonteeseen, sitä perusteellisemmin kemistit tekevät tutkimusta. Ja yhä tarkemmasta tieteestä on tulossa farmakologiaa, joka aiemmin harjoitti vain erilaisten lääkkeiden valmistusta ja suosituksia niiden käytöstä eri sairauksia vastaan. Nyt farmakologin tulisi olla kemisti, biologi, lääkäri ja biokemisti. Älä koskaan toista tolidomidin tragedioita.
Lääkeaineiden synteesi on yksi kemistien, toisen luonnon luojien, tärkeimmistä saavutuksista.
... Vuosisadamme alussa kemistit yrittivät itsepintaisesti valmistaa uusia väriaineita. Ja niin kutsuttu sulfaniilihappo otettiin lähtötuotteeksi. Sillä on erittäin "joustava" molekyyli, joka kykenee erilaisiin uudelleenjärjestelyihin. Joissakin tapauksissa kemistit päättelivät, että sulfaniilihappomolekyyli voitaisiin muuttaa arvokkaaksi väriainemolekyyliksi.
Ja niin kävi todellisuudessa. Mutta vuoteen 1935 asti kukaan ei uskonut, että synteettiset sulfanyylivärit olisivat myös tehokkaita huumeita. Väriaineiden tavoittelu haihtui taustalle: kemistit alkoivat metsästää uusia lääkkeitä, joita kutsuttiin yhteisesti sulfalääkkeiksi. Tässä ovat tunnetuimpien nimet: sulfidiini, streptosidi, sulfatsoli, sulfadimetsiini. Tällä hetkellä sulfonamidit ovat yksi ensimmäisistä paikoista mikrobien torjuntakeinojen joukossa.
... Etelä-Amerikan intiaanit tuottivat chilibukha-kasvin kuoresta ja juurista tappavan myrkyn - curaren. Nuolen, jonka kärki oli kastettu curareen, osuma vihollinen kuoli välittömästi.
Miksi? Vastatakseen tähän kysymykseen kemistien oli ymmärrettävä perusteellisesti myrkyn mysteeri.
He havaitsivat, että curaren tärkein aktiivinen ainesosa on alkaloidi tubokurariini. Kun se tulee kehoon, lihakset eivät voi supistua. Lihakset muuttuvat liikkumattomiksi. Ihminen menettää kykynsä hengittää. Kuolema on tulossa.
Tietyissä olosuhteissa tämä myrkky voi kuitenkin olla hyödyllistä. Siitä voi olla hyötyä kirurgeille, kun he suorittavat erittäin monimutkaisia operaatioita. Esimerkiksi sydämessä. Kun sinun täytyy sammuttaa keuhkolihakset ja siirtää kehon tekohengitykseen. Joten kuolevainen vihollinen toimii ystävänä. Tubokurariini on tulossa kliiniseen käytäntöön.
Se on kuitenkin liian kallista. Ja tarvitsemme lääkkeen, joka on halpa ja edullinen.
Kemistit puuttuivat jälleen asiaan. Kaikessa suhteessa he tutkivat tubokurariinimolekyyliä. He jakoivat sen eri osiin, tutkivat tuloksena olevia "fragmentteja" ja selvittivät askel askeleelta lääkkeen kemiallisen rakenteen ja fysiologisen aktiivisuuden välisen suhteen. Kävi ilmi, että sen toiminnan määräävät erityiset ryhmät, jotka sisältävät positiivisesti varautuneen typpiatomin. Ja että ryhmien välinen etäisyys tulisi määritellä tarkasti.
Nyt kemistit voisivat lähteä luonnon jäljittelyn polulle. Ja jopa yrittää ylittää se. Ensin he saivat lääkkeen, joka ei ole teholtaan huonompi kuin tubokurariini. Ja sitten he paransivat sitä. Näin syntyi sinkurin; se on kaksi kertaa niin aktiivinen kuin tubokurariini.
Ja tässä vielä silmiinpistävämpi esimerkki. Taistele malariaa vastaan. Häntä hoidettiin kiniinillä (tai tieteellisesti kiniinillä), luonnollisella alkaloidilla. Kemistit onnistuivat myös luomaan plasmokiinin - aineen, joka on kuusikymmentä kertaa aktiivisempi kuin kiniini.
Nykyaikaisella lääketieteellä on valtava työkaluarsenaali, niin sanotusti, kaikkiin tilanteisiin. Lähes kaikkia tunnettuja sairauksia vastaan.
On olemassa tehokkaita lääkkeitä, jotka rauhoittavat hermostoa ja palauttavat rauhan jopa ärtyneimmälle henkilölle. On olemassa esimerkiksi lääke, joka poistaa pelon tunteen kokonaan. Kukaan ei tietenkään suosittelisi sitä opiskelijalle, joka pelkää koetta.
On olemassa koko joukko niin sanottuja rauhoittavia lääkkeitä, rauhoittavia lääkkeitä. Näitä ovat esimerkiksi reserpiini. Sen käytöllä tiettyjen mielenterveyssairauksien (skitsofrenian) hoidossa oli aikansa valtava rooli. Kemoterapialla on nyt ensimmäinen paikka taistelussa mielenterveyshäiriöitä vastaan.
Lääkekemian saavutukset eivät kuitenkaan aina muutu positiiviseksi. On olemassa esimerkiksi sellainen pahaenteinen (muuten sitä on vaikea kutsua) lääke kuin LSD-25.
Monissa kapitalistisissa maissa sitä käytetään lääkkeenä, joka aiheuttaa keinotekoisesti erilaisia skitsofrenian oireita (kaikenlaisia hallusinaatioita, joiden avulla voit luopua "maallisista vaikeuksista" joksikin aikaa). Mutta oli monia tapauksia, joissa LSD-25-pillereitä käyttäneet ihmiset eivät palanneet normaalitilaansa.
Nykyaikaiset tilastot osoittavat, että suurin osa kuolemista maailmassa johtuu sydänkohtauksista tai aivoverenvuodoista (halvauksista). Kemistit taistelevat näitä vihollisia vastaan keksimällä erilaisia sydänlääkkeitä ja valmistamalla lääkkeitä, jotka laajentavat aivojen verisuonia.
Kemistien syntetisoimien Tubazidin ja PAS:n avulla lääkärit onnistuvat voittamaan tuberkuloosin.
Ja lopuksi, tiedemiehet etsivät itsepäisesti tapoja torjua syöpää - tätä ihmiskunnan kauheaa vitsausta. Täällä on vielä paljon epäselvää ja tuntematonta.
Lääkärit odottavat uusia ihmeaineita kemistiltä. He odottavat turhaan. Täällä kemia ei ole vielä osoittanut, mihin se pystyy.
Muodin ihme
Tämä sana on tunnettu jo kauan. Lääkärit ja mikrobiologit. Mainittu erikoiskirjoissa. Mutta mitään ei sanottu ihmiselle, joka on kaukana biologiasta ja lääketieteestä. Ja harvinainen kemisti tiesi sen merkityksen. Nyt kaikki tuntevat hänet.
Sana on "antibiootit".
Mutta jopa aikaisemmin kuin sanalla "antibiootit", henkilö tutustui sanaan "mikrobit". Todettiin, että useat sairaudet, kuten keuhkokuume, aivokalvontulehdus, punatauti, lavantauti, tuberkuloosi ja muut, johtuvat mikro-organismeista. Niiden torjumiseen tarvitaan antibiootteja.
Jo keskiajalla tiedettiin tiettyjen hometyyppien parantava vaikutus. Totta, keskiaikaisen Aesculapiuksen esitykset olivat melko omituisia. Esimerkiksi uskottiin, että vain hirtettyjen tai rikoksista teloitettujen ihmisten kalloista otetut muotit auttavat taistelussa sairauksia vastaan.
Mutta tämä ei ole välttämätöntä. Merkittävästi erilainen: englantilainen kemisti Alexander Fleming, joka tutki yhtä hometyyppiä, eristi siitä aktiivisen aineen. Näin syntyi penisilliini, ensimmäinen antibiootti.
Kävi ilmi, että penisilliini on erinomainen ase taistelussa monia taudinaiheuttajia vastaan: streptokokit, stafylokokit jne. Se pystyy voittamaan jopa vaalean spirokeetin, kupan aiheuttajan.
Mutta vaikka Alexander Fleming löysi penisilliinin vuonna 1928, tämän lääkkeen kaava selvitettiin vasta vuonna 1945. Ja jo vuonna 1947 oli mahdollista suorittaa täydellinen penisilliinisynteesi laboratoriossa. Näytti siltä, että tällä kertaa ihminen tarttui luontoon. Se ei kuitenkaan ollut siellä. Penisilliinin laboratoriosynteesin suorittaminen ei ole helppo tehtävä. Paljon helpompi saada se muotista.
Mutta kemistit eivät perääntyneet. Ja täällä he saivat sanoa mielipiteensä. Ei ehkä sanaakaan sanottavana, mutta teko on tehtävä. Tärkeintä on, että muotti, josta penisilliiniä tavallisesti saatiin, on hyvin vähän "tuottava". Ja tutkijat päättivät lisätä sen tuottavuutta.
He ratkaisivat tämän ongelman löytämällä aineita, jotka joutuessaan mikro-organismin perinnölliseen laitteeseen muuttivat sen ominaisuuksia. Lisäksi uusia merkkejä pystyttiin perimään. Heidän avullaan he onnistuivat kehittämään uuden "sienirodun", joka oli paljon aktiivisempi penisilliinin tuotannossa.
Nyt antibioottien sarja on erittäin vaikuttava: streptomysiini ja terramysiini, tetrasykliini ja aureomysiini, biomysiini ja erytromysiini. Kaiken kaikkiaan monimuotoisimpia antibiootteja tunnetaan nykyään noin tuhat ja niistä noin sata käytetään erilaisten sairauksien hoitoon. Ja kemialla on merkittävä rooli niiden valmistuksessa.
Sen jälkeen kun mikrobiologit ovat keränneet niin sanotun viljelynesteen, joka sisältää mikro-organismipesäkkeitä, on kemistien vuoro.
Juuri heidän edessään on eristää antibiootit, "aktiivinen periaate". Monimutkaisten orgaanisten yhdisteiden uuttamiseksi luonnollisista "raaka-aineista" otetaan käyttöön erilaisia kemiallisia menetelmiä. Antibiootit imeytyvät erityisillä imeytysaineilla. Tutkijat käyttävät "kemiallisia kynsiä" - he uuttavat antibiootteja erilaisilla liuottimilla. Puhdistettu ioninvaihtohartseilla, saostettu liuoksista. Näin saadaan raaka antibiootti, jolle suoritetaan jälleen pitkä puhdistussykli, kunnes lopulta se ilmestyy puhtaan kiteisen aineen muodossa.
Jotkut, kuten penisilliini, syntetisoidaan edelleen mikro-organismien avulla. Mutta muiden hankkiminen on vain puolet luonnon työstä.
Mutta on myös sellaisia antibiootteja, esimerkiksi syntomysiini, jossa kemistit luopuvat kokonaan luonnon palveluista. Tämän lääkkeen synteesi alusta loppuun suoritetaan tehtaissa.
Ilman tehokkaita kemian menetelmiä sana "antibiootti" ei olisi koskaan saavuttanut näin laajaa suosiota. Eikä olisi ollut sitä aitoa vallankumousta lääkkeiden käytössä, monien sairauksien hoidossa, joita nämä antibiootit ovat tuottaneet.
Mikroelementit - kasvivitamiinit
Sanalla "elementti" on monia merkityksiä. Niinpä niitä kutsutaan esimerkiksi samanlaisiksi atomeiksi, joilla on sama ydinvaraus. Mitä ovat "mikroravinteet"? Niin sanottuja kemiallisia alkuaineita, joita eläin- ja kasviorganismeissa on hyvin pieniä määriä. Joten ihmiskehossa 65 prosenttia happea, noin 18 prosenttia hiiltä, 10 prosenttia vetyä. Nämä ovat makroravinteita, niitä on monia. Mutta titaani ja alumiini ovat vain yksi tuhannesosa prosenttia - niitä voidaan kutsua mikroelementeiksi.
Biokemian alkuaikoina tällaiset pienet asiat jätettiin huomiotta. Ajatelkaapa joitakin prosentin sadasosia tai tuhannesosia. Tällaisia määriä ei silloin voitu määrittää.
Analyysitekniikka ja -menetelmät paranivat, ja tutkijat löysivät yhä enemmän elementtejä elävistä esineistä. Hivenaineiden roolia ei kuitenkaan saatu selville pitkään aikaan. Huolimatta siitä, että kemiallinen analyysi mahdollistaa prosentin miljoonasosien ja jopa sadan miljoonasosan määrittämisen lähes kaikista näytteistä, ei monien hivenainesten merkitystä kasvien ja eläinten elintärkeälle toiminnalle ole vielä selvitetty.
Mutta jotkut asiat ovat jo tiedossa. Esimerkiksi, että eri organismeissa on alkuaineita, kuten koboltti, boori, kupari, mangaani, vanadiini, jodi, fluori, molybdeeni, sinkki ja jopa ... radiumia. Kyllä, se on radiumia, vaikkakin mitättömiä määriä.
Muuten, noin 70 kemiallista alkuainetta on nyt löydetty ihmiskehosta, ja on syytä uskoa, että koko jaksollinen järjestelmä sisältyy ihmisen elimiin. Lisäksi jokaisella elementillä on jokin hyvin erityinen rooli. On jopa sitä mieltä, että monet sairaudet johtuvat kehon mikroelementtitasapainon rikkomisesta.
Raudalla ja mangaanilla on tärkeä rooli kasvien fotosynteesin prosessissa. Jos kasvatat kasvin maaperässä, jossa ei ole edes jäämiä rautaa, sen lehdet ja varret ovat valkoisia kuin paperi. Mutta kannattaa ruiskuttaa tällainen kasvi rautasuolojen liuoksella, koska se saa luonnollisen vihreän värinsä. Kupari on myös välttämätön fotosynteesiprosessissa ja vaikuttaa typpiyhdisteiden imeytymiseen kasviorganismeissa. Kun kasveissa ei ole riittävästi kuparia, proteiinit muodostuvat erittäin heikosti, jotka sisältävät typpeä.

Molybdeenin monimutkaiset orgaaniset yhdisteet sisältyvät komponentteina eri entsyymeihin. Ne edistävät typen parempaa imeytymistä. Molybdeenin puute johtaa joskus lehtien palovammoihin, koska niihin kertyy runsaasti typpihapposuoloja, jotka molybdeenin puuttuessa kasvit eivät imeydy. Ja molybdeenillä on vaikutusta kasvien fosforipitoisuuteen. Sen puuttuessa epäorgaaniset fosfaatit eivät muutu orgaanisiksi. Molybdeenin puute vaikuttaa myös pigmenttien (väriaineiden) kertymiseen kasveihin - lehtien pilkku ja vaalea väri näkyvät.
Boorin puuttuessa kasvit eivät ime fosforia hyvin. Boori edistää myös erilaisten sokereiden parempaa liikkumista kasvijärjestelmän läpi.
Hivenaineilla on tärkeä rooli paitsi kasveissa myös eläinorganismeissa. Kävi ilmi, että vanadiinin täydellinen puuttuminen eläinten ruoasta aiheuttaa ruokahaluttomuuden ja jopa kuoleman. Samanaikaisesti lisääntynyt vanadiinipitoisuus sikojen ruokavaliossa johtaa niiden nopeaan kasvuun ja paksun rasvakerroksen laskeutumiseen.
Esimerkiksi sinkillä on tärkeä rooli aineenvaihdunnassa ja se on eläinten punasolujen ainesosa.
Maksa, jos eläin (ja jopa ihminen) on kiihtyneessä tilassa, vapauttaa yleiseen verenkiertoon mangaania, piitä, alumiinia, titaania ja kuparia, mutta keskushermoston estyessä mangaania, kuparia ja titaania ja piin ja alumiinin vapautumisen viiveet. Maksan lisäksi aivot, munuaiset, keuhkot ja lihakset osallistuvat kehon veren hivenainepitoisuuden säätelyyn.
Mikroelementtien roolin selvittäminen kasvien ja eläinten kasvu- ja kehitysprosesseissa on tärkeä ja kiehtova kemian ja biologian tehtävä. Lähitulevaisuudessa tämä johtaa varmasti erittäin merkittäviin tuloksiin. Ja se avaa tieteelle vielä yhden tavan luoda toinen luonto.
Mitä kasvit syövät ja mitä tekemistä kemialla on sen kanssa?
Jopa antiikin kokit olivat kuuluisia kulinaarisista menestyksestään. Kuninkaallisten palatsin pöydät olivat täynnä herkullisia ruokia. Rikkaista ihmisistä tuli nirsoja syöjiä.
Kasvit näyttivät olevan paljon vaatimattomampia. Ja helteisessä autiomaassa ja napatundrassa ruohoa ja pensaita esiintyi rinnakkain. Olkoon kitukasvuinen, jopa kurja, mutta tuli toimeen.
Niiden kehittymiseen tarvittiin jotain. Mutta mitä? Tiedemiehet ovat etsineet tätä mystistä "jotain" monta vuotta. He järjestivät kokeita. Keskusteltiin tuloksista.
Mutta ei ollut selvyyttä.
Kuuluisa saksalainen kemisti Justus Liebig esitteli sen viime vuosisadan puolivälissä. Häntä auttoi kemiallinen analyysi. Tiedemies "hajotti" monipuolisimmat kasvit erillisiksi kemiallisiksi alkuaineiksi. Aluksi niitä ei ollut paljon. Vain kymmenen: hiili ja vety, happi ja typpi, kalsium ja kalium, fosfori ja rikki, magnesium ja rauta. Mutta tämä kymmenen sai vihreän valtameren raivoamaan maapallolla.
Tästä seurasi johtopäätös: elääkseen kasvin on jotenkin omaksuttava, "syötävä" nimetyt alkuaineet.
Miten tarkalleen? Missä kasviruokakaupat sijaitsevat?
Maaperässä, vedessä, ilmassa.
Mutta ihmeellisiä asioita tapahtui. Joillakin maaperäillä kasvi kehittyi nopeasti, kukki ja kantoi hedelmää. Toisilla se sairastui, kuivui ja muuttui haalistuneeksi kummaksi. Koska näistä maaperistä puuttui joitain elementtejä.
Jo ennen Liebigia ihmiset tiesivät jotain muuta. Vaikka samoja viljelykasveja kylvettäisiin vuodesta toiseen hedelmällisimpään maahan, sato huononee ja huononee.
Maaperä oli tyhjentynyt. Kasvit "söivät" vähitellen kaikki sen sisältämät tarvittavat kemialliset alkuaineet.
Oli tarpeen "ruokkia" maaperää. Lisää siihen puuttuvat aineet, lannoitteet. Niitä on käytetty antiikista lähtien. Sovelletaan intuitiivisesti esi-isiensä kokemuksen perusteella.

Liebig nosti lannoitteiden käytön tieteen tasolle. Näin syntyi agrokemia. Kemiasta on tullut kasvintuotannon palvelija. Hänen edessään syntyi tehtävä: opettaa ihmisiä käyttämään tunnettuja lannoitteita oikein ja keksimään uusia.
Nyt käytössä on kymmeniä erilaisia lannoitteita. Ja tärkeimmät niistä ovat kalium, typpi ja fosfori. Koska kalium, typpi ja fosfori ovat alkuaineita, joita ilman mikään kasvi ei kasva.
Pieni analogia tai kuinka kemistit ruokkivat kasveja kaliumilla
... Oli aika, jolloin nyt niin kuuluisa uraani käpertyi jonnekin kemian etujen takapihalle. Ainoastaan lasien väritys ja valokuvaus esittivät arkoja vaatimuksia häntä vastaan. Myöhemmin radiumia löydettiin uraanista. Tuhansista tonneista uraanimalmeista uutettiin merkityksetön hopeametallirae. Ja jätteet, jotka sisälsivät valtavia määriä uraania, sotkivat edelleen tehtaan varastoja. Viimeinkin uraanin tunti on koittanut. Kävi ilmi, että juuri hän antaa ihmiselle vallan käyttää atomienergiaa. Jäteestä on tullut aarre.
... Saksan Stassfurtin suolaesiintymät ovat olleet tiedossa pitkään. Ne sisälsivät monia suoloja, pääasiassa kaliumia ja natriumia. Natriumsuola, ruokasuola, löytyi heti käyttöön. Kaliumsuolat heitettiin pois katumatta. Valtavia vuoria niistä kasautui kaivosten lähelle. Ja ihmiset eivät tienneet mitä tehdä heidän kanssaan. Maatalous tarvitsi kipeästi kaliumlannoitteita, mutta Stassfurtin jätettä ei voitu käyttää. Ne sisälsivät paljon magnesiumia. Ja hän, joka oli hyödyllinen kasveille pieninä annoksina, osoittautui tuhoisaksi suurina annoksina.
Tässä kemia auttaa. Hän löysi yksinkertaisen menetelmän magnesiumin poistamiseksi kaliumsuoloista. Ja Stassfurtin kaivoksia ympäröivät vuoret alkoivat sulaa silmiemme edessä. Tieteen historioitsijat raportoivat seuraavan tosiasian: Saksaan rakennettiin vuonna 1811 ensimmäinen potaskan käsittelylaitos. Vuotta myöhemmin niitä oli jo neljä, ja vuonna 1872 Saksassa 33 tehdasta käsitteli yli puoli miljoonaa tonnia raakasuolaa.
Pian sen jälkeen moniin maihin perustettiin tehtaita kaliumlannoitteiden tuotantoa varten. Ja nyt monissa maissa potaskan raaka-aineiden uuttaminen on monta kertaa suurempi kuin ruokasuolan uuttaminen.
"Typpikatastrofi"
Noin sata vuotta typen löytämisen jälkeen yksi suurimmista mikrobiologeista kirjoitti: "Typpi on yleisestä biologisesta näkökulmasta arvokkaampaa kuin harvinaisimmat jalometallit." Ja hän oli täysin oikeassa. Loppujen lopuksi typpi on olennainen osa melkein kaikkia proteiinimolekyylejä, sekä kasveja että eläimiä. Ei typpeä, ei proteiinia. Ja ei proteiinia - ei elämää. Engels sanoi, että "elämä on proteiinikappaleiden olemassaolon muoto."
Kasvit tarvitsevat typpeä proteiinimolekyylien muodostamiseen. Mutta mistä he saavat sen? Typelle on ominaista alhainen kemiallinen aktiivisuus. Normaaleissa olosuhteissa se ei reagoi. Siksi kasvit eivät voi käyttää ilmakehän typpeä. Aivan sama: "... vaikka silmä näkee, mutta hammas on tunnoton." Joten kasvien typpivarasto on maaperä. Valitettavasti ruokakomero on melko huono. Siinä ei ole tarpeeksi typpeä sisältäviä yhdisteitä. Siksi maaperä hukkaa nopeasti typensä, ja sitä on rikastettava edelleen. Levitä typpilannoitteita.
Nyt käsitteestä "chilen salpetteri" on tullut historian osa. Ja noin seitsemänkymmentä vuotta sitten se ei lähtenyt huulilta.
Chilen tasavallan laajoilla alueilla ulottuu synkkä Atacaman autiomaa. Se ulottuu satoja kilometrejä. Ensi silmäyksellä tämä on tavallisin autiomaa, mutta yksi omituinen seikka erottaa sen muista maapallon aavikoista: ohuen hiekkakerroksen alla on voimakkaita natriumnitraatin tai natriumnitraatin kerrostumia. Nämä esiintymät ovat olleet tiedossa pitkään, mutta ehkä ne muistettiin ensimmäisen kerran, kun Euroopassa oli pula ruudista. Itse asiassa ruudin valmistukseen käytettiin aiemmin hiiltä, rikkiä ja salpetaria.

Retkikunta varustettiin kiireellisesti toimittamaan merentakaisia tuotteita. Koko lasti jouduttiin kuitenkin heittämään mereen. Kävi ilmi, että ruudin valmistukseen soveltui vain kaliumnitraatti. Natrium imesi ahneesti kosteutta ilmasta, ruuti kostui, eikä sitä voinut käyttää.
Ei ensimmäinen kerta, kun eurooppalaiset joutuivat heittämään ulkomaista lastia mereen. 1600-luvulla Platino del Pino -joen rannoilta löydettiin platinaksi kutsutun valkoisen metallin rakeita. Platina tuli Eurooppaan ensimmäisen kerran vuonna 1735. Mutta he eivät oikein tienneet mitä tehdä hänen kanssaan. Jalometalleista tunnettiin tuolloin vain kulta ja hopea, eikä platina löytänyt itselleen markkinoita. Mutta taitavat ihmiset huomasivat, että platina ja kulta ovat melko lähellä toisiaan ominaispainon suhteen. He käyttivät tätä hyväkseen ja alkoivat lisätä platinaa kultaan, jota käytettiin kolikoiden valmistukseen. Se oli jo väärennös. Espanjan hallitus kielsi platinan tuonnin, ja osavaltiossa vielä jäljellä olevat varannot kerättiin ja hukkuivat mereen lukuisten todistajien läsnäollessa.
Mutta tarina Chilen salpetterin kanssa ei päättynyt tähän. Se osoittautui erinomaiseksi typpilannoitteeksi, jonka luonto tarjoaa ihmiselle suotuisasti. Muita typpilannoitteita ei tuolloin tunnettu. Natriumnitraatin luonnollisten esiintymien intensiivinen kehitys alkoi. Chilen Ikvikwen satamasta laivat kulkivat päivittäin toimittaen näin arvokasta lannoitetta kaikkialle maailmaan.
... Vuonna 1898 maailma järkyttyi kuuluisan Crookesin synkästä ennustuksesta. Puheessaan hän ennusti ihmiskunnalle kuolemaa typen nälkään. Joka vuosi sadonkorjuun myötä pelloilta puuttuu typpeä, ja Chilen salpietariesiintymiä kehitetään vähitellen. Atacaman aavikon aarteet osoittautuivat pisaraksi meressä.
Sitten tiedemiehet muistivat ilmapiirin. Ehkä ensimmäinen henkilö, joka kiinnitti huomiota ilmakehän rajattomiin typpivaroihin, oli kuuluisa tiedemiehemme Kliment Arkadyevich Timiryazev. Timiryazev uskoi syvästi tieteeseen ja ihmisen nerouden voimaan. Hän ei jakanut Crookesin huolia. Ihmiskunta voittaa typpikatastrofin, selviää vaikeuksista, Timirjazev uskoi. Ja hän osoittautui oikeaksi. Jo vuonna 1908 tutkijat Birkeland ja Eide Norjassa kiinnittivät teollisessa mittakaavassa ilmakehän typpeä sähkökaaren avulla.
Samaan aikaan Saksassa Fritz Haber kehitti menetelmän ammoniakin valmistamiseksi typestä ja vedystä. Siten kasvien ravinnon kannalta välttämättömän sitoutuneen typen ongelma lopulta ratkesi. Ja ilmakehässä on paljon vapaata typpeä: tutkijat ovat laskeneet, että jos kaikki ilmakehän typpi muutetaan lannoitteeksi, tämä riittää kasveille yli miljoonaksi vuodeksi.
Mihin fosfori on tarkoitettu?
Justus Liebig uskoi, että kasvi voi imeä typpeä ilmasta. Maaperää on tarpeen lannoittaa vain kaliumilla ja fosforilla. Mutta juuri näiden elementtien kanssa hän ei ollut onnekas. Hänen "patentoitu lannoitteensa", jonka yksi englantilaisista yrityksistä sitoutui tuottamaan, ei johtanut sadon kasvuun. Vasta monien vuosien jälkeen Liebig ymmärsi ja myönsi avoimesti virheensä. Hän käytti liukenemattomia fosfaattisuoloja peläten, että hyvin liukenevat suolat huuhtoutuisivat nopeasti pois maaperästä sateen vaikutuksesta. Mutta kävi ilmi, että kasvit eivät pysty absorboimaan fosforia liukenemattomista fosfaateista. Ja ihmisen piti valmistaa eräänlainen "puolivalmiste" kasveille.
Joka vuosi maailman pellolta otetaan noin 10 miljoonaa tonnia fosforihappoa. Miksi kasvit tarvitsevat fosforia? Loppujen lopuksi se ei ole osa rasvoja tai hiilihydraatteja. Ja monet proteiinimolekyylit, varsinkin yksinkertaisimmat, eivät sisällä fosforia. Mutta ilman fosforia kaikki nämä yhdisteet eivät yksinkertaisesti voi muodostua.
Fotosynteesi ei ole vain hiilihydraattien synteesiä hiilidioksidista ja vedestä, jota kasvi "vitsillä" tuottaa. Tämä on monimutkainen prosessi. Fotosynteesi tapahtuu niin kutsutuissa kloroplasteissa - eräänlaisissa kasvisolujen "elimissä". Kloroplastien koostumus sisältää vain paljon fosforiyhdisteitä. Karkeasti ottaen kloroplastit voidaan kuvitella eläimen mahalaukun muodossa, jossa ruoka sulatetaan ja assimiloituu, koska juuri ne käsittelevät kasvien suoria "rakennuspalikoita": hiilidioksidia ja vettä.
Kasvit imevät hiilidioksidia ilmasta fosforiyhdisteiden avulla. Epäorgaaniset fosfaatit muuttavat hiilidioksidin hiilihappoanioneiksi, jotka myöhemmin muodostavat monimutkaisia orgaanisia molekyylejä.
Fosforin rooli kasvien elämässä ei tietenkään rajoitu tähän. Eikä voida sanoa, että sen merkitys kasveille olisi jo täysin selvitetty. Kuitenkin myös se, mitä tiedetään, osoittaa tärkeän roolinsa heidän elämässään.
Kemiallinen sodankäynti
Tämä on todella sota. Vain ilman aseita ja tankkeja, raketteja ja pommeja. Tämä on "hiljaista", joskus monille näkymätöntä sotaa ei elämästä, vaan kuolemasta. Ja voitto siinä on onnea kaikille ihmisille.
Kuinka paljon haittaa on esimerkiksi tavallisesta käpälästä? Osoittautuu, että tämä ilkeä olento tuottaa tappiota, pelkästään maassamme, arviolta miljoonia ruplaa vuodessa. Entä rikkaruohot? Pelkästään Yhdysvalloissa niiden olemassaolon arvo on neljä miljardia dollaria. Tai ota heinäsirkat, todellinen katastrofi, joka muuttaa kukkivat pellot paljaaksi, elottomaksi maaksi. Jos laskemme kaikki vahingot, joita kasvi- ja eläinsaalistajat aiheuttavat maailman maataloudelle yhden vuoden aikana, tulee käsittämätön määrä. Näillä rahoilla 200 miljoonaa ihmistä voitaisiin ruokkia ilmaiseksi koko vuoden!
Mikä on "cide" käännettynä venäjäksi? Se tarkoittaa tappajaa. Ja niin kemistit ottivat käyttöön erilaisten "sidosten" luomisen. He loivat hyönteismyrkkyjä - "tappaa hyönteisiä", eläinmyrkkyjä - "tappaa jyrsijöitä", rikkakasvien torjunta-aineita - "tappaa ruohoa". Kaikkia näitä "sidejä" käytetään nykyään laajalti maataloudessa.
Ennen toista maailmansotaa epäorgaanisia torjunta-aineita käytettiin laajalti. Erilaisia jyrsijöitä ja hyönteisiä, rikkaruohoja käsiteltiin arseenilla, rikillä, kuparilla, bariumilla, fluorilla ja monilla muilla myrkyllisillä yhdisteillä. Kuitenkin 40-luvun puolivälistä lähtien orgaaniset torjunta-aineet ovat yleistymässä. Tällainen "rulla" orgaanisten yhdisteiden suuntaan tehtiin varsin tarkoituksella. Asia ei ole vain siinä, että ne osoittautuivat vaarattomiksi ihmisille ja kotieläimille. Niillä on enemmän monipuolisuutta, ja ne vaativat huomattavasti vähemmän kuin epäorgaaniset saadakseen saman vaikutuksen. Joten vain gramman miljoonasosa DDT-jauhetta neliösenttimetriä kohden pintaa tuhoaa täysin jotkin hyönteiset.

Orgaanisten torjunta-aineiden käytössä oli joitain kummallisuuksia. Heksakloraania pidetään tällä hetkellä yhtenä tehokkaista torjunta-aineista. Kuitenkin luultavasti harvat tietävät, että Faraday hankki tämän aineen ensimmäisen kerran vuonna 1825. Kemistit ovat tutkineet heksakloraania yli sadan vuoden ajan epäilemättä sen ihmeellisiä ominaisuuksia. Ja vasta vuoden 1935 jälkeen, kun biologit alkoivat tutkia sitä, tätä hyönteismyrkkyä alettiin tuottaa teollisessa mittakaavassa. Tällä hetkellä parhaita hyönteismyrkkyjä ovat organofosforiyhdisteet, kuten fosfamidi tai M-81.
Viime aikoihin asti kasvien ja eläinten suojelemiseen käytettiin ulkoisia valmisteita. Arvioi kuitenkin itse: satoi, tuuli puhalsi ja suojaava aineesi katosi. Kaikki on aloitettava alusta. Tiedemiehet miettivät kysymystä - onko mahdollista viedä torjunta-aineita suojattuun organismiin? He rokottavat ihmisen - eikä hän pelkää sairauksia. Heti kun mikrobit pääsevät sellaiseen organismiin, näkymättömät "terveydenhuoltajat", jotka ilmestyivät sinne seerumin lisäämisen seurauksena, tuhoavat ne välittömästi.
Kävi ilmi, että on täysin mahdollista luoda sisäisen toiminnan torjunta-aineita. Tutkijat ovat leikkineet tuhohyönteisten ja kasvien organismien erilaisella rakenteella. Kasveille tällainen torjunta-aine on vaaratonta, hyönteiselle se on tappava myrkky.
Kemia suojaa kasveja paitsi hyönteisiltä, myös rikkaruohoilta. On luotu ns. rikkakasvien torjunta-aineita, joilla on rikkakasveja masentava vaikutus ja jotka eivät käytännössä haittaa viljelykasvin kehitystä.
Ehkä yksi ensimmäisistä rikkakasvien torjunta-aineista, kummallista kyllä, olivat ... lannoitteet. Maatalouden harjoittajat ovat siis pitkään panneet merkille, että jos pelloille levitetään suurempia määriä superfosfaattia tai kaliumsulfaattia, viljeltyjen kasvien intensiivisen kasvun myötä rikkakasvien kasvu estyy. Mutta täällä, kuten hyönteismyrkkyjen tapauksessa, orgaanisilla yhdisteillä on ratkaiseva rooli aikanamme.
Maanviljelijän apulaiset
Poika on yli kuusitoista. Ja tässä hän on, ehkä ensimmäistä kertaa hajuvesiosastolla. Hän ei ole täällä uteliaisuudesta, vaan pakosta. Hänen viikset ovat jo alkaneet murtautua, ja ne on ajettava.
Aloittelijoille tämä on varsin mielenkiintoinen operaatio. Mutta noin kymmenen tai viidentoista vuoden kuluttua hän kyllästyy niin, että joskus tekee mieli kasvattaa parta.
Otetaan esimerkiksi ruoho. Se ei ole sallittua rautateillä. Ja ihmiset vuodesta toiseen "ajelevat" sen sirpeillä ja viikateillä. Mutta kuvittele rautatie Moskova - Habarovsk. Tämä on yhdeksäntuhatta kilometriä. Ja jos kaikki ruoho leikataan sen pituudelta ja useammin kuin kerran kesän aikana, lähes tuhat ihmistä on pidettävä tässä operaatiossa.
Onko mahdollista keksiä jonkinlainen kemiallinen tapa "ajella"? Osoittautuu, että voit.
Hehtaarin ruohon leikkaamiseen tarvitaan 20 ihmistä koko päivän. Rikkakasvien torjunta-aineet suorittavat "tappamisoperaation" samalla alueella muutamassa tunnissa. Ja tuhota ruoho kokonaan.
Tiedätkö mitä defoliantit ovat? "Folio" tarkoittaa "lehteä". Defoliantti on aine, joka saa ne putoamaan. Niiden käyttö mahdollisti puuvillan korjuun mekanisoinnin. Vuodesta vuoteen, vuosisadasta vuosisadalle ihmiset menivät pelloille poimimaan käsin puuvillapensaita. Jokainen, joka ei ole nähnyt manuaalista puuvillanpoimintaa, voi tuskin kuvitella koko taakkaa sellaisesta työstä, joka ennen kaikkea tapahtuu epätoivoisessa 40-50 asteen kuumuudessa.
Nyt kaikki on paljon helpompaa. Muutama päivä ennen puuvillapullien avaamista puuvillaviljelmät käsitellään lehtienpoistoaineilla. Yksinkertaisin niistä on Mg2. Lehdet putoavat pensaista, ja nyt puuvillankorjuukoneet työskentelevät pelloilla. Muuten, CaCN 2:ta voidaan käyttää defoliantina, mikä tarkoittaa, että kun pensaita käsitellään sillä, maaperään lisätään lisäksi typpilannoitetta.

Mutta maatalouden auttamisessa, luonnon "korjauksessa" kemia meni vielä pidemmälle. Kemistit löysivät niin sanotut auksiinit - kasvien kasvun kiihdyttimet. Totta, aluksi luonnollista. Yksinkertaisimpia niistä, kuten heteroauksiinin, kemistit ovat oppineet syntetisoimaan laboratorioissaan. Nämä aineet eivät vain nopeutta kasvien kasvua, kukintaa ja hedelmällisyyttä, vaan lisäävät niiden vakautta ja elinkelpoisuutta. Lisäksi kävi ilmi, että auksiinien käytöllä suurina pitoisuuksina on päinvastainen vaikutus - se estää kasvien kasvua ja kehitystä.
Lääkeaineiden kanssa on lähes täydellinen analogia. Siten arseenia, vismuttia ja elohopeaa sisältävät lääkkeet tunnetaan, mutta suurina (melko kohonneina) pitoisuuksina kaikki nämä aineet ovat myrkyllisiä.
Esimerkiksi auksiinit voivat pidentää huomattavasti koristekasvien ja ensisijaisesti kukkien kukinta-aikaa. Äkillisillä kevätpakkailla hidasta puiden silmujen puhkeamista ja kukintaa ja niin edelleen ja niin edelleen. Toisaalta kylmillä alueilla, joilla on lyhyet kesät, tämä mahdollistaa "nopealla" menetelmällä monien hedelmien ja vihannesten sadon. Ja vaikka näitä auksiinien kykyjä ei ole vielä toteutettu suuressa mittakaavassa, vaan ne ovat vain laboratoriokokeita, ei voi olla epäilystäkään siitä, että lähitulevaisuudessa viljelijöiden auttajat tulevat laajoille avoimille tiloille.
Aaveiden palveleminen
Tässä on tosiasia sanomalehtisensaatiolle: kiitolliset kollegat antavat kunnianarvoisalle tiedemiehelle ... alumiinimaljakon. Jokainen lahja ansaitsee kiitoksen. Mutta eikö olekin totta, antaa alumiinimaljakko... Siinä on jotain ironista...
Se on nyt. Sata vuotta sitten tällainen lahja olisi vaikuttanut poikkeuksellisen anteliaalta. Sen esittelivät todella englantilaiset kemistit. Eikä kenellekään, vaan itse Dmitri Ivanovitš Mendelejeville. Merkkinä suurista palveluista tieteelle.
Katso kuinka kaikki maailmassa on suhteellista. Viime vuosisadalla he eivät tienneet halpaa tapaa erottaa alumiinia malmeista, ja siksi metalli oli kallista. Löysimme tavan, ja hinnat putosivat nopeasti.
Monet jaksollisen järjestelmän elementit ovat edelleen kalliita. Ja tämä usein rajoittaa niiden käyttöä. Mutta olemme varmoja, toistaiseksi. Kemia ja fysiikka suorittavat useammin kuin kerran elementtien "hinnan alennuksen". He tekevät sen ehdottomasti, koska mitä pidemmälle, sitä enemmän jaksollisen järjestelmän asukkaita käytäntö sisältää toimintansa laajuudessa.
Mutta niiden joukossa on niitä, joita joko ei löydy maankuoresta tai niitä on järjettömän vähän, lähes olemattomia. Sanotaan, astatiini ja francium, neptunium ja plutonium, prometium ja teknetium…
Ne voidaan kuitenkin valmistaa keinotekoisesti. Ja heti kun kemisti pitää käsissään uutta elementtiä, hän alkaa miettiä: kuinka antaa hänelle aloitus elämässä?
Toistaiseksi tärkein keinotekoinen alkuaine käytännössä on plutonium. Ja sen maailmantuotanto ylittää nyt monien "tavallisten" jaksollisen järjestelmän elementtien talteenoton. Lisäämme vielä, että kemistit pitävät plutoniumia yhtenä tutkituimmista alkuaineista, vaikka se onkin hieman yli neljännesvuosisadan vanha. Kaikki tämä ei ole sattumaa, koska plutonium on erinomainen "polttoaine" ydinreaktoreille, ei millään tavalla huonompi kuin uraani.
Joillakin amerikkalaisilla maasatelliiteilla americium ja curium toimivat energialähteinä. Nämä alkuaineet ovat erittäin radioaktiivisia. Kun ne hajoavat, vapautuu paljon lämpöä. Termoparien avulla se muunnetaan sähköksi.
Entä prometium, jota ei ole vielä löydetty maanpäällisistä malmeista? Pienikokoiset paristot, jotka ovat hieman suuremmat kuin tavallisen neulan kansi, luodaan prometiumin avulla. Kemialliset akut kestävät parhaimmillaan enintään kuusi kuukautta. Promethium-atomiakku toimii yhtäjaksoisesti viisi vuotta. Ja sen käyttöalue on erittäin laaja: kuulokojeista ohjattuihin ammuksiin.
Astat on valmis tarjoamaan palvelujaan lääkäreille kilpirauhasen sairauksien torjumiseksi. He yrittävät nyt hoitaa sitä radioaktiivisen säteilyn avulla. Tiedetään, että jodia voi kertyä kilpirauhaseen, mutta astatiini on jodin kemiallinen analogi. Kehoon joutunut astatiini keskittyy kilpirauhaseen. Sitten sen radioaktiiviset ominaisuudet sanovat painavan sanan.
Joten jotkut keinotekoiset elementit eivät suinkaan ole tyhjä paikka harjoituksen tarpeille. Totta, ne palvelevat ihmistä yksipuolisesti. Ihmiset voivat käyttää vain radioaktiivisia ominaisuuksiaan. Kädet eivät ole vielä saavuttaneet kemiallisia ominaisuuksia. Poikkeuksena on teknetium. Tämän metallin suolat, kuten kävi ilmi, voivat tehdä teräs- ja rautatuotteista korroosionkestäviä.
Lähetä hyvä työsi tietokanta on yksinkertainen. Käytä alla olevaa lomaketta
Opiskelijat, jatko-opiskelijat, nuoret tutkijat, jotka käyttävät tietopohjaa opinnoissaan ja työssään, ovat sinulle erittäin kiitollisia.
Lähetetty http:// www. kaikkea parasta. fi
FSBEI HPE "Bashkir State University"
Skenaario koulun ulkopuolisesta tapahtumastakemiassa
"Kemia levittää kätensä ihmisasioissa..."
Tavoitteet:
1. Laajenna tietämystä kemiasta, herätä kiinnostusta tieteeseen.
2. Kehitä luovia kykyjä.
3. Kasvata kykyä työskennellä ryhmässä.
Jäsenet: 9. luokan oppilaat.
Suorituslomake: KVN.
Toimintajärjestys:
1. Kapteenien vala.
2. Lämmitä.
3. Kilpailu "Arvauspeli".
4. Kilpailu "D.I. Mendelejevin pöytä".
5. Kilpailu "Piirrä itse".
6. Kapteenien kilpailu.
7. Kilpailu "Kokeilijat".
8. Musiikkikilpailu.
9. Kilpailu "Tehtävä kirjekuoresta."
10. Kotitehtävät.
11. Yhteenveto.
Johtava:
Oi te onnelliset tieteet!
Ojenna käsiäsi ahkerasti
Ja katso kaukaisimmille paikoille
Ohita maa ja kuilu
Ja arot ja syvä metsä
Ja aivan taivaan korkeus.
Tutki kaikkialla koko ajan,
Mikä on hienoa ja kaunista
Mitä maailma ei ole koskaan nähnyt...
Maan suolistoihin sinä, kemia,
Läpäise silmä terävästi
Ja mitä Venäjä siihen sisältää
Avaa aarreaarteita.
M.V. Lomonosov.
Hyvää iltaa rakkaat ystävät. Kutsuimme sinut tänään todistamaan 9. luokan joukkueiden välistä kilpailua kekseliäisyydestä, iloisuudesta ja myös kemian tuntemisesta.
Kutsumme tiimin "Kemistit" (joukkueen esitys, tervehdys) Kutsumme joukkueen "Lyrics" (joukkueen esitys, tervehdys)
Johtava:
Ennen kilpailun alkua joukkueiden kapteenit vannovat valan.
Kapteenien vala.
Me, Chemists (Lyrics) -joukkueen kapteenit, olemme koonneet joukkueemme kemian kaksintaistelukentälle ja joukkueidemme, fanien, tuomariston ja viisaan kemian kirjan edessä vannomme juhlallisesti:
1) Ole rehellinen. opetuksen ulkopuolinen kemian koulutus luova
2) Älä kaada happoa toistensa päälle fyysisesti ja moraalisesti.
3) Älä käytä paini-, nyrkkeily- ja karatemenetelmiä kemiallisten tehtävien ratkaisemisessa.
4) Älä menetä huumorintajuasi illan loppuun asti.
Johtava:
Ja nyt treenit. Lämmittelyaihe: ”Ekologiset ongelmat ja kemia. Kuka on syyllinen?" Joukkueet valmistivat toisilleen 4 kysymystä.
Kemistit aloittavat ensin.
Kysymys kuuluu - 1 min. keskustelua varten.
Joukkueen vastaus.
Lyrika-tiimi esittää ensimmäisen kysymyksensä.
(jne. 4 kysymystä varten).
Johtava:
Jatketaan kilpailuihin.
1. "Arvauspeli".
Julkaisemme koulun sisällä poistumiskilpailun. Kutsumme 2 henkilöä. Tehtävä: "Mene sinne, en tiedä minne, tuo jotain, en tiedä mitä." (Aika 25 min).
2. "Taulukko D.I. Mendelejev".
Toinen kilpailu edellyttää jaksollisen järjestelmän tuntemista. Valitse ja kirjoita merkkien kaaoksesta kemiallisia alkuaineita ja nimeä ne. Luovuta kortit tuomaristolle.
3. "Piirrä itsesi."
Kolmas kilpailu kutsuu ne, jotka osaavat piirtää. Piirrä sidottu silmät, mitä esittäjä lukee. (1 minuutti.).
Kemiahuoneessa taulun vieressä on pöytä, pöydällä on pullo, pullosta tulee ruskeaa kaasua.
Ovat piirtäneet. Millainen kaasu mahtaa olla? (NO2).
Tuomariston sana.
Johtava:
Kapteenien kilpailu. (Kutsu lavalle, tarjoudu istumaan, anna paperi ja kynä).
Kuuntelet tarinan, jossa kemialliset alkuaineet tai kemikaalit nimetään. Kirjoita ne muistiin kemiallisilla symboleilla.
Kemian tarina.
Se oli Euroopassa ja ehkä Amerikassa. Istuimme Bohrin ja Berkeleyn kanssa Fermiassa. Sat ja Kali. Sanon: "Lopeta hapen pilaaminen, ja niin on rikki sielussani. Mennään Rubidiumiin." Ja Berkel: "Olen siis Galliasta yksin. Enkä anna sinulle kahta Rubidiumia. Miksi minun pitäisi ylipäätään jättää Fermius?" Tässä olen, kuten Actiny itse, ja sanon: "Platina, ja siinä se!" Lopuksi Palladium. He alkoivat miettiä, kenen pitäisi mennä Bariyyn. Berkeley ja sanoo: "Olen täysin rampa." Sitten Bor Plumbum tuli meille, kauhisi Rubidiamme arseenin alta ja lähti. Olemme Radius. Me istumme Curiumissa ja odotamme Boria. Yhtäkkiä kuulemme: "Aurum, Aurum!". Sanon: "Ei Bor!" Ja Berkeley: "Ei, Neon!" Ja hän itse on ovela, seisoo Galliumin kanssa, kädellä Thaliaa ja litiumia hänelle, jotain Franciuksesta. Vanha plutonium. Ja tässä taas: "Aurum, Aurum!" Katsomme, Boori juoksee, ja hänen takanaan on naapuri Koboltti, Argon ja Hafnium hänen päällänsä ja hänen Terbium Arseenin takana, missä Rubidiumimme sijaitsevat. Borista tuli kokonaan Lutetsky. Huutaa, heiluttaa käsiään. Yhtäkkiä katsomme, ja Rubidiumissamme on argonia elohopeassa. Tässä Berkeley petti meidät. Hän seisoo nelijalkain, ja hän itse on sellainen Strontski, Strontski ja sanoo: "Argonchik, kerro Hafniukselle." Argon on hiljaa ja vain Cesium hänen hampaidensa läpi "Rrr". Sitten myös Berkliy, Lyutetsky nousi seisomaan ja ikään kuin huusi: "Mene ulos", Argon juoksi karkuun. Ja Berkelium sanoo Borulle: "Anna minulle Rubidium." A bor: "Ei beryllium, minä olen sinun Rubidium. Mitä, olenko minä heidän rodiuminsa vai mitä? Astane minua rauhassa. Ja Berkel hänelle: "Jos näen sinut taas Fermiassa, natrium on korvasi."
Kapteenit luovuttavat esitteitä, joissa on kirjoitettuja merkkejä tarinassa nimetyistä kemiallisista alkuaineista.
4. 4. kilpailu "Kokeilijat" Kutsu 2 henkilöä joukkueesta. Tuomaristosta 1 edustaja tarkkailuun.
Kokemus: "Seosten erottelu"
a) hiekka- ja rautaviilat
a) puu- ja rautaviilat
b) hiekka ja sokeri
b) suolaa ja savea
Kokemus: "Tunnista aineet"
a) KOH, H2SO4, KCl
a) NaOH, Ba(OH)2, H2SO4
Kokemus: "Hanki seuraavat aineet"
Yhteenveto kapteenien kilpailusta.
Tuomariston sana.
5. Musiikkikilpailu. Ryhmät saivat valmistaa laulun ja tanssin kemiallisesta teemasta.
Yhteenveto "Kokeilijat" -kilpailun tuloksista.
6. Kilpailu "Tehtävä kirjekuoresta."
1) Millaista maitoa ei juo?
2) Mikä alkuaine on elottoman luonnon perusta?
3) Mihin veteen kulta liukenee?
4) Mistä elementistä yksinkertaisen aineen muodossa he joko maksavat enemmän kuin kullasta tai päinvastoin, maksavat päästäkseen siitä eroon?
5) Mikä on Neuvostoliiton kemistien tieteellisen seuran nimi?
6) Mitä allotropia on? Antaa esimerkkejä.
Johtava:
Kuuntelemme poistumiskilpailun osallistujia.
Kotitehtäviin valmistautuminen.
Tällä hetkellä tuomaristo tekee yhteenvedon viimeisimmistä kilpailuista.
Jos joukkueet eivät ole vielä valmiita, faneille esitetään kysymyksiä. Jokaisesta oikeasta vastauksesta fanille annetaan ympyrä ja joukkue saa 1 pisteen.
1. Onko metallia, joka sulaa kädessä?
2. Mikä on jäähappo?
3. Mikä on valkokulta?
4. Millainen alkoholi ei pala?
Johtava:
Kotitehtävät esittelee Chemists-tiimi (lyrics)
Aihe: "Kemiatunti viime vuosisadalla."
Yhteenveto.
Osallistujien palkinnot.
Kirjallisuus:
1. Blokhina O.G. Menen kemian tunnille: Opettajan kirja. - M .: Kustantaja "Syyskuun ensimmäinen", 2001.
2. Bocharova S.I. Kemian opetuksen ulkopuolinen työ. Luokat 8-9 - Volgograd: ITD "Corifey", 2006
3. Kurgansky S.M. Kemian opetuksen ulkopuoliset työt: Tietokilpailut ja kemian illat - M .: 5 tiedoksi, 2006.
4. CER kemiassa, levy luokalle 9. 1C Koulutus 4. koulu: ZAO 1C, 2006
Isännöi Allbest.ru:ssa
...Samanlaisia asiakirjoja
Kirjallisuuden ja kemian välisen suhteen tutkiminen taideteosten esimerkillä, kirjallisuuden kemialliset virheet. Metallien taiteellisia kuvia Lermontovin sanoituksissa. Taideteosten vaikutuksen analyysi opiskelijoiden kognitiiviseen kiinnostukseen kemiaa kohtaan.
opinnäytetyö, lisätty 23.9.2014
Tutkimustyö mahdollistaa opiskelijoiden kognitiivisen toiminnan, luovuuden kehittämisen, auttaa synnyttämään kiinnostusta tieteelliseen tietoon, kehittää ajattelua. Tutkimustyötä voidaan tehdä kouluajan ulkopuolella.
artikkeli, lisätty 03.03.2008
Opiskelijoiden kemian opiskelumotivaation muodostumisen riippuvuus pedagogisen prosessin organisoinnin pedagogisista edellytyksistä. Merkittävimmät pedagogiset olosuhteet, jotka määräävät kemian opiskelumotivaation yhdeksännen esiprofiilin opiskelijoiden keskuudessa.
opinnäytetyö, lisätty 13.4.2009
Epätavallinen kemian määritelmä. Herättää kiinnostusta aineen oppimiseen. Initiaatioiden tekeminen kemistiksi ehdokkaiden ammatillisen soveltuvuuden testaamiseksi aineiden välisten muunnosten toteuttamiseen. Kemia arvoituksina, arvoituksina ja kokeissa.
esitys, lisätty 20.3.2011
Yleisen itsemääräämisvalmiuden muodostuminen, ammatinvalintaongelman aktivointi; laajentaa opiskelijoiden tietämystä eri ammateista, herättää kiinnostusta ammatteja kohtaan. Kokoaminen ja menettely pro-testin suorittamiseksi seitsemännen luokan oppilaiden kesken.
oppitunnin kehitys, lisätty 25.8.2011
Kuka on opettaja ja mikä on hänen tehtävänsä opiskelijan elämässä. Opettajan kyky kasvattaa opiskelijoita itsenäisyyteen, kyky elää ja selviytyä maailmassa, kyky ottaa yhteyttä ihmisiin, kehittää taitoja ja kykyjä, ohjata heitä oikealle tielle.
essee, lisätty 19.1.2014
Opiskelijoiden tiedon hallinnan käsite ja lajikkeet, käytännön tehokkuuden arviointi. Temaattisen ohjauksen organisointitavat, opetusprosessin tehokkuuden varmistaminen, niiden toteuttamismenetelmät ja toteutuksen erityispiirteet koulun kemian tunneilla.
opinnäytetyö, lisätty 15.6.2010
Kognitiivinen, opettavainen, kehittävä ja kouluttava oppitunnin ulkopuolisen toiminnan tavoitteita, sen laitteita ja pelin "Hangman" sääntöjä. Kasvatustoiminnan psykologinen analyysi, opiskelijoiden arvoasenteiden muodostuminen historiaa ja yhteiskuntaa kohtaan.
käytännön työ, lisätty 19.1.2010
Koulutustapahtuman aiheen muodon valinnan perustelut. Ennen tapahtumaa tehty työ. Koulutussuunnitelma. Koulutustapahtuman kulku (skenaario). Yhteenveto ja voittajan selvittäminen.
harjoitusraportti, lisätty 17.4.2007
Tieteellisen kirjallisuuden analyysi koulun ulkopuolisen lukemisen metodologiasta. Lukemisen valmistelu ja suorittaminen kirjallisuuden tunneilla. Luokan ulkopuolisen lukemisen tuntisuunnitelman laatiminen B. Akhmadulinan runon "Sateen tarina" perusteella 7-8-luokkien oppilaille.