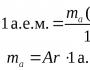ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಸೂತ್ರಗಳ ಸಂಗ್ರಹ. ಸಮಸ್ಯೆಗಳನ್ನು ಪರಿಹರಿಸಲು ಮೂಲ ಸೂತ್ರಗಳು
|
ಪರಿಮಾಣ ಮತ್ತು ಅದರ ಆಯಾಮ |
ಅನುಪಾತ |
|
ಅಂಶ X ನ ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿ (ಸಂಬಂಧಿ) |
|
|
ಅಂಶದ ಸರಣಿ ಸಂಖ್ಯೆ |
Z= ಎನ್(ಇ –) = ಎನ್(ಆರ್ +) |
|
X ವಸ್ತುವಿನಲ್ಲಿ ಅಂಶ E ಯ ದ್ರವ್ಯರಾಶಿ ಭಾಗ, ಒಂದು ಘಟಕದ ಭಿನ್ನರಾಶಿಗಳಲ್ಲಿ, % ನಲ್ಲಿ) |
|
|
ವಸ್ತುವಿನ ಪ್ರಮಾಣ X, mol | |
|
ಅನಿಲ ವಸ್ತುವಿನ ಪ್ರಮಾಣ, ಮೋಲ್ |
ಸರಿ. ಆರ್– = 101 325 Pa,ಟಿ |
|
= 273 ಕೆ |
|
|
ವಸ್ತುವಿನ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿ X, g/mol, kg/mol |
ಮೀವಸ್ತುವಿನ ದ್ರವ್ಯರಾಶಿ X, g, kg (X) =ಎನ್ (X)ಎಂ |
|
(X) |
ವಿ ಮೀಅನಿಲದ ಮೋಲಾರ್ ಪರಿಮಾಣ, l/mol, m 3 /mol |
|
N.S ನಲ್ಲಿ = 22.4 l/mol |
ವಿ = ವಿ ಮೀ × (X) = |
|
ಅನಿಲ ಪರಿಮಾಣ, ಮೀ 3 |
|
|
ಉತ್ಪನ್ನ ಇಳುವರಿ |
|
|
ವಸ್ತುವಿನ ಸಾಂದ್ರತೆ X, g/l, g/ml, kg/m3 |
|
|
ಹೈಡ್ರೋಜನ್ ಮೂಲಕ X ಅನಿಲ ಪದಾರ್ಥದ ಸಾಂದ್ರತೆ |
ಗಾಳಿಯಲ್ಲಿ X ಅನಿಲ ಪದಾರ್ಥದ ಸಾಂದ್ರತೆಎಂ |
|
(ಗಾಳಿ) = 29 g/mol |
|
|
ಯುನೈಟೆಡ್ ಗ್ಯಾಸ್ ಕಾನೂನು |
ಮೆಂಡಲೀವ್-ಕ್ಲಾಪಿರಾನ್ ಸಮೀಕರಣ = ಪಿ.ವಿ, nRTಆರ್ |
|
= 8.314 J/mol×K |
|
|
ಅನಿಲಗಳ ಮಿಶ್ರಣದಲ್ಲಿ, ಒಂದು ಘಟಕದ ಭಿನ್ನರಾಶಿಗಳಲ್ಲಿ ಅಥವಾ % ನಲ್ಲಿ ಅನಿಲ ಪದಾರ್ಥದ ಪರಿಮಾಣದ ಭಾಗ |
|
|
ಅನಿಲಗಳ ಮಿಶ್ರಣದ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿ |
|
|
ಮಿಶ್ರಣದಲ್ಲಿರುವ ವಸ್ತುವಿನ (X) ಮೋಲ್ ಭಾಗ |
ಶಾಖದ ಪ್ರಮಾಣ, ಜೆ, ಕೆಜೆ = (X) =ಎನ್ ಶಾಖದ ಪ್ರಮಾಣ, ಜೆ, ಕೆಜೆಎಂ |
|
ಪ್ರ |
ಪ್ರತಿಕ್ರಿಯೆಯ ಉಷ್ಣ ಪರಿಣಾಮಪ್ರಶ್ನೆ =- |
|
ಎಚ್ |
|
|
X, J/mol, kJ/mol ವಸ್ತುವಿನ ರಚನೆಯ ಶಾಖ |
|
|
ರಾಸಾಯನಿಕ ಪ್ರತಿಕ್ರಿಯೆ ದರ (mol/lsec) ಸಾಮೂಹಿಕ ಕ್ರಿಯೆಯ ಕಾನೂನು |
(ಸರಳ ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ)ಎ A+ವಿ ಬಿ=ಜೊತೆಗೆ ಸಿ +ಡಿ ಡಿ = ಯು ಬಿ= (ಸರಳ ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ)ಕೆ ಬಿ= (ಎ)ವಿ |
|
(ಬಿ) |
|
|
ವ್ಯಾಂಟ್ ಹಾಫ್ ಅವರ ನಿಯಮ |
|
|
ವಸ್ತುವಿನ ಕರಗುವಿಕೆ (X) (g/100 g ದ್ರಾವಕ) |
|
|
A + X ಮಿಶ್ರಣದಲ್ಲಿ X ಪದಾರ್ಥದ ದ್ರವ್ಯರಾಶಿ, ಒಂದು ಘಟಕದ ಭಿನ್ನರಾಶಿಗಳಲ್ಲಿ, % |
ಮೀದ್ರಾವಣದ ತೂಕ, ಗ್ರಾಂ, ಕೆಜಿ ಮೀ(ಆರ್ಆರ್) = ಮೀ(X)+ ಮೀದ್ರಾವಣದ ತೂಕ, ಗ್ರಾಂ, ಕೆಜಿ ವಿ(H2O) (ಆರ್ಆರ್) |
|
(ಆರ್ಆರ್) |
|
|
ದ್ರಾವಣದಲ್ಲಿ ಕರಗಿದ ವಸ್ತುವಿನ ದ್ರವ್ಯರಾಶಿ, ಘಟಕದ ಭಿನ್ನರಾಶಿಗಳಲ್ಲಿ,% |
|
|
ಪರಿಹಾರ ಸಾಂದ್ರತೆ |
|
|
ದ್ರಾವಣದ ಪರಿಮಾಣ, cm 3, l, m 3 |
|
|
ಮೋಲಾರ್ ಸಾಂದ್ರತೆ, mol/l |
|
|
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆಯ ಪದವಿ (X), ಒಂದು ಘಟಕದ ಭಿನ್ನರಾಶಿಗಳಲ್ಲಿ ಅಥವಾ% |
ನೀರಿನ ಅಯಾನಿಕ್ ಉತ್ಪನ್ನಕೆ |
|
(H2O) = |
pH ಮೌಲ್ಯ |
pH = -lg
ಮುಖ್ಯ:ಕುಜ್ನೆಟ್ಸೊವಾ ಎನ್.ಇ. ಮತ್ತು ಇತ್ಯಾದಿ
. ರಸಾಯನಶಾಸ್ತ್ರ. 8 ನೇ ಗ್ರೇಡ್-10 ನೇ ಗ್ರೇಡ್ - ಎಂ.: ವೆಂಟಾನಾ-ಗ್ರಾಫ್, 2005-2007.ಕುಜ್ನೆಟ್ಸೊವಾ ಎನ್.ಇ., ಲಿಟ್ವಿನೋವಾ ಟಿ.ಎನ್., ಲೆವ್ಕಿನ್ ಎ.ಎನ್.
ರಸಾಯನಶಾಸ್ತ್ರ. 2 ಭಾಗಗಳಲ್ಲಿ 11 ನೇ ತರಗತಿ, 2005-2007.ಎಗೊರೊವ್ ಎ.ಎಸ್.
ರಸಾಯನಶಾಸ್ತ್ರ. ಉನ್ನತ ಶಿಕ್ಷಣಕ್ಕಾಗಿ ತಯಾರಿಗಾಗಿ ಹೊಸ ಪಠ್ಯಪುಸ್ತಕ. ರೋಸ್ಟೊವ್ ಎನ್/ಡಿ: ಫೀನಿಕ್ಸ್, 2004.– 640 ಪು.
ರಸಾಯನಶಾಸ್ತ್ರ. 2 ಭಾಗಗಳಲ್ಲಿ 11 ನೇ ತರಗತಿ, 2005-2007.ಎಗೊರೊವ್ ಎ.ಎಸ್. ರಸಾಯನಶಾಸ್ತ್ರ: ಏಕೀಕೃತ ರಾಜ್ಯ ಪರೀಕ್ಷೆಗೆ ತಯಾರಿ ಮಾಡುವ ಆಧುನಿಕ ಕೋರ್ಸ್. ರೋಸ್ಟೊವ್ ಎನ್ / ಎ: ಫೀನಿಕ್ಸ್, 2011. (2012) - 699 ಪು.
ರಾಸಾಯನಿಕ ಸಮಸ್ಯೆಗಳನ್ನು ಪರಿಹರಿಸಲು ಸ್ವಯಂ ಸೂಚನಾ ಕೈಪಿಡಿ. - ರೋಸ್ಟೊವ್-ಆನ್-ಡಾನ್: ಫೀನಿಕ್ಸ್, 2000. - 352 ಪು.
ವಿಶ್ವವಿದ್ಯಾಲಯಗಳಿಗೆ ಅರ್ಜಿದಾರರಿಗೆ ರಸಾಯನಶಾಸ್ತ್ರ/ಬೋಧಕ ಕೈಪಿಡಿ. ರೋಸ್ಟೊವ್-ಎನ್/ಡಿ, ಫೀನಿಕ್ಸ್, 2005– 536 ಪು.ಖೊಮ್ಚೆಂಕೊ ಜಿ.ಪಿ., ಖೊಮ್ಚೆಂಕೊ ಐ.ಜಿ.
. ವಿಶ್ವವಿದ್ಯಾಲಯಗಳಿಗೆ ಅರ್ಜಿದಾರರಿಗೆ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿನ ಸಮಸ್ಯೆಗಳು. ಎಂ.: ಹೈಯರ್ ಸ್ಕೂಲ್. 2007.–302 ಪು.
ಹೆಚ್ಚುವರಿ:. ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಕೇಂದ್ರೀಕೃತ ಪರೀಕ್ಷೆಗೆ ತಯಾರಿಗಾಗಿ ಶೈಕ್ಷಣಿಕ ಮತ್ತು ತರಬೇತಿ ಸಾಮಗ್ರಿಗಳು / A.I. ವ್ರುಬ್ಲೆವ್ಸ್ಕಿ -Mn.: ಯುನಿಪ್ರೆಸ್ LLC, 2004. - 368 ಪು.
ಹೆಚ್ಚುವರಿ:. ಶಾಲಾ ಮಕ್ಕಳು ಮತ್ತು ಅರ್ಜಿದಾರರಿಗೆ ರೂಪಾಂತರಗಳು ಮತ್ತು ನಿಯಂತ್ರಣ ಪರೀಕ್ಷೆಗಳೊಂದಿಗೆ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ 1000 ಸಮಸ್ಯೆಗಳು - Mn.: Unipress LLC, 2003. - 400 p.
ಎಗೊರೊವ್ ಎ.ಎಸ್.. ಏಕೀಕೃತ ರಾಜ್ಯ ಪರೀಕ್ಷೆಗೆ ತಯಾರಿಗಾಗಿ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಎಲ್ಲಾ ರೀತಿಯ ಲೆಕ್ಕಾಚಾರದ ಸಮಸ್ಯೆಗಳು - ರೋಸ್ಟೊವ್ ಎನ್ / ಡಿ: ಫೀನಿಕ್ಸ್, 2003. - 320 ಪು.
ಎಗೊರೊವ್ A.S., ಅಮಿನೋವಾ G.Kh.. ರಸಾಯನಶಾಸ್ತ್ರ ಪರೀಕ್ಷೆಗೆ ತಯಾರಿಗಾಗಿ ವಿಶಿಷ್ಟ ಕಾರ್ಯಗಳು ಮತ್ತು ವ್ಯಾಯಾಮಗಳು. - ರೋಸ್ಟೊವ್ ಎನ್ / ಡಿ: ಫೀನಿಕ್ಸ್, 2005. - 448 ಪು.
ಏಕೀಕೃತ ರಾಜ್ಯ ಪರೀಕ್ಷೆ 2007. ರಸಾಯನಶಾಸ್ತ್ರ. ವಿದ್ಯಾರ್ಥಿಗಳನ್ನು ಸಿದ್ಧಪಡಿಸಲು ಶೈಕ್ಷಣಿಕ ಮತ್ತು ತರಬೇತಿ ಸಾಮಗ್ರಿಗಳು / FIPI - M.: ಇಂಟೆಲೆಕ್ಟ್-ಸೆಂಟರ್, 2007. – 272 ಪು.
ಏಕೀಕೃತ ರಾಜ್ಯ ಪರೀಕ್ಷೆ 2011. ರಸಾಯನಶಾಸ್ತ್ರ. ಶೈಕ್ಷಣಿಕ ಮತ್ತು ತರಬೇತಿ ಕಿಟ್ ಆವೃತ್ತಿ. ಎ.ಎ. ಕಾವೇರಿನಾ - ಎಂ.: ರಾಷ್ಟ್ರೀಯ ಶಿಕ್ಷಣ, 2011.
ಏಕೀಕೃತ ರಾಜ್ಯ ಪರೀಕ್ಷೆಗೆ ತಯಾರಾಗಲು ಕಾರ್ಯಗಳಿಗಾಗಿ ಮಾತ್ರ ನಿಜವಾದ ಆಯ್ಕೆಗಳು. ಏಕೀಕೃತ ರಾಜ್ಯ ಪರೀಕ್ಷೆ 2007. ರಸಾಯನಶಾಸ್ತ್ರ/ವಿ.ಯು. ಮಿಶಿನಾ, ಇ.ಎನ್. ಸ್ಟ್ರೆಲ್ನಿಕೋವಾ. ಎಂ.: ಫೆಡರಲ್ ಟೆಸ್ಟಿಂಗ್ ಸೆಂಟರ್, 2007.–151 ಪು.
ಕಾವೇರಿನಾ ಎ.ಎ. ವಿದ್ಯಾರ್ಥಿಗಳನ್ನು ಸಿದ್ಧಪಡಿಸಲು ಕಾರ್ಯಗಳ ಅತ್ಯುತ್ತಮ ಬ್ಯಾಂಕ್. ಏಕೀಕೃತ ರಾಜ್ಯ ಪರೀಕ್ಷೆ 2012. ರಸಾಯನಶಾಸ್ತ್ರ. ಪಠ್ಯಪುಸ್ತಕ./ ಎ.ಎ. ಕಾವೇರಿನಾ, ಡಿ.ಯು. ಡೊಬ್ರೊಟಿನ್, ಯು.ಎನ್. ಮೆಡ್ವೆಡೆವ್, ಎಂ.ಜಿ. ಸ್ನಾಸ್ಟಿನಾ - ಎಂ.: ಇಂಟೆಲೆಕ್ಟ್-ಸೆಂಟರ್, 2012. - 256 ಪು.
ಲಿಟ್ವಿನೋವಾ ಟಿ.ಎನ್., ವೈಸ್ಕುಬೊವಾ ಎನ್.ಕೆ., ಅಜಿಪಾ ಎಲ್.ಟಿ., ಸೊಲೊವಿಯೋವಾ ಎಂ.ವಿ.. 10 ತಿಂಗಳ ಪತ್ರವ್ಯವಹಾರದ ಪೂರ್ವಸಿದ್ಧತಾ ಕೋರ್ಸ್ಗಳ ವಿದ್ಯಾರ್ಥಿಗಳಿಗೆ ಪರೀಕ್ಷೆಗಳಿಗೆ ಹೆಚ್ಚುವರಿಯಾಗಿ ಪರೀಕ್ಷಾ ಕಾರ್ಯಗಳು (ವಿಧಾನಶಾಸ್ತ್ರದ ಸೂಚನೆಗಳು). ಕ್ರಾಸ್ನೋಡರ್, 2004. - P. 18 - 70.
ಲಿಟ್ವಿನೋವಾ ಟಿ.ಎನ್.. ರಸಾಯನಶಾಸ್ತ್ರ. ಏಕೀಕೃತ ರಾಜ್ಯ ಪರೀಕ್ಷೆ 2011. ತರಬೇತಿ ಪರೀಕ್ಷೆಗಳು. ರೋಸ್ಟೊವ್ ಎನ್/ಡಿ: ಫೀನಿಕ್ಸ್, 2011.– 349 ಪು.
ಲಿಟ್ವಿನೋವಾ ಟಿ.ಎನ್.. ರಸಾಯನಶಾಸ್ತ್ರ. ಏಕೀಕೃತ ರಾಜ್ಯ ಪರೀಕ್ಷೆಗಾಗಿ ಪರೀಕ್ಷೆಗಳು. ರೋಸ್ಟೊವ್ ಎನ್ / ಡಿ.: ಫೀನಿಕ್ಸ್, 2012. - 284 ಪು.
ಲಿಟ್ವಿನೋವಾ ಟಿ.ಎನ್.. ರಸಾಯನಶಾಸ್ತ್ರ. ನಿಯಮಗಳು, ಅಂಶಗಳ ಗುಣಲಕ್ಷಣಗಳು ಮತ್ತು ಅವುಗಳ ಸಂಯುಕ್ತಗಳು. ರೋಸ್ಟೊವ್ ಎನ್ / ಡಿ.: ಫೀನಿಕ್ಸ್, 2012. - 156 ಪು.
ಲಿಟ್ವಿನೋವಾ ಟಿ.ಎನ್., ಮೆಲ್ನಿಕೋವಾ ಇ.ಡಿ., ಸೊಲೊವಿಯೋವಾ ಎಂ.ವಿ.., ಅಜಿಪಾ ಎಲ್.ಟಿ., ವೈಸ್ಕುಬೊವಾ ಎನ್.ಕೆ.ವಿಶ್ವವಿದ್ಯಾನಿಲಯಗಳಿಗೆ ಅರ್ಜಿದಾರರಿಗೆ ಕಾರ್ಯಗಳಲ್ಲಿ ರಸಾಯನಶಾಸ್ತ್ರ - M.: ಓನಿಕ್ಸ್ ಪಬ್ಲಿಷಿಂಗ್ ಹೌಸ್ LLC: ಮಿರ್ ಮತ್ತು ಶಿಕ್ಷಣ ಪಬ್ಲಿಷಿಂಗ್ ಹೌಸ್ LLC, 2009. - 832 ಪು.
ವೈದ್ಯಕೀಯ ಮತ್ತು ಜೈವಿಕ ತರಗತಿಗಳ ವಿದ್ಯಾರ್ಥಿಗಳಿಗೆ ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಶೈಕ್ಷಣಿಕ ಮತ್ತು ಕ್ರಮಶಾಸ್ತ್ರೀಯ ಸಂಕೀರ್ಣ, ಸಂ. ಟಿ.ಎನ್. ಲಿಟ್ವಿನೋವಾ - ಕ್ರಾಸ್ನೋಡರ್.: KSMU, - 2008.
ರಸಾಯನಶಾಸ್ತ್ರ. ಏಕೀಕೃತ ರಾಜ್ಯ ಪರೀಕ್ಷೆ 2008. ಪ್ರವೇಶ ಪರೀಕ್ಷೆಗಳು, ಬೋಧನಾ ನೆರವು / ಸಂ. ವಿ.ಎನ್. ಡೊರೊಂಕಿನಾ. – ರೋಸ್ಟೊವ್ ಎನ್/ಎ: ಲೀಜನ್, 2008.– 271 ಪು.
ರಸಾಯನಶಾಸ್ತ್ರದ ವೆಬ್ಸೈಟ್ಗಳ ಪಟ್ಟಿ:
1. ಅಲ್ಹಿಮಿಕ್. http:// www. ಅಲ್ಹಿಮಿಕ್. ರು
2. ಎಲ್ಲರಿಗೂ ರಸಾಯನಶಾಸ್ತ್ರ. ಸಂಪೂರ್ಣ ರಸಾಯನಶಾಸ್ತ್ರ ಕೋರ್ಸ್ಗಾಗಿ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಉಲ್ಲೇಖ ಪುಸ್ತಕ.
http:// www. ಮಾಹಿತಿಯುಕ್ತ. ರು/ ಪಠ್ಯ/ ಡೇಟಾಬೇಸ್/ ರಸಾಯನಶಾಸ್ತ್ರ/ ಪ್ರಾರಂಭಿಸಿ. html
3. ಶಾಲಾ ರಸಾಯನಶಾಸ್ತ್ರ - ಉಲ್ಲೇಖ ಪುಸ್ತಕ. http:// www. ಶಾಲಾ ರಸಾಯನಶಾಸ್ತ್ರ. ಮೂಲಕ. ರು
4. ರಸಾಯನಶಾಸ್ತ್ರ ಬೋಧಕ. http://www. chemistry.nm.ru
ಇಂಟರ್ನೆಟ್ ಸಂಪನ್ಮೂಲಗಳು
ಅಲ್ಹಿಮಿಕ್. http:// www. ಅಲ್ಹಿಮಿಕ್. ರು
ಎಲ್ಲರಿಗೂ ರಸಾಯನಶಾಸ್ತ್ರ. ಸಂಪೂರ್ಣ ರಸಾಯನಶಾಸ್ತ್ರ ಕೋರ್ಸ್ಗಾಗಿ ಎಲೆಕ್ಟ್ರಾನಿಕ್ ಉಲ್ಲೇಖ ಪುಸ್ತಕ.
http:// www. ಮಾಹಿತಿಯುಕ್ತ. ರು/ ಪಠ್ಯ/ ಡೇಟಾಬೇಸ್/ ರಸಾಯನಶಾಸ್ತ್ರ/ ಪ್ರಾರಂಭಿಸಿ. html
ಶಾಲಾ ರಸಾಯನಶಾಸ್ತ್ರ - ಉಲ್ಲೇಖ ಪುಸ್ತಕ. http:// www. ಶಾಲಾ ರಸಾಯನಶಾಸ್ತ್ರ. ಮೂಲಕ. ರು
http://www.classchem.narod.ru
ರಸಾಯನಶಾಸ್ತ್ರ ಬೋಧಕ. http://www. chemistry.nm.ru
http://www.alleng.ru/edu/chem.htm- ರಸಾಯನಶಾಸ್ತ್ರದ ಶೈಕ್ಷಣಿಕ ಇಂಟರ್ನೆಟ್ ಸಂಪನ್ಮೂಲಗಳು
http://schoolchemistry.by.ru/- ಶಾಲಾ ರಸಾಯನಶಾಸ್ತ್ರ. ಈ ಸೈಟ್ ವಿವಿಧ ವಿಷಯಗಳ ಮೇಲೆ ಆನ್ಲೈನ್ ಪರೀಕ್ಷೆಯನ್ನು ತೆಗೆದುಕೊಳ್ಳಲು ಅವಕಾಶವನ್ನು ಹೊಂದಿದೆ, ಜೊತೆಗೆ ಏಕೀಕೃತ ರಾಜ್ಯ ಪರೀಕ್ಷೆಯ ಡೆಮೊ ಆವೃತ್ತಿಗಳನ್ನು ಹೊಂದಿದೆ
ರಸಾಯನಶಾಸ್ತ್ರ ಮತ್ತು ಜೀವನ-XXI ಶತಮಾನ: ಜನಪ್ರಿಯ ವಿಜ್ಞಾನ ಪತ್ರಿಕೆ. http:// www. ಹೈಜ್. ರು
ಶಾಲಾ ರಸಾಯನಶಾಸ್ತ್ರ ಕೋರ್ಸ್ಗೆ ಮೂಲ ಸೂತ್ರಗಳ ಸಂಗ್ರಹ
ಶಾಲಾ ರಸಾಯನಶಾಸ್ತ್ರ ಕೋರ್ಸ್ಗೆ ಮೂಲ ಸೂತ್ರಗಳ ಸಂಗ್ರಹ
ಜಿಪಿ ಲಾಗಿನೋವಾ
ಎಲೆನಾ ಸವಿಂಕಿನಾ
E. V. ಸವಿಂಕಿನಾ G. P. ಲಾಗಿನೋವಾ
ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಮೂಲ ಸೂತ್ರಗಳ ಸಂಗ್ರಹ
ವಿದ್ಯಾರ್ಥಿಗಳ ಪಾಕೆಟ್ ಗೈಡ್
ಸಾಮಾನ್ಯ ರಸಾಯನಶಾಸ್ತ್ರ
ಪ್ರಮುಖ ರಾಸಾಯನಿಕ ಪರಿಕಲ್ಪನೆಗಳು ಮತ್ತು ಕಾನೂನುಗಳು
ರಾಸಾಯನಿಕ ಅಂಶ- ಇದು ಅದೇ ಪರಮಾಣು ಚಾರ್ಜ್ ಹೊಂದಿರುವ ನಿರ್ದಿಷ್ಟ ರೀತಿಯ ಪರಮಾಣು.
ಸಾಪೇಕ್ಷ ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿ(A r) ಕೊಟ್ಟಿರುವ ರಾಸಾಯನಿಕ ಅಂಶದ ಪರಮಾಣುವಿನ ದ್ರವ್ಯರಾಶಿಯು ಕಾರ್ಬನ್-12 ಪರಮಾಣುವಿನ (12 C) ದ್ರವ್ಯರಾಶಿಗಿಂತ ಎಷ್ಟು ಪಟ್ಟು ಹೆಚ್ಚಾಗಿದೆ ಎಂಬುದನ್ನು ತೋರಿಸುತ್ತದೆ.
ರಾಸಾಯನಿಕ ವಸ್ತು- ಯಾವುದೇ ರಾಸಾಯನಿಕ ಕಣಗಳ ಸಂಗ್ರಹ.
ರಾಸಾಯನಿಕ ಕಣಗಳು
ಫಾರ್ಮುಲಾ ಘಟಕ- ಒಂದು ಸಾಂಪ್ರದಾಯಿಕ ಕಣ, ಅದರ ಸಂಯೋಜನೆಯು ನಿರ್ದಿಷ್ಟ ರಾಸಾಯನಿಕ ಸೂತ್ರಕ್ಕೆ ಅನುರೂಪವಾಗಿದೆ, ಉದಾಹರಣೆಗೆ:ಆರ್ - ಆರ್ಗಾನ್ ವಸ್ತು (ಆರ್ ಪರಮಾಣುಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ),
H 2 O - ವಸ್ತುವಿನ ನೀರು (H 2 O ಅಣುಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ),
KNO 3 - ಪೊಟ್ಯಾಸಿಯಮ್ ನೈಟ್ರೇಟ್ ವಸ್ತು (K + ಕ್ಯಾಟಯಾನ್ಸ್ ಮತ್ತು NO 3 ¯ ಅಯಾನುಗಳನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ).
ಭೌತಿಕ ಪ್ರಮಾಣಗಳ ನಡುವಿನ ಸಂಬಂಧಗಳು
ಅಂಶದ ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿ (ಸಂಬಂಧಿ).ಬಿ, ಎ ಆರ್ (ಬಿ):ಎಲ್ಲಿ *ಟಿ(ಅಣು ಬಿ) - ಅಂಶ B ಯ ಪರಮಾಣುವಿನ ದ್ರವ್ಯರಾಶಿ;
* ಟಿ ಮತ್ತು- ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿ ಘಟಕ;
*ಟಿ ಮತ್ತು = 1/12 ಟಿ(12 ಸಿ ಪರಮಾಣು) = 1.6610 24 ಗ್ರಾಂ.
ವಸ್ತುವಿನ ಪ್ರಮಾಣ B, n(B), mol:
ಎಲ್ಲಿ ಎನ್(ಬಿ)- ಕಣಗಳ ಸಂಖ್ಯೆ ಬಿ;
ಎನ್ / ಎ– ಅವೊಗಾಡ್ರೊ ಸ್ಥಿರ (ಎನ್ ಎ = 6.0210 23 mol -1).
ವಸ್ತುವಿನ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿ V, M(V), g/mol:
ಎಲ್ಲಿ t(V)- ಮಾಸ್ ಬಿ.
ಅನಿಲದ ಮೋಲಾರ್ ಪರಿಮಾಣ IN, ವಿ ಎಂ l/mol:
ಎಲ್ಲಿ ವಿ ಎಂ = 22.4 ಲೀ/ಮೋಲ್ (ಅವೊಗಾಡ್ರೊ ನಿಯಮದ ಪರಿಣಾಮ), ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ (ಎನ್ಎಸ್ - ವಾತಾವರಣದ ಒತ್ತಡ p = 101,325 Pa (1 atm); ಥರ್ಮೋಡೈನಾಮಿಕ್ ತಾಪಮಾನ ಟಿ = 273.15 ಕೆ ಅಥವಾ ಸೆಲ್ಸಿಯಸ್ ತಾಪಮಾನ t = 0 °C).
ಬಿ ಹೈಡ್ರೋಜನ್, ಡಿ(ಗ್ಯಾಸ್ ಬಿ ಹೆಚ್ 2):
*ಅನಿಲ ಪದಾರ್ಥದ ಸಾಂದ್ರತೆ IN ಗಾಳಿಯ ಮೂಲಕ, ಡಿ(ಗಾಳಿಯಲ್ಲಿ ಅನಿಲ ಬಿ): ಅಂಶದ ದ್ರವ್ಯರಾಶಿಯ ಭಾಗಇ ವಿಷಯದಲ್ಲಿವಿ, ಡಬ್ಲ್ಯೂ(ಇ):ಇಲ್ಲಿ x ಎಂಬುದು ಬಿ ವಸ್ತುವಿನ ಸೂತ್ರದಲ್ಲಿ ಇ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆ
ಪರಮಾಣುವಿನ ರಚನೆ ಮತ್ತು ಆವರ್ತಕ ಕಾನೂನು D.I. ಮೆಂಡಲೀವ್
ದ್ರವ್ಯರಾಶಿ ಸಂಖ್ಯೆ (A) - ಪರಮಾಣು ನ್ಯೂಕ್ಲಿಯಸ್ನಲ್ಲಿರುವ ಪ್ರೋಟಾನ್ಗಳು ಮತ್ತು ನ್ಯೂಟ್ರಾನ್ಗಳ ಒಟ್ಟು ಸಂಖ್ಯೆ:
A = N(p 0) + N(p +).
ಪರಮಾಣು ಪರಮಾಣು ಚಾರ್ಜ್ (Z)ನ್ಯೂಕ್ಲಿಯಸ್ನಲ್ಲಿರುವ ಪ್ರೋಟಾನ್ಗಳ ಸಂಖ್ಯೆ ಮತ್ತು ಪರಮಾಣುವಿನ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಗೆ ಸಮನಾಗಿರುತ್ತದೆ:Z = N(p+) = N(e¯).
ಸಮಸ್ಥಾನಿಗಳು- ಅದೇ ಅಂಶದ ಪರಮಾಣುಗಳು, ನ್ಯೂಕ್ಲಿಯಸ್ನಲ್ಲಿರುವ ನ್ಯೂಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆಯಲ್ಲಿ ಭಿನ್ನವಾಗಿರುತ್ತವೆ, ಉದಾಹರಣೆಗೆ: ಪೊಟ್ಯಾಸಿಯಮ್ -39: 39 ಕೆ (19 p +, 20n 0, 19e¯); ಪೊಟ್ಯಾಸಿಯಮ್-40: 40 ಕೆ (19 p+, 21n 0, 19e¯).*ಶಕ್ತಿಯ ಮಟ್ಟಗಳು ಮತ್ತು ಉಪಮಟ್ಟಗಳು
* ಪರಮಾಣು ಕಕ್ಷೆ(AO) ಬಾಹ್ಯಾಕಾಶದ ಪ್ರದೇಶವನ್ನು ನಿರೂಪಿಸುತ್ತದೆ, ಇದರಲ್ಲಿ ಒಂದು ನಿರ್ದಿಷ್ಟ ಶಕ್ತಿಯನ್ನು ಹೊಂದಿರುವ ಎಲೆಕ್ಟ್ರಾನ್ನ ಸಂಭವನೀಯತೆಯು ದೊಡ್ಡದಾಗಿದೆ.*s- ಮತ್ತು p-ಕಕ್ಷೆಗಳ ಆಕಾರಗಳು
ಆವರ್ತಕ ಕಾನೂನು ಮತ್ತು ಆವರ್ತಕ ವ್ಯವಸ್ಥೆ D.I. ಮೆಂಡಲೀವ್
ಅಂಶಗಳ ಗುಣಲಕ್ಷಣಗಳು ಮತ್ತು ಅವುಗಳ ಸಂಯುಕ್ತಗಳು ನಿಯತಕಾಲಿಕವಾಗಿ ಹೆಚ್ಚುತ್ತಿರುವ ಪರಮಾಣು ಸಂಖ್ಯೆಯೊಂದಿಗೆ ಪುನರಾವರ್ತಿಸುತ್ತವೆ, ಇದು ಅಂಶದ ಪರಮಾಣುವಿನ ನ್ಯೂಕ್ಲಿಯಸ್ನ ಚಾರ್ಜ್ಗೆ ಸಮಾನವಾಗಿರುತ್ತದೆ.ಅವಧಿ ಸಂಖ್ಯೆಅನುರೂಪವಾಗಿದೆ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ತುಂಬಿದ ಶಕ್ತಿಯ ಮಟ್ಟಗಳ ಸಂಖ್ಯೆ,ಮತ್ತು ನಿಂತಿದೆ ತುಂಬಬೇಕಾದ ಕೊನೆಯ ಶಕ್ತಿಯ ಮಟ್ಟ(ಇಯು).
ಗುಂಪು ಸಂಖ್ಯೆ ಎತೋರಿಸುತ್ತದೆ ಮತ್ತು ಇತ್ಯಾದಿ
ಗುಂಪು ಸಂಖ್ಯೆ ಬಿತೋರಿಸುತ್ತದೆ ವೇಲೆನ್ಸಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳ ಸಂಖ್ಯೆ nsಮತ್ತು (ಎನ್ - 1) ಡಿ.
ಎಸ್-ಎಲಿಮೆಂಟ್ಸ್ ವಿಭಾಗ- ಶಕ್ತಿಯ ಉಪಮಟ್ಟದ (ESL) ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ತುಂಬಿರುತ್ತದೆ ns-EPU– IA- ಮತ್ತು IIA-ಗುಂಪುಗಳು, H ಮತ್ತು He.
ಪಿ-ಎಲಿಮೆಂಟ್ಸ್ ವಿಭಾಗ- ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ತುಂಬಿದೆ np-EPU- IIIA-VIIIA-ಗುಂಪುಗಳು.
ಡಿ-ಎಲಿಮೆಂಟ್ಸ್ ವಿಭಾಗ- ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ತುಂಬಿದೆ (ಪ- 1) d-EPU - IB-VIIIB2-ಗುಂಪುಗಳು.
f-ಅಂಶಗಳ ವಿಭಾಗ- ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ತುಂಬಿದೆ (ಪ-2) f-EPU - ಲ್ಯಾಂಥನೈಡ್ಗಳು ಮತ್ತು ಆಕ್ಟಿನೈಡ್ಗಳು.
ಆವರ್ತಕ ಕೋಷ್ಟಕದ 3 ನೇ ಅವಧಿಯ ಅಂಶಗಳ ಹೈಡ್ರೋಜನ್ ಸಂಯುಕ್ತಗಳ ಸಂಯೋಜನೆ ಮತ್ತು ಗುಣಲಕ್ಷಣಗಳಲ್ಲಿನ ಬದಲಾವಣೆಗಳು
ಬಾಷ್ಪಶೀಲವಲ್ಲದ, ನೀರಿನಿಂದ ಕೊಳೆತ: NaH, MgH 2, AlH 3.ಬಾಷ್ಪಶೀಲ: SiH 4, PH 3, H 2 S, HCl.
ಆವರ್ತಕ ಕೋಷ್ಟಕದ 3 ನೇ ಅವಧಿಯ ಅಂಶಗಳ ಹೆಚ್ಚಿನ ಆಕ್ಸೈಡ್ಗಳು ಮತ್ತು ಹೈಡ್ರಾಕ್ಸೈಡ್ಗಳ ಸಂಯೋಜನೆ ಮತ್ತು ಗುಣಲಕ್ಷಣಗಳಲ್ಲಿನ ಬದಲಾವಣೆಗಳು
ಮೂಲಭೂತ: Na 2 O - NaOH, MgO - Mg(OH) 2.ಆಂಫೋಟೆರಿಕ್:ಅಲ್ 2 ಒ 3 – ಅಲ್(ಓಎಚ್) 3.
ಆಮ್ಲೀಯ: SiO 2 – H 4 SiO 4, P 2 O 5 – H 3 PO 4, SO 3 – H 2 SO 4, Cl 2 O 7 – HClO 4.
ರಾಸಾಯನಿಕ ಬಂಧ
ಎಲೆಕ್ಟ್ರೋನೆಜಿಟಿವಿಟಿ(χ) ಋಣಾತ್ಮಕ ಚಾರ್ಜ್ ಅನ್ನು ಪಡೆಯಲು ಅಣುವಿನಲ್ಲಿ ಪರಮಾಣುವಿನ ಸಾಮರ್ಥ್ಯವನ್ನು ನಿರೂಪಿಸುವ ಪ್ರಮಾಣವಾಗಿದೆ.ಕೋವೆಲನ್ಸಿಯ ಬಂಧ ರಚನೆಯ ಕಾರ್ಯವಿಧಾನಗಳು
ವಿನಿಮಯ ಕಾರ್ಯವಿಧಾನ- ನೆರೆಯ ಪರಮಾಣುಗಳ ಎರಡು ಕಕ್ಷೆಗಳ ಅತಿಕ್ರಮಣ, ಪ್ರತಿಯೊಂದೂ ಒಂದು ಎಲೆಕ್ಟ್ರಾನ್ ಅನ್ನು ಹೊಂದಿತ್ತು.ದಾನಿ-ಸ್ವೀಕರಿಸುವ ಕಾರ್ಯವಿಧಾನ- ಒಂದು ಜೋಡಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ಹೊಂದಿರುವ ಮತ್ತೊಂದು ಪರಮಾಣುವಿನ ಕಕ್ಷೆಯೊಂದಿಗೆ ಒಂದು ಪರಮಾಣುವಿನ ಮುಕ್ತ ಕಕ್ಷೆಯ ಅತಿಕ್ರಮಣ.
ಬಂಧ ರಚನೆಯ ಸಮಯದಲ್ಲಿ ಕಕ್ಷೆಗಳ ಅತಿಕ್ರಮಣ
*ಹೈಬ್ರಿಡೈಸೇಶನ್ ಪ್ರಕಾರ - ಕಣದ ಜ್ಯಾಮಿತೀಯ ಆಕಾರ - ಬಂಧಗಳ ನಡುವಿನ ಕೋನ
ಕೇಂದ್ರ ಪರಮಾಣು ಕಕ್ಷೆಗಳ ಹೈಬ್ರಿಡೈಸೇಶನ್- ಅವರ ಶಕ್ತಿ ಮತ್ತು ರೂಪದ ಜೋಡಣೆ.sp- ರೇಖೀಯ - 180 °
sp 2- ತ್ರಿಕೋನ - 120 °
sp 3- ಟೆಟ್ರಾಹೆಡ್ರಲ್ - 109.5 °
sp 3 ಡಿ- ತ್ರಿಕೋನ-ಬೈಪಿರಮಿಡ್ - 90 °; 120°
ಎಸ್ಪಿ 3 ಡಿ 2- ಆಕ್ಟಾಹೆಡ್ರಲ್ - 90 °
ಮಿಶ್ರಣಗಳು ಮತ್ತು ಪರಿಹಾರಗಳು
ಪರಿಹಾರ- ಎರಡು ಅಥವಾ ಹೆಚ್ಚಿನ ಪದಾರ್ಥಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ಏಕರೂಪದ ವ್ಯವಸ್ಥೆ, ಅದರ ವಿಷಯವು ಕೆಲವು ಮಿತಿಗಳಲ್ಲಿ ಬದಲಾಗಬಹುದು.
ಪರಿಹಾರ:ದ್ರಾವಕ (ಉದಾ ನೀರು) + ದ್ರಾವಕ.
ನಿಜವಾದ ಪರಿಹಾರಗಳು 1 ನ್ಯಾನೊಮೀಟರ್ಗಿಂತ ಚಿಕ್ಕದಾದ ಕಣಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ.
ಕೊಲೊಯ್ಡಲ್ ಪರಿಹಾರಗಳು 1 ರಿಂದ 100 ನ್ಯಾನೊಮೀಟರ್ ಗಾತ್ರದವರೆಗಿನ ಕಣಗಳನ್ನು ಹೊಂದಿರುತ್ತದೆ.
ಯಾಂತ್ರಿಕ ಮಿಶ್ರಣಗಳು(ಅಮಾನತುಗಳು) 100 ನ್ಯಾನೊಮೀಟರ್ಗಳಿಗಿಂತ ದೊಡ್ಡದಾದ ಕಣಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ.
ಅಮಾನತು=> ಘನ + ದ್ರವ
ಎಮಲ್ಷನ್=> ದ್ರವ + ದ್ರವ
ಫೋಮ್, ಮಂಜು=> ಅನಿಲ + ದ್ರವ
ವೈವಿಧ್ಯಮಯ ಮಿಶ್ರಣಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸಲಾಗಿದೆನೆಲೆಗೊಳ್ಳುವಿಕೆ ಮತ್ತು ಫಿಲ್ಟರಿಂಗ್.
ಏಕರೂಪದ ಮಿಶ್ರಣಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸಲಾಗಿದೆಆವಿಯಾಗುವಿಕೆ, ಬಟ್ಟಿ ಇಳಿಸುವಿಕೆ, ಕ್ರೊಮ್ಯಾಟೋಗ್ರಫಿ.
ಸ್ಯಾಚುರೇಟೆಡ್ ಪರಿಹಾರದ್ರಾವಕದೊಂದಿಗೆ ಸಮತೋಲನದಲ್ಲಿರಬಹುದು ಅಥವಾ ಇರಬಹುದು (ದ್ರಾವಕವು ಘನವಾಗಿದ್ದರೆ, ಅದರ ಅಧಿಕವು ಅವಕ್ಷೇಪದಲ್ಲಿದೆ).
ಕರಗುವಿಕೆ- ನಿರ್ದಿಷ್ಟ ತಾಪಮಾನದಲ್ಲಿ ಸ್ಯಾಚುರೇಟೆಡ್ ದ್ರಾವಣದಲ್ಲಿ ಕರಗಿದ ವಸ್ತುವಿನ ವಿಷಯ.
ಅಪರ್ಯಾಪ್ತ ಪರಿಹಾರ ಕಡಿಮೆ,
ಸೂಪರ್ಸಾಚುರೇಟೆಡ್ ಪರಿಹಾರದ್ರಾವಣವನ್ನು ಹೊಂದಿರುತ್ತದೆ ಹೆಚ್ಚು,ನಿರ್ದಿಷ್ಟ ತಾಪಮಾನದಲ್ಲಿ ಅದರ ಕರಗುವಿಕೆಗಿಂತ.
ದ್ರಾವಣದಲ್ಲಿ ಭೌತ ರಾಸಾಯನಿಕ ಪ್ರಮಾಣಗಳ ನಡುವಿನ ಸಂಬಂಧಗಳು
ದ್ರಾವಣದ ದ್ರವ್ಯರಾಶಿ IN, w(B);ಒಂದು ಘಟಕದ ಭಾಗ ಅಥವಾ %:ಎಲ್ಲಿ t(V)- ದ್ರವ್ಯರಾಶಿ ಬಿ,
ಟಿ(ಆರ್)- ಪರಿಹಾರದ ದ್ರವ್ಯರಾಶಿ.
ಪರಿಹಾರದ ತೂಕ, m(p), g:
m(p) = m(B) + m(H 2 O) = V(p) ρ(p),
ಇಲ್ಲಿ F(p) ಎಂಬುದು ಪರಿಹಾರದ ಪರಿಮಾಣವಾಗಿದೆ;ρ (p) - ಪರಿಹಾರ ಸಾಂದ್ರತೆ.
ಪರಿಹಾರದ ಪರಿಮಾಣ, V(p),ಎಲ್:
ಮೋಲಾರ್ ಸಾಂದ್ರತೆ, s(V), mol/l:ಇಲ್ಲಿ n(B) ಎಂಬುದು B ವಸ್ತುವಿನ ಪ್ರಮಾಣ;
M(B) - ವಸ್ತು B ಯ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿ.
ಪರಿಹಾರದ ಸಂಯೋಜನೆಯನ್ನು ಬದಲಾಯಿಸುವುದು
ದ್ರಾವಣವನ್ನು ನೀರಿನಿಂದ ದುರ್ಬಲಗೊಳಿಸುವುದು:> ಟಿ"(ವಿ)= ಟಿ (ಬಿ);
> ಸೇರಿಸಿದ ನೀರಿನ ದ್ರವ್ಯರಾಶಿಯಿಂದ ದ್ರಾವಣದ ದ್ರವ್ಯರಾಶಿ ಹೆಚ್ಚಾಗುತ್ತದೆ: m"(p) = m(p) + m(H 2 O).
ದ್ರಾವಣದಿಂದ ನೀರನ್ನು ಆವಿಯಾಗಿಸುವುದು:
> ದ್ರಾವಣದ ದ್ರವ್ಯರಾಶಿಯು ಬದಲಾಗುವುದಿಲ್ಲ: t"(B) = t(B).
ಆವಿಯಾದ ನೀರಿನ ದ್ರವ್ಯರಾಶಿಯಿಂದ ದ್ರಾವಣದ ದ್ರವ್ಯರಾಶಿ ಕಡಿಮೆಯಾಗುತ್ತದೆ: m"(p) = m(p) – m(H 2 O).
ಎರಡು ಪರಿಹಾರಗಳನ್ನು ವಿಲೀನಗೊಳಿಸುವುದು:ದ್ರಾವಣಗಳ ದ್ರವ್ಯರಾಶಿಗಳು, ಹಾಗೆಯೇ ಕರಗಿದ ವಸ್ತುವಿನ ದ್ರವ್ಯರಾಶಿಗಳನ್ನು ಸೇರಿಸಲಾಗುತ್ತದೆ:
t"(B) = t(B) + t"(B);
t"(p) = t(p) + t"(p).
ಕ್ರಿಸ್ಟಲ್ ಡ್ರಾಪ್:ದ್ರಾವಣದ ದ್ರವ್ಯರಾಶಿ ಮತ್ತು ದ್ರಾವಣದ ದ್ರವ್ಯರಾಶಿಯು ಅವಕ್ಷೇಪಿತ ಹರಳುಗಳ ದ್ರವ್ಯರಾಶಿಯಿಂದ ಕಡಿಮೆಯಾಗುತ್ತದೆ:
m"(B) = m(B) – m(ಸೆಡಿಮೆಂಟ್); m"(p) = m(p) - m(ಸೆಡಿಮೆಂಟ್).
ನೀರಿನ ದ್ರವ್ಯರಾಶಿ ಬದಲಾಗುವುದಿಲ್ಲ.
ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ಉಷ್ಣ ಪರಿಣಾಮ
*ಒಂದು ವಸ್ತುವಿನ ರಚನೆಯ ಎಂಥಾಲ್ಪಿ ΔH°(B), kJ/mol, ಒಂದು ವಸ್ತುವಿನ 1 ಮೋಲ್ ಅನ್ನು ಅವುಗಳ ಪ್ರಮಾಣಿತ ಸ್ಥಿತಿಗಳಲ್ಲಿ ಸರಳ ಪದಾರ್ಥಗಳಿಂದ ರಚನೆಯ ಪ್ರತಿಕ್ರಿಯೆಯ ಎಂಥಾಲ್ಪಿ, ಅಂದರೆ, ಸ್ಥಿರ ಒತ್ತಡದಲ್ಲಿ (ವ್ಯವಸ್ಥೆಯಲ್ಲಿನ ಪ್ರತಿ ಅನಿಲಕ್ಕೆ 1 ಎಟಿಎಮ್ ಅಥವಾ ಒಟ್ಟು ಅನಿಲ ಪ್ರತಿಕ್ರಿಯೆ ಭಾಗವಹಿಸುವವರ ಅನುಪಸ್ಥಿತಿಯಲ್ಲಿ 1 ಎಟಿಎಮ್ ಒತ್ತಡ) ಮತ್ತು ಸ್ಥಿರ ತಾಪಮಾನ (ಸಾಮಾನ್ಯವಾಗಿ 298 ಕೆ , ಅಥವಾ 25 °C).ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ಉಷ್ಣ ಪರಿಣಾಮ (ಹೆಸ್ ಕಾನೂನು)
Q = ΣQ(ಉತ್ಪನ್ನಗಳು) - ΣQ(ಕಾರಕಗಳು).
ΔН° = ΣΔН°(ಉತ್ಪನ್ನಗಳು) - Σ ΔН°(ಕಾರಕಗಳು).
ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ aA + bB +... = dD + eE +...ΔH° = (dΔH°(D) + eΔH°(E) +…) – (aΔH°(A) + bΔH°(B) +…),
ಎಲ್ಲಿ a, b, d, e- ಪ್ರತಿಕ್ರಿಯೆ ಸಮೀಕರಣದಲ್ಲಿನ ಗುಣಾಂಕಗಳಿಗೆ ಅನುಗುಣವಾದ ಪದಾರ್ಥಗಳ ಸ್ಟೊಚಿಯೊಮೆಟ್ರಿಕ್ ಪ್ರಮಾಣಗಳು.ರಾಸಾಯನಿಕ ಪ್ರತಿಕ್ರಿಯೆ ದರ
ಸಮಯದಲ್ಲಿ ವೇಳೆ τ ಪರಿಮಾಣದಲ್ಲಿ ವಿΔ ನಿಂದ ಬದಲಾದ ಪ್ರತಿಕ್ರಿಯಾಕಾರಿ ಅಥವಾ ಉತ್ಪನ್ನದ ಪ್ರಮಾಣ n,ವೇಗ ಪ್ರತಿಕ್ರಿಯೆ:
ಮೊನೊಮಾಲಿಕ್ಯುಲರ್ ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ A →...:
ವಿ = ಕೆಸಿ(ಎ)
ಬೈಮೋಲಿಕ್ಯುಲರ್ ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ A + B → ...:ವಿ = ಕೆಸಿ(ಎ) ಸಿ(ಬಿ).
ಟ್ರೈಮೋಲಿಕ್ಯುಲರ್ ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ A + B + C → ...:ವಿ = ಕೆಸಿ (ಎ) ಸಿ (ಬಿ) ಸಿ (ಸಿ).
ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ದರವನ್ನು ಬದಲಾಯಿಸುವುದು
ವೇಗದ ಪ್ರತಿಕ್ರಿಯೆ ಹೆಚ್ಚಳ:1) ರಾಸಾಯನಿಕವಾಗಿ ಸಕ್ರಿಯಕಾರಕಗಳು;
2) ಪ್ರಚಾರಕಾರಕ ಸಾಂದ್ರತೆಗಳು;
3) ಹೆಚ್ಚಳ
4) ಪ್ರಚಾರತಾಪಮಾನ;
5) ವೇಗವರ್ಧಕಗಳು.ವೇಗದ ಪ್ರತಿಕ್ರಿಯೆ ಕಡಿಮೆ ಮಾಡಿ:
1) ರಾಸಾಯನಿಕವಾಗಿ ನಿಷ್ಕ್ರಿಯಕಾರಕಗಳು;
2) ಪದಚ್ಯುತಿಕಾರಕ ಸಾಂದ್ರತೆಗಳು;
3) ಇಳಿಕೆಘನ ಮತ್ತು ದ್ರವ ಕಾರಕಗಳ ಮೇಲ್ಮೈಗಳು;
4) ಪದಚ್ಯುತಿತಾಪಮಾನ;
5) ಪ್ರತಿರೋಧಕಗಳು.
*ತಾಪಮಾನ ವೇಗ ಗುಣಾಂಕ(γ) ತಾಪಮಾನವು ಹತ್ತು ಡಿಗ್ರಿಗಳಷ್ಟು ಹೆಚ್ಚಾದಾಗ ಪ್ರತಿಕ್ರಿಯೆ ದರವು ಎಷ್ಟು ಬಾರಿ ಹೆಚ್ಚಾಗುತ್ತದೆ ಎಂಬುದನ್ನು ತೋರಿಸುವ ಸಂಖ್ಯೆಗೆ ಸಮಾನವಾಗಿರುತ್ತದೆ:
ರಾಸಾಯನಿಕ ಸಮತೋಲನ
*ರಾಸಾಯನಿಕ ಸಮತೋಲನಕ್ಕಾಗಿ ಸಾಮೂಹಿಕ ಕ್ರಿಯೆಯ ನಿಯಮ:ಸಮತೋಲನದ ಸ್ಥಿತಿಯಲ್ಲಿ, ಉತ್ಪನ್ನಗಳ ಮೋಲಾರ್ ಸಾಂದ್ರತೆಯ ಉತ್ಪನ್ನದ ಅನುಪಾತಕ್ಕೆ ಸಮಾನವಾದ ಶಕ್ತಿಗಳಲ್ಲಿ
ಅವುಗಳ ಸ್ಟೊಚಿಯೊಮೆಟ್ರಿಕ್ ಗುಣಾಂಕಗಳು, ಅವುಗಳ ಸ್ಟೊಚಿಯೊಮೆಟ್ರಿಕ್ ಗುಣಾಂಕಗಳಿಗೆ ಸಮಾನವಾದ ಶಕ್ತಿಗಳಲ್ಲಿನ ಪ್ರತಿಕ್ರಿಯಾಕಾರಿಗಳ ಮೋಲಾರ್ ಸಾಂದ್ರತೆಯ ಉತ್ಪನ್ನಕ್ಕೆ, ಸ್ಥಿರ ತಾಪಮಾನದಲ್ಲಿ ಸ್ಥಿರ ಮೌಲ್ಯವಾಗಿದೆ. (ಸಾಂದ್ರೀಕರಣ ಸಮತೋಲನ ಸ್ಥಿರ).
ಹಿಂತಿರುಗಿಸಬಹುದಾದ ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ ರಾಸಾಯನಿಕ ಸಮತೋಲನದ ಸ್ಥಿತಿಯಲ್ಲಿ:
aA + bB + … ↔ dD + fF + ...
K c = [D] d [F] f .../ [A] a [B] b ...
*ಉತ್ಪನ್ನಗಳ ರಚನೆಯ ಕಡೆಗೆ ರಾಸಾಯನಿಕ ಸಮತೋಲನದಲ್ಲಿ ಬದಲಾವಣೆ
1) ಕಾರಕಗಳ ಸಾಂದ್ರತೆಯನ್ನು ಹೆಚ್ಚಿಸುವುದು;2) ಉತ್ಪನ್ನಗಳ ಸಾಂದ್ರತೆಯನ್ನು ಕಡಿಮೆ ಮಾಡುವುದು;
3) ತಾಪಮಾನದಲ್ಲಿ ಹೆಚ್ಚಳ (ಎಂಡೋಥರ್ಮಿಕ್ ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ);
4) ತಾಪಮಾನದಲ್ಲಿ ಇಳಿಕೆ (ಎಕ್ಸೋಥರ್ಮಿಕ್ ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ);
5) ಒತ್ತಡದಲ್ಲಿ ಹೆಚ್ಚಳ (ಪರಿಮಾಣದಲ್ಲಿ ಇಳಿಕೆಯೊಂದಿಗೆ ಸಂಭವಿಸುವ ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ);
6) ಒತ್ತಡದಲ್ಲಿ ಇಳಿಕೆ (ಪರಿಮಾಣದ ಹೆಚ್ಚಳದೊಂದಿಗೆ ಸಂಭವಿಸುವ ಪ್ರತಿಕ್ರಿಯೆಗಾಗಿ).
ದ್ರಾವಣದಲ್ಲಿ ಪ್ರತಿಕ್ರಿಯೆಗಳನ್ನು ವಿನಿಮಯ ಮಾಡಿಕೊಳ್ಳಿ
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ವಿಘಟನೆ- ಕೆಲವು ವಸ್ತುಗಳು ನೀರಿನಲ್ಲಿ ಕರಗಿದಾಗ ಅಯಾನುಗಳ (ಕ್ಯಾಟಯಾನುಗಳು ಮತ್ತು ಅಯಾನುಗಳು) ರಚನೆಯ ಪ್ರಕ್ರಿಯೆ.
ಆಮ್ಲಗಳುರಚನೆಯಾಗುತ್ತವೆ ಹೈಡ್ರೋಜನ್ ಕ್ಯಾಟಯಾನುಗಳುಮತ್ತು ಆಮ್ಲ ಅಯಾನುಗಳು,ಉದಾಹರಣೆಗೆ:
HNO 3 = H + + NO 3 ¯
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ವಿಘಟನೆಯ ಸಮಯದಲ್ಲಿ ಕಾರಣಗಳುರಚನೆಯಾಗುತ್ತವೆ ಲೋಹದ ಕ್ಯಾಟಯಾನುಗಳುಮತ್ತು ಹೈಡ್ರಾಕ್ಸೈಡ್ ಅಯಾನುಗಳು, ಉದಾಹರಣೆಗೆ:NaOH = Na + + OH¯
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ವಿಘಟನೆಯ ಸಮಯದಲ್ಲಿ ಲವಣಗಳು(ಮಧ್ಯಮ, ಡಬಲ್, ಮಿಶ್ರ) ರಚನೆಯಾಗುತ್ತದೆ ಲೋಹದ ಕ್ಯಾಟಯಾನುಗಳುಮತ್ತು ಆಮ್ಲ ಅಯಾನುಗಳು, ಉದಾಹರಣೆಗೆ:NaNO 3 = Na + + NO 3 ¯
KAl(SO 4) 2 = K + + Al 3+ + 2SO 4 2-
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ವಿಘಟನೆಯ ಸಮಯದಲ್ಲಿ ಆಮ್ಲ ಲವಣಗಳುರಚನೆಯಾಗುತ್ತವೆ ಲೋಹದ ಕ್ಯಾಟಯಾನುಗಳುಮತ್ತು ಆಸಿಡ್ ಹೈಡ್ರೇನಿಯನ್ಗಳು, ಉದಾಹರಣೆಗೆ:NaHCO 3 = Na + + HCO 3 ‾
ಕೆಲವು ಪ್ರಬಲ ಆಮ್ಲಗಳು
HBr, HCl, HClO 4, H 2 Cr 2 O 7, HI, HMnO 4, H 2 SO 4, H 2 SeO 4, HNO 3, H 2 CrO 4ಕೆಲವು ಬಲವಾದ ಕಾರಣಗಳು
RbOH, CsOH, KOH, NaOH, LiOH, Ba(OH) 2, Sr(OH) 2, Ca(OH) 2ಡಿಸೋಸಿಯೇಷನ್ ಪದವಿ α- ಆರಂಭಿಕ ಕಣಗಳ ಸಂಖ್ಯೆಗೆ ವಿಘಟಿತ ಕಣಗಳ ಸಂಖ್ಯೆಯ ಅನುಪಾತ.
ಸ್ಥಿರ ಪರಿಮಾಣದಲ್ಲಿ:
ವಿಘಟನೆಯ ಮಟ್ಟದಿಂದ ಪದಾರ್ಥಗಳ ವರ್ಗೀಕರಣ
ಬರ್ತೊಲೆಟ್ ನಿಯಮ
ಒಂದು ಅವಕ್ಷೇಪ, ಅನಿಲ ಅಥವಾ ದುರ್ಬಲ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ರಚನೆಯ ಪರಿಣಾಮವಾಗಿ ದ್ರಾವಣದಲ್ಲಿನ ವಿನಿಮಯ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಬದಲಾಯಿಸಲಾಗದಂತೆ ಮುಂದುವರಿಯುತ್ತವೆ.ಆಣ್ವಿಕ ಮತ್ತು ಅಯಾನಿಕ್ ಪ್ರತಿಕ್ರಿಯೆ ಸಮೀಕರಣಗಳ ಉದಾಹರಣೆಗಳು
1. ಆಣ್ವಿಕ ಸಮೀಕರಣ: CuCl 2 + 2NaOH = Cu(OH) 2 ↓ + 2NaCl“ಸಂಪೂರ್ಣ” ಅಯಾನಿಕ್ ಸಮೀಕರಣ: Сu 2+ + 2Сl¯ + 2Na + + 2OH¯ = Cu(OH) 2 ↓ + 2Na + + 2Сl¯
“ಸಣ್ಣ” ಅಯಾನಿಕ್ ಸಮೀಕರಣ: Cu 2+ + 2OH¯ = Cu(OH) 2 ↓
2. ಆಣ್ವಿಕ ಸಮೀಕರಣ: FeS (T) + 2HCl = FeCl 2 + H 2 S
“ಸಂಪೂರ್ಣ” ಅಯಾನಿಕ್ ಸಮೀಕರಣ: FeS + 2H + + 2Сl¯ = Fe 2+ + 2Сl¯ + H 2 S
"ಸಣ್ಣ" ಅಯಾನಿಕ್ ಸಮೀಕರಣ: FeS (T) + 2H + = Fe 2+ + H 2 S
3. ಆಣ್ವಿಕ ಸಮೀಕರಣ: 3HNO 3 + K 3 PO 4 = H 3 PO 4 + 3KNO 3
"ಸಂಪೂರ್ಣ" ಅಯಾನಿಕ್ ಸಮೀಕರಣ: 3H + + 3NO 3 ¯ + 3K + + PO 4 3- = H 3 PO 4 + 3K + + 3NO 3 ¯
"ಸಣ್ಣ" ಅಯಾನಿಕ್ ಸಮೀಕರಣ: 3H + + PO 4 3- = H 3 PO 4
* ಹೈಡ್ರೋಜನ್ ಮೌಲ್ಯ
(pH) pH = – ಲಾಗ್ = 14 + ಲಾಗ್* ತೆಳುವಾದ ಜಲೀಯ ದ್ರಾವಣಗಳಿಗೆ pH ಶ್ರೇಣಿ
pH 7 (ತಟಸ್ಥ ಪರಿಸರ)ವಿನಿಮಯ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಉದಾಹರಣೆಗಳು
ತಟಸ್ಥೀಕರಣ ಪ್ರತಿಕ್ರಿಯೆ- ಒಂದು ಆಸಿಡ್ ಮತ್ತು ಬೇಸ್ ಸಂವಹನ ಮಾಡಿದಾಗ ಸಂಭವಿಸುವ ವಿನಿಮಯ ಪ್ರತಿಕ್ರಿಯೆ.1. ಕ್ಷಾರ + ಪ್ರಬಲ ಆಮ್ಲ: Ba(OH) 2 + 2HCl = BaCl 2 + 2H 2 O
Ba 2+ + 2ON¯ + 2H + + 2Сl¯ = Ba 2+ + 2Сl¯ + 2Н 2 O
H + + OH¯ = H 2 O
2. ಸ್ವಲ್ಪ ಕರಗುವ ಬೇಸ್ + ಪ್ರಬಲ ಆಮ್ಲ: Cu(OH) 2(t) + 2HCl = CuCl 2 + 2H 2 O
Cu(OH) 2 + 2H + + 2Cl¯ = Cu 2+ + 2Cl¯ + 2H 2 O
Cu(OH) 2 + 2H + = Cu 2+ + 2H 2 O
* ಜಲವಿಚ್ಛೇದನ- ಪರಮಾಣುಗಳ ಆಕ್ಸಿಡೀಕರಣ ಸ್ಥಿತಿಯನ್ನು ಬದಲಾಯಿಸದೆ ವಸ್ತು ಮತ್ತು ನೀರಿನ ನಡುವಿನ ವಿನಿಮಯ ಪ್ರತಿಕ್ರಿಯೆ.
1. ಬೈನರಿ ಸಂಯುಕ್ತಗಳ ಬದಲಾಯಿಸಲಾಗದ ಜಲವಿಚ್ಛೇದನ:
Mg 3 N 2 + 6H 2 O = 3Mg(OH) 2 + 2NH 3
2. ಲವಣಗಳ ರಿವರ್ಸಿಬಲ್ ಜಲವಿಚ್ಛೇದನ:
ಎ) ಉಪ್ಪು ರೂಪುಗೊಳ್ಳುತ್ತದೆ ಬಲವಾದ ಬೇಸ್ ಕ್ಯಾಷನ್ ಮತ್ತು ಬಲವಾದ ಆಮ್ಲ ಅಯಾನು:
NaCl = Na + + Сl¯
Na + + H 2 O ≠ ;
Cl¯ + H 2 O ≠
ಜಲವಿಚ್ಛೇದನೆ ಇಲ್ಲ; ತಟಸ್ಥ ಪರಿಸರ, pH = 7.
ಬಿ) ಉಪ್ಪು ರೂಪುಗೊಳ್ಳುತ್ತದೆ ಬಲವಾದ ಬೇಸ್ ಕ್ಯಾಷನ್ ಮತ್ತು ದುರ್ಬಲ ಆಮ್ಲ ಅಯಾನು:
Na 2 S = 2Na + + S 2-
Na + + H 2 O ≠
S 2- + H 2 O ↔ HS¯ + OH¯
ಅಯಾನುಗಳಿಂದ ಜಲವಿಚ್ಛೇದನ; ಕ್ಷಾರೀಯ ಪರಿಸರ, pH >7.
ಬಿ) ಉಪ್ಪು ರೂಪುಗೊಳ್ಳುತ್ತದೆ ದುರ್ಬಲ ಅಥವಾ ಸ್ವಲ್ಪ ಕರಗುವ ಬೇಸ್ನ ಕ್ಯಾಟಯಾನ್ ಮತ್ತು ಬಲವಾದ ಆಮ್ಲದ ಅಯಾನ್:
ಪರಿಚಯಾತ್ಮಕ ತುಣುಕಿನ ಅಂತ್ಯ.
ಲೀಟರ್ LLC ನಿಂದ ಪಠ್ಯವನ್ನು ಒದಗಿಸಲಾಗಿದೆ.
ನೀವು ವೀಸಾ, ಮಾಸ್ಟರ್ಕಾರ್ಡ್, ಮೆಸ್ಟ್ರೋ ಬ್ಯಾಂಕ್ ಕಾರ್ಡ್ನೊಂದಿಗೆ, ಮೊಬೈಲ್ ಫೋನ್ ಖಾತೆಯಿಂದ, ಪಾವತಿ ಟರ್ಮಿನಲ್ನಿಂದ, MTS ಅಥವಾ Svyaznoy ಅಂಗಡಿಯಲ್ಲಿ, PayPal, WebMoney, Yandex.Money, QIWI ವಾಲೆಟ್, ಬೋನಸ್ ಕಾರ್ಡ್ಗಳು ಅಥವಾ ಮೂಲಕ ಪುಸ್ತಕವನ್ನು ಸುರಕ್ಷಿತವಾಗಿ ಪಾವತಿಸಬಹುದು. ನಿಮಗೆ ಅನುಕೂಲಕರವಾದ ಇನ್ನೊಂದು ವಿಧಾನ.
ಮಾಹಿತಿಯನ್ನು ಪರಿಶೀಲಿಸಿ. ಈ ಲೇಖನದಲ್ಲಿ ಪ್ರಸ್ತುತಪಡಿಸಿದ ಮಾಹಿತಿಯ ಸತ್ಯ ಮತ್ತು ವಿಶ್ವಾಸಾರ್ಹತೆಯ ನಿಖರತೆಯನ್ನು ಪರಿಶೀಲಿಸುವುದು ಅವಶ್ಯಕ. ಚರ್ಚೆ ಪುಟದಲ್ಲಿ ವಿಷಯದ ಕುರಿತು ಚರ್ಚೆ ಇದೆ: ಪರಿಭಾಷೆಯ ಬಗ್ಗೆ ಅನುಮಾನಗಳು. ರಾಸಾಯನಿಕ ಸೂತ್ರ ... ವಿಕಿಪೀಡಿಯಾ
ರಾಸಾಯನಿಕ ಸೂತ್ರವು ರಾಸಾಯನಿಕ ಚಿಹ್ನೆಗಳು, ಸಂಖ್ಯೆಗಳು ಮತ್ತು ಬ್ರಾಕೆಟ್ಗಳ ವಿಭಜಿಸುವ ಚಿಹ್ನೆಗಳನ್ನು ಬಳಸಿಕೊಂಡು ವಸ್ತುಗಳ ಸಂಯೋಜನೆ ಮತ್ತು ರಚನೆಯ ಬಗ್ಗೆ ಮಾಹಿತಿಯನ್ನು ಪ್ರತಿಬಿಂಬಿಸುತ್ತದೆ. ಪ್ರಸ್ತುತ, ಕೆಳಗಿನ ರೀತಿಯ ರಾಸಾಯನಿಕ ಸೂತ್ರಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸಲಾಗಿದೆ: ಸರಳವಾದ ಸೂತ್ರ. ಅನುಭವಿ ಮೂಲಕ ಪಡೆಯಬಹುದು... ... ವಿಕಿಪೀಡಿಯಾ
ರಾಸಾಯನಿಕ ಸೂತ್ರವು ರಾಸಾಯನಿಕ ಚಿಹ್ನೆಗಳು, ಸಂಖ್ಯೆಗಳು ಮತ್ತು ಬ್ರಾಕೆಟ್ಗಳ ವಿಭಜಿಸುವ ಚಿಹ್ನೆಗಳನ್ನು ಬಳಸಿಕೊಂಡು ವಸ್ತುಗಳ ಸಂಯೋಜನೆ ಮತ್ತು ರಚನೆಯ ಬಗ್ಗೆ ಮಾಹಿತಿಯನ್ನು ಪ್ರತಿಬಿಂಬಿಸುತ್ತದೆ. ಪ್ರಸ್ತುತ, ಕೆಳಗಿನ ರೀತಿಯ ರಾಸಾಯನಿಕ ಸೂತ್ರಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸಲಾಗಿದೆ: ಸರಳವಾದ ಸೂತ್ರ. ಅನುಭವಿ ಮೂಲಕ ಪಡೆಯಬಹುದು... ... ವಿಕಿಪೀಡಿಯಾ
ರಾಸಾಯನಿಕ ಸೂತ್ರವು ರಾಸಾಯನಿಕ ಚಿಹ್ನೆಗಳು, ಸಂಖ್ಯೆಗಳು ಮತ್ತು ಬ್ರಾಕೆಟ್ಗಳ ವಿಭಜಿಸುವ ಚಿಹ್ನೆಗಳನ್ನು ಬಳಸಿಕೊಂಡು ವಸ್ತುಗಳ ಸಂಯೋಜನೆ ಮತ್ತು ರಚನೆಯ ಬಗ್ಗೆ ಮಾಹಿತಿಯನ್ನು ಪ್ರತಿಬಿಂಬಿಸುತ್ತದೆ. ಪ್ರಸ್ತುತ, ಕೆಳಗಿನ ರೀತಿಯ ರಾಸಾಯನಿಕ ಸೂತ್ರಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸಲಾಗಿದೆ: ಸರಳವಾದ ಸೂತ್ರ. ಅನುಭವಿ ಮೂಲಕ ಪಡೆಯಬಹುದು... ... ವಿಕಿಪೀಡಿಯಾ
ರಾಸಾಯನಿಕ ಸೂತ್ರವು ರಾಸಾಯನಿಕ ಚಿಹ್ನೆಗಳು, ಸಂಖ್ಯೆಗಳು ಮತ್ತು ಬ್ರಾಕೆಟ್ಗಳ ವಿಭಜಿಸುವ ಚಿಹ್ನೆಗಳನ್ನು ಬಳಸಿಕೊಂಡು ವಸ್ತುಗಳ ಸಂಯೋಜನೆ ಮತ್ತು ರಚನೆಯ ಬಗ್ಗೆ ಮಾಹಿತಿಯನ್ನು ಪ್ರತಿಬಿಂಬಿಸುತ್ತದೆ. ಪ್ರಸ್ತುತ, ಕೆಳಗಿನ ರೀತಿಯ ರಾಸಾಯನಿಕ ಸೂತ್ರಗಳನ್ನು ಪ್ರತ್ಯೇಕಿಸಲಾಗಿದೆ: ಸರಳವಾದ ಸೂತ್ರ. ಅನುಭವಿ ಮೂಲಕ ಪಡೆಯಬಹುದು... ... ವಿಕಿಪೀಡಿಯಾ
ಮುಖ್ಯ ಲೇಖನ: ಅಜೈವಿಕ ಸಂಯುಕ್ತಗಳು ಅಜೈವಿಕ ಸಂಯುಕ್ತಗಳ ಅಂಶದ ಮೂಲಕ ಅಜೈವಿಕ ಸಂಯುಕ್ತಗಳ ಪಟ್ಟಿ ಪ್ರತಿ ವಸ್ತುವಿಗೆ ವರ್ಣಮಾಲೆಯ ಕ್ರಮದಲ್ಲಿ (ಸೂತ್ರದ ಮೂಲಕ) ಪ್ರಸ್ತುತಪಡಿಸಲಾದ ಅಜೈವಿಕ ಸಂಯುಕ್ತಗಳ ಪಟ್ಟಿ, ಅಂಶಗಳ ಹೈಡ್ರೋಜನ್ ಆಮ್ಲಗಳು (ಒಂದು ವೇಳೆ ... ... ವಿಕಿಪೀಡಿಯಾ
ಈ ಲೇಖನ ಅಥವಾ ವಿಭಾಗಕ್ಕೆ ಪರಿಷ್ಕರಣೆ ಅಗತ್ಯವಿದೆ. ದಯವಿಟ್ಟು ಲೇಖನಗಳನ್ನು ಬರೆಯುವ ನಿಯಮಗಳಿಗೆ ಅನುಸಾರವಾಗಿ ಲೇಖನವನ್ನು ಸುಧಾರಿಸಿ... ವಿಕಿಪೀಡಿಯಾ
ರಾಸಾಯನಿಕ ಸಮೀಕರಣ (ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ಸಮೀಕರಣ) ರಾಸಾಯನಿಕ ಸೂತ್ರಗಳು, ಸಂಖ್ಯಾತ್ಮಕ ಗುಣಾಂಕಗಳು ಮತ್ತು ಗಣಿತದ ಸಂಕೇತಗಳನ್ನು ಬಳಸಿಕೊಂಡು ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ಸಾಂಪ್ರದಾಯಿಕ ಪ್ರಾತಿನಿಧ್ಯವಾಗಿದೆ. ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ಸಮೀಕರಣವು ಗುಣಾತ್ಮಕ ಮತ್ತು ಪರಿಮಾಣಾತ್ಮಕತೆಯನ್ನು ನೀಡುತ್ತದೆ... ... ವಿಕಿಪೀಡಿಯಾ
ರಾಸಾಯನಿಕ ತಂತ್ರಾಂಶಗಳು ರಸಾಯನಶಾಸ್ತ್ರ ಕ್ಷೇತ್ರದಲ್ಲಿ ಬಳಸುವ ಕಂಪ್ಯೂಟರ್ ಪ್ರೋಗ್ರಾಂಗಳಾಗಿವೆ. ಪರಿವಿಡಿ 1 ರಾಸಾಯನಿಕ ಸಂಪಾದಕರು 2 ವೇದಿಕೆಗಳು 3 ಸಾಹಿತ್ಯ ... ವಿಕಿಪೀಡಿಯಾ
ಪುಸ್ತಕಗಳು
- ಕೈಗಾರಿಕಾ ಉಪಕರಣಗಳ ಸ್ಥಾಪನೆಗಾಗಿ ಜಪಾನೀಸ್-ಇಂಗ್ಲಿಷ್-ರಷ್ಯನ್ ನಿಘಂಟು. ಸುಮಾರು 8,000 ಪದಗಳು, ಪೊಪೊವಾ I.S.. ನಿಘಂಟನ್ನು ವ್ಯಾಪಕ ಶ್ರೇಣಿಯ ಬಳಕೆದಾರರಿಗಾಗಿ ಮತ್ತು ಪ್ರಾಥಮಿಕವಾಗಿ ಜಪಾನ್ ಅಥವಾ ಕೈಗಾರಿಕಾ ಉಪಕರಣಗಳ ಪೂರೈಕೆ ಮತ್ತು ಅನುಷ್ಠಾನದಲ್ಲಿ ತೊಡಗಿರುವ ಅನುವಾದಕರು ಮತ್ತು ತಾಂತ್ರಿಕ ತಜ್ಞರಿಗೆ ಉದ್ದೇಶಿಸಲಾಗಿದೆ.
- ಜೀವರಾಸಾಯನಿಕ ಪದಗಳ ಸಂಕ್ಷಿಪ್ತ ನಿಘಂಟು, ಕುನಿಝೆವ್ S.M.. ನಿಘಂಟು ಸಾಮಾನ್ಯ ಜೀವರಸಾಯನಶಾಸ್ತ್ರ, ಪರಿಸರ ವಿಜ್ಞಾನ ಮತ್ತು ಜೈವಿಕ ತಂತ್ರಜ್ಞಾನದ ಮೂಲಭೂತ ಕೋರ್ಸ್ಗಳನ್ನು ಅಧ್ಯಯನ ಮಾಡುವ ವಿಶ್ವವಿದ್ಯಾಲಯಗಳಲ್ಲಿ ರಾಸಾಯನಿಕ ಮತ್ತು ಜೈವಿಕ ವಿಶೇಷತೆಗಳ ವಿದ್ಯಾರ್ಥಿಗಳಿಗೆ ಉದ್ದೇಶಿಸಲಾಗಿದೆ ಮತ್ತು ಇದನ್ನು ಸಹ ಬಳಸಬಹುದು ...
ಹಲವಾರು ಮೂಲಭೂತ ಪರಿಕಲ್ಪನೆಗಳು ಮತ್ತು ಸೂತ್ರಗಳು.
ಎಲ್ಲಾ ಪದಾರ್ಥಗಳು ವಿಭಿನ್ನ ದ್ರವ್ಯರಾಶಿ, ಸಾಂದ್ರತೆ ಮತ್ತು ಪರಿಮಾಣವನ್ನು ಹೊಂದಿವೆ. ಒಂದು ಅಂಶದಿಂದ ಲೋಹದ ತುಂಡು ಮತ್ತೊಂದು ಲೋಹದ ನಿಖರವಾಗಿ ಅದೇ ಗಾತ್ರದ ತುಂಡುಗಿಂತ ಅನೇಕ ಪಟ್ಟು ಹೆಚ್ಚು ತೂಗುತ್ತದೆ.
ಮೋಲ್(ಮೋಲ್ಗಳ ಸಂಖ್ಯೆ)
ಹುದ್ದೆ: ಮೋಲ್, ಅಂತಾರಾಷ್ಟ್ರೀಯ: mol- ವಸ್ತುವಿನ ಪ್ರಮಾಣಕ್ಕೆ ಮಾಪನದ ಘಟಕ. ಒಳಗೊಂಡಿರುವ ವಸ್ತುವಿನ ಪ್ರಮಾಣಕ್ಕೆ ಅನುರೂಪವಾಗಿದೆ ಎನ್ / ಎ.ಕಣಗಳು (ಅಣುಗಳು, ಪರಮಾಣುಗಳು, ಅಯಾನುಗಳು) ಆದ್ದರಿಂದ, ಸಾರ್ವತ್ರಿಕ ಪ್ರಮಾಣವನ್ನು ಪರಿಚಯಿಸಲಾಯಿತು - ಮೋಲ್ಗಳ ಸಂಖ್ಯೆ.ಕಾರ್ಯಗಳಲ್ಲಿ ಆಗಾಗ್ಗೆ ಎದುರಾಗುವ ನುಡಿಗಟ್ಟು "ಸ್ವೀಕರಿಸಲಾಗಿದೆ... ವಸ್ತುವಿನ ಮೋಲ್"
ಎನ್ / ಎ.= 6.02 1023
ಎನ್ / ಎ.- ಅವೊಗಾಡ್ರೊ ಸಂಖ್ಯೆ. ಸಹ "ಒಪ್ಪಂದದ ಮೂಲಕ ಒಂದು ಸಂಖ್ಯೆ." ಪೆನ್ಸಿಲ್ನ ತುದಿಯಲ್ಲಿ ಎಷ್ಟು ಪರಮಾಣುಗಳಿವೆ? ಸುಮಾರು ಒಂದು ಸಾವಿರ. ಅಂತಹ ಪ್ರಮಾಣದಲ್ಲಿ ಕಾರ್ಯನಿರ್ವಹಿಸಲು ಇದು ಅನುಕೂಲಕರವಾಗಿಲ್ಲ. ಆದ್ದರಿಂದ, ಪ್ರಪಂಚದಾದ್ಯಂತದ ರಸಾಯನಶಾಸ್ತ್ರಜ್ಞರು ಮತ್ತು ಭೌತವಿಜ್ಞಾನಿಗಳು ಒಪ್ಪಿಕೊಂಡರು - 6.02 × 1023 ಕಣಗಳನ್ನು (ಪರಮಾಣುಗಳು, ಅಣುಗಳು, ಅಯಾನುಗಳು) ಎಂದು ಗೊತ್ತುಪಡಿಸೋಣ 1 ಮೋಲ್ ಪದಾರ್ಥಗಳು.
1 ಮೋಲ್ = 6.02 1023 ಕಣಗಳು
ಸಮಸ್ಯೆಗಳನ್ನು ಪರಿಹರಿಸುವ ಮೂಲ ಸೂತ್ರಗಳಲ್ಲಿ ಇದು ಮೊದಲನೆಯದು.
ವಸ್ತುವಿನ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿ
ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿವಸ್ತುವು ಒಂದರ ದ್ರವ್ಯರಾಶಿ ವಸ್ತುವಿನ ಮೋಲ್.
ಶ್ರೀ ಎಂದು ಸೂಚಿಸಲಾಗುತ್ತದೆ. ಇದು ಆವರ್ತಕ ಕೋಷ್ಟಕದ ಪ್ರಕಾರ ಕಂಡುಬರುತ್ತದೆ - ಇದು ಕೇವಲ ವಸ್ತುವಿನ ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿಗಳ ಮೊತ್ತವಾಗಿದೆ.
ಉದಾಹರಣೆಗೆ, ನಮಗೆ ಸಲ್ಫ್ಯೂರಿಕ್ ಆಮ್ಲವನ್ನು ನೀಡಲಾಗುತ್ತದೆ - H2SO4. ವಸ್ತುವಿನ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿಯನ್ನು ಲೆಕ್ಕಾಚಾರ ಮಾಡೋಣ: ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿ H = 1, S-32, O-16.
ಶ್ರೀ(H2SO4)=1 2+32+16 4=98 g\mol.
ಸಮಸ್ಯೆಗಳನ್ನು ಪರಿಹರಿಸಲು ಅಗತ್ಯವಿರುವ ಎರಡನೆಯ ಸೂತ್ರ
ವಸ್ತುವಿನ ದ್ರವ್ಯರಾಶಿ ಸೂತ್ರ:
ಅಂದರೆ, ವಸ್ತುವಿನ ದ್ರವ್ಯರಾಶಿಯನ್ನು ಕಂಡುಹಿಡಿಯಲು, ನೀವು ಮೋಲ್ಗಳ (n) ಸಂಖ್ಯೆಯನ್ನು ತಿಳಿದುಕೊಳ್ಳಬೇಕು ಮತ್ತು ಆವರ್ತಕ ಕೋಷ್ಟಕದಿಂದ ನಾವು ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿಯನ್ನು ಕಂಡುಕೊಳ್ಳುತ್ತೇವೆ.
ದ್ರವ್ಯರಾಶಿಯ ಸಂರಕ್ಷಣೆಯ ನಿಯಮ -ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗೆ ಪ್ರವೇಶಿಸುವ ವಸ್ತುಗಳ ದ್ರವ್ಯರಾಶಿ ಯಾವಾಗಲೂ ಪರಿಣಾಮವಾಗಿ ಉಂಟಾಗುವ ವಸ್ತುಗಳ ದ್ರವ್ಯರಾಶಿಗೆ ಸಮಾನವಾಗಿರುತ್ತದೆ.
ನಾವು ಪ್ರತಿಕ್ರಿಯಿಸಿದ ಪದಾರ್ಥಗಳ ದ್ರವ್ಯರಾಶಿಯನ್ನು ತಿಳಿದಿದ್ದರೆ, ಆ ಕ್ರಿಯೆಯ ಉತ್ಪನ್ನಗಳ ದ್ರವ್ಯರಾಶಿಯನ್ನು ಕಂಡುಹಿಡಿಯಬಹುದು. ಮತ್ತು ಪ್ರತಿಯಾಗಿ.
ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿನ ಸಮಸ್ಯೆಗಳನ್ನು ಪರಿಹರಿಸುವ ಮೂರನೇ ಸೂತ್ರ
ವಸ್ತುವಿನ ಪರಿಮಾಣ:
ಕ್ಷಮಿಸಿ, ಈ ಚಿತ್ರವು ನಮ್ಮ ಮಾರ್ಗಸೂಚಿಗಳನ್ನು ಪೂರೈಸುತ್ತಿಲ್ಲ. ಪ್ರಕಟಣೆಯನ್ನು ಮುಂದುವರಿಸಲು, ದಯವಿಟ್ಟು ಚಿತ್ರವನ್ನು ಅಳಿಸಿ ಅಥವಾ ಇನ್ನೊಂದನ್ನು ಅಪ್ಲೋಡ್ ಮಾಡಿ.22.4 ಸಂಖ್ಯೆ ಎಲ್ಲಿಂದ ಬಂತು? ಇಂದ ಅವೊಗಾಡ್ರೊ ಕಾನೂನು:
ಒಂದೇ ತಾಪಮಾನ ಮತ್ತು ಒತ್ತಡದಲ್ಲಿ ತೆಗೆದುಕೊಳ್ಳಲಾದ ವಿಭಿನ್ನ ಅನಿಲಗಳ ಸಮಾನ ಪರಿಮಾಣಗಳು ಒಂದೇ ಸಂಖ್ಯೆಯ ಅಣುಗಳನ್ನು ಹೊಂದಿರುತ್ತವೆ.
ಅವೊಗಾಡ್ರೊ ನಿಯಮದ ಪ್ರಕಾರ, ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳಲ್ಲಿ (ಎನ್ಎಸ್) ಆದರ್ಶ ಅನಿಲದ 1 ಮೋಲ್ ಒಂದೇ ಪರಿಮಾಣವನ್ನು ಹೊಂದಿರುತ್ತದೆ Vm= 22.413 996(39) ಎಲ್
ಅಂದರೆ, ಸಮಸ್ಯೆಯಲ್ಲಿ ನಮಗೆ ಸಾಮಾನ್ಯ ಪರಿಸ್ಥಿತಿಗಳನ್ನು ನೀಡಿದರೆ, ಮೋಲ್ಗಳ ಸಂಖ್ಯೆಯನ್ನು (ಎನ್) ತಿಳಿದುಕೊಳ್ಳುವುದರಿಂದ, ನಾವು ವಸ್ತುವಿನ ಪರಿಮಾಣವನ್ನು ಕಂಡುಹಿಡಿಯಬಹುದು.
ಆದ್ದರಿಂದ, ಸಮಸ್ಯೆಗಳನ್ನು ಪರಿಹರಿಸಲು ಮೂಲ ಸೂತ್ರಗಳುರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ
ಅವಗಾಡ್ರೊ ಸಂಖ್ಯೆಎನ್ / ಎ.
6.02 1023 ಕಣಗಳು
ವಸ್ತುವಿನ ಪ್ರಮಾಣ n (mol)
n=V\22.4 (l\mol)
ವಸ್ತುವಿನ ದ್ರವ್ಯರಾಶಿಮೀ (ಜಿ)
ವಸ್ತುವಿನ ಪರಿಮಾಣ ವಿ(ಎಲ್)
V=n 22.4 (l\mol)
ಕ್ಷಮಿಸಿ, ಈ ಚಿತ್ರವು ನಮ್ಮ ಮಾರ್ಗಸೂಚಿಗಳನ್ನು ಪೂರೈಸುತ್ತಿಲ್ಲ. ಪ್ರಕಟಣೆಯನ್ನು ಮುಂದುವರಿಸಲು, ದಯವಿಟ್ಟು ಚಿತ್ರವನ್ನು ಅಳಿಸಿ ಅಥವಾ ಇನ್ನೊಂದನ್ನು ಅಪ್ಲೋಡ್ ಮಾಡಿ.ಇವು ಸೂತ್ರಗಳು. ಸಾಮಾನ್ಯವಾಗಿ, ಸಮಸ್ಯೆಗಳನ್ನು ಪರಿಹರಿಸಲು, ನೀವು ಮೊದಲು ಪ್ರತಿಕ್ರಿಯೆ ಸಮೀಕರಣವನ್ನು ಬರೆಯಬೇಕು ಮತ್ತು (ಅಗತ್ಯವಿದೆ!) ಗುಣಾಂಕಗಳನ್ನು ವ್ಯವಸ್ಥೆಗೊಳಿಸಬೇಕು - ಅವರ ಅನುಪಾತವು ಪ್ರಕ್ರಿಯೆಯಲ್ಲಿ ಮೋಲ್ಗಳ ಅನುಪಾತವನ್ನು ನಿರ್ಧರಿಸುತ್ತದೆ.
ಪ್ರಮುಖ ಪದಗಳು: ರಸಾಯನಶಾಸ್ತ್ರ 8 ನೇ ತರಗತಿ. ಎಲ್ಲಾ ಸೂತ್ರಗಳು ಮತ್ತು ವ್ಯಾಖ್ಯಾನಗಳು, ಭೌತಿಕ ಪ್ರಮಾಣಗಳ ಚಿಹ್ನೆಗಳು, ಮಾಪನದ ಘಟಕಗಳು, ಮಾಪನದ ಘಟಕಗಳನ್ನು ಗೊತ್ತುಪಡಿಸುವ ಪೂರ್ವಪ್ರತ್ಯಯಗಳು, ಘಟಕಗಳ ನಡುವಿನ ಸಂಬಂಧಗಳು, ರಾಸಾಯನಿಕ ಸೂತ್ರಗಳು, ಮೂಲ ವ್ಯಾಖ್ಯಾನಗಳು, ಸಂಕ್ಷಿಪ್ತವಾಗಿ, ಕೋಷ್ಟಕಗಳು, ರೇಖಾಚಿತ್ರಗಳು.
1. ಚಿಹ್ನೆಗಳು, ಹೆಸರುಗಳು ಮತ್ತು ಅಳತೆಯ ಘಟಕಗಳು
ರಸಾಯನಶಾಸ್ತ್ರದಲ್ಲಿ ಬಳಸಲಾಗುವ ಕೆಲವು ಭೌತಿಕ ಪ್ರಮಾಣಗಳು
| ಭೌತಿಕ ಪ್ರಮಾಣ | ಹುದ್ದೆ | ಘಟಕ |
| ಸಮಯ | ಟಿ | ಬಿ= |
| ಒತ್ತಡ | ಪ | ಪಾ, ಕೆಪಿಎ |
| ವಸ್ತುವಿನ ಪ್ರಮಾಣ | ν | ಮೋಲ್ |
| ವಸ್ತುವಿನ ದ್ರವ್ಯರಾಶಿ | ಮೀ | ಕೆಜಿ, ಜಿ |
| ಮಾಸ್ ಫ್ರಾಕ್ಷನ್ | ω | ಆಯಾಮರಹಿತ |
| ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿ | ಎಂ | ಕೆಜಿ / ಮೋಲ್, ಜಿ / ಮೋಲ್ |
| ಮೋಲಾರ್ ಪರಿಮಾಣ | Vn | m 3 / mol, l / mol |
| ವಸ್ತುವಿನ ಪರಿಮಾಣ | ವಿ | ಮೀ 3, ಎಲ್ |
| ಪರಿಮಾಣದ ಭಾಗ | ಆಯಾಮರಹಿತ | |
| ಸಾಪೇಕ್ಷ ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿ | ಎ ಆರ್ | ಆಯಾಮರಹಿತ |
| ಶ್ರೀ | ಆಯಾಮರಹಿತ | |
| ಅನಿಲ A ಗೆ ಅನಿಲ B ಗೆ ಸಾಪೇಕ್ಷ ಸಾಂದ್ರತೆ | ಡಿಬಿ (ಎ) | ಆಯಾಮರಹಿತ |
| ವಸ್ತುವಿನ ಸಾಂದ್ರತೆ | ಆರ್ | kg/m 3, g/cm 3, g/ml |
| ಅವಗಾಡ್ರೊ ಸ್ಥಿರ | ಎನ್ / ಎ | 1/mol |
| ಸಂಪೂರ್ಣ ತಾಪಮಾನ | ಟಿ | ಕೆ (ಕೆಲ್ವಿನ್) |
| ಸೆಲ್ಸಿಯಸ್ನಲ್ಲಿ ತಾಪಮಾನ | ಟಿ | °C (ಡಿಗ್ರಿ ಸೆಲ್ಸಿಯಸ್) |
| ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯ ಉಷ್ಣ ಪರಿಣಾಮ | ಪ್ರ | kJ/mol |

2. ಭೌತಿಕ ಪ್ರಮಾಣಗಳ ಘಟಕಗಳ ನಡುವಿನ ಸಂಬಂಧಗಳು

3. 8 ನೇ ತರಗತಿಯಲ್ಲಿ ರಾಸಾಯನಿಕ ಸೂತ್ರಗಳು
4. 8 ನೇ ತರಗತಿಯಲ್ಲಿ ಮೂಲಭೂತ ವ್ಯಾಖ್ಯಾನಗಳು

- ಪರಮಾಣು- ವಸ್ತುವಿನ ಚಿಕ್ಕ ರಾಸಾಯನಿಕವಾಗಿ ಅವಿಭಾಜ್ಯ ಕಣ.
- ರಾಸಾಯನಿಕ ಅಂಶ- ಒಂದು ನಿರ್ದಿಷ್ಟ ರೀತಿಯ ಪರಮಾಣು.
- ಅಣು- ಅದರ ಸಂಯೋಜನೆ ಮತ್ತು ರಾಸಾಯನಿಕ ಗುಣಲಕ್ಷಣಗಳನ್ನು ಉಳಿಸಿಕೊಳ್ಳುವ ಮತ್ತು ಪರಮಾಣುಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ವಸ್ತುವಿನ ಚಿಕ್ಕ ಕಣ.
- ಸರಳ ಪದಾರ್ಥಗಳು- ಅಣುಗಳು ಒಂದೇ ರೀತಿಯ ಪರಮಾಣುಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ವಸ್ತುಗಳು.
- ಸಂಕೀರ್ಣ ಪದಾರ್ಥಗಳು- ಅಣುಗಳು ವಿವಿಧ ರೀತಿಯ ಪರಮಾಣುಗಳನ್ನು ಒಳಗೊಂಡಿರುವ ವಸ್ತುಗಳು.
- ವಸ್ತುವಿನ ಗುಣಾತ್ಮಕ ಸಂಯೋಜನೆ ಇದು ಯಾವ ಅಂಶಗಳ ಪರಮಾಣುಗಳನ್ನು ಒಳಗೊಂಡಿದೆ ಎಂಬುದನ್ನು ತೋರಿಸುತ್ತದೆ.
- ವಸ್ತುವಿನ ಪರಿಮಾಣಾತ್ಮಕ ಸಂಯೋಜನೆ ಅದರ ಸಂಯೋಜನೆಯಲ್ಲಿ ಪ್ರತಿ ಅಂಶದ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆಯನ್ನು ತೋರಿಸುತ್ತದೆ.
- ರಾಸಾಯನಿಕ ಸೂತ್ರ- ರಾಸಾಯನಿಕ ಚಿಹ್ನೆಗಳು ಮತ್ತು ಸೂಚ್ಯಂಕಗಳನ್ನು ಬಳಸಿಕೊಂಡು ವಸ್ತುವಿನ ಗುಣಾತ್ಮಕ ಮತ್ತು ಪರಿಮಾಣಾತ್ಮಕ ಸಂಯೋಜನೆಯ ಸಾಂಪ್ರದಾಯಿಕ ರೆಕಾರ್ಡಿಂಗ್.
- ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿ ಘಟಕ(ಅಮು) - ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿಯ ಮಾಪನದ ಘಟಕ, ಇಂಗಾಲದ ಪರಮಾಣುವಿನ 1/12 ದ್ರವ್ಯರಾಶಿಗೆ ಸಮಾನವಾಗಿರುತ್ತದೆ 12 ಸಿ.
- ಮೋಲ್- 0.012 ಕೆಜಿ ಇಂಗಾಲದ 12 ಸಿ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆಗೆ ಸಮಾನವಾದ ಕಣಗಳ ಸಂಖ್ಯೆಯನ್ನು ಹೊಂದಿರುವ ವಸ್ತುವಿನ ಪ್ರಮಾಣ.
- ಅವಗಾಡ್ರೊ ಸ್ಥಿರ (ಎನ್ / ಎ = 6*10 23 mol -1) - ಒಂದು ಮೋಲ್ನಲ್ಲಿರುವ ಕಣಗಳ ಸಂಖ್ಯೆ.
- ವಸ್ತುವಿನ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿ (ಗಾಳಿಯಲ್ಲಿ X ಅನಿಲ ಪದಾರ್ಥದ ಸಾಂದ್ರತೆ ) 1 ಮೋಲ್ನ ಪ್ರಮಾಣದಲ್ಲಿ ತೆಗೆದುಕೊಳ್ಳಲಾದ ವಸ್ತುವಿನ ದ್ರವ್ಯರಾಶಿಯಾಗಿದೆ.
- ಸಾಪೇಕ್ಷ ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿಅಂಶ ಎ ಆರ್ - ನಿರ್ದಿಷ್ಟ ಅಂಶದ ಪರಮಾಣುವಿನ ದ್ರವ್ಯರಾಶಿಯ ಅನುಪಾತವು ಇಂಗಾಲದ ಪರಮಾಣುವಿನ ದ್ರವ್ಯರಾಶಿಯ m 0 ರಿಂದ 1/12 12 ಸಿ.
- ಸಾಪೇಕ್ಷ ಆಣ್ವಿಕ ತೂಕಪದಾರ್ಥಗಳು ಗಾಳಿಯಲ್ಲಿ X ಅನಿಲ ಪದಾರ್ಥದ ಸಾಂದ್ರತೆ ಆರ್ - ನಿರ್ದಿಷ್ಟ ವಸ್ತುವಿನ ಅಣುವಿನ ದ್ರವ್ಯರಾಶಿಯ ಅನುಪಾತವು ಇಂಗಾಲದ ಪರಮಾಣುವಿನ 1/12 ದ್ರವ್ಯರಾಶಿಯ 12 ಸಿ. ಸಾಪೇಕ್ಷ ಆಣ್ವಿಕ ದ್ರವ್ಯರಾಶಿಯು ಸಂಯುಕ್ತವನ್ನು ರೂಪಿಸುವ ರಾಸಾಯನಿಕ ಅಂಶಗಳ ಸಾಪೇಕ್ಷ ಪರಮಾಣು ದ್ರವ್ಯರಾಶಿಗಳ ಮೊತ್ತಕ್ಕೆ ಸಮಾನವಾಗಿರುತ್ತದೆ. ನಿರ್ದಿಷ್ಟ ಅಂಶದ ಪರಮಾಣುಗಳ ಸಂಖ್ಯೆಯನ್ನು ಗಣನೆಗೆ ತೆಗೆದುಕೊಳ್ಳಿ.
- ಮಾಸ್ ಫ್ರಾಕ್ಷನ್ರಾಸಾಯನಿಕ ಅಂಶ ω(X) X ವಸ್ತುವಿನ ಸಾಪೇಕ್ಷ ಆಣ್ವಿಕ ದ್ರವ್ಯರಾಶಿಯ ಯಾವ ಭಾಗವನ್ನು ನಿರ್ದಿಷ್ಟ ಅಂಶದಿಂದ ಪರಿಗಣಿಸಲಾಗಿದೆ ಎಂಬುದನ್ನು ತೋರಿಸುತ್ತದೆ.
ಪರಮಾಣು-ಮಾಲಿಕ್ಯೂಲರ್ ಬೋಧನೆ
1. ಆಣ್ವಿಕ ಮತ್ತು ಅಣುರಹಿತ ರಚನೆಯೊಂದಿಗೆ ಪದಾರ್ಥಗಳಿವೆ.
2. ಅಣುಗಳ ನಡುವೆ ಅಂತರಗಳಿವೆ, ಅದರ ಗಾತ್ರಗಳು ವಸ್ತು ಮತ್ತು ತಾಪಮಾನದ ಒಟ್ಟುಗೂಡಿಸುವಿಕೆಯ ಸ್ಥಿತಿಯನ್ನು ಅವಲಂಬಿಸಿರುತ್ತದೆ.
3. ಅಣುಗಳು ನಿರಂತರ ಚಲನೆಯಲ್ಲಿವೆ.
4. ಅಣುಗಳು ಪರಮಾಣುಗಳಿಂದ ಮಾಡಲ್ಪಟ್ಟಿದೆ.
6. ಪರಮಾಣುಗಳನ್ನು ನಿರ್ದಿಷ್ಟ ದ್ರವ್ಯರಾಶಿ ಮತ್ತು ಗಾತ್ರದಿಂದ ನಿರೂಪಿಸಲಾಗಿದೆ.
ಭೌತಿಕ ವಿದ್ಯಮಾನಗಳ ಸಮಯದಲ್ಲಿ, ರಾಸಾಯನಿಕ ವಿದ್ಯಮಾನಗಳ ಸಮಯದಲ್ಲಿ ಅಣುಗಳನ್ನು ಸಂರಕ್ಷಿಸಲಾಗಿದೆ, ನಿಯಮದಂತೆ, ಅವು ನಾಶವಾಗುತ್ತವೆ. ರಾಸಾಯನಿಕ ವಿದ್ಯಮಾನಗಳ ಸಮಯದಲ್ಲಿ ಪರಮಾಣುಗಳು ಮರುಹೊಂದಿಸಲ್ಪಡುತ್ತವೆ, ಹೊಸ ಪದಾರ್ಥಗಳ ಅಣುಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ.

ವಸ್ತುವಿನ ಸ್ಥಿರ ಸಂಯೋಜನೆಯ ಕಾನೂನು
ಆಣ್ವಿಕ ರಚನೆಯ ಪ್ರತಿಯೊಂದು ರಾಸಾಯನಿಕವಾಗಿ ಶುದ್ಧ ಪದಾರ್ಥ, ತಯಾರಿಕೆಯ ವಿಧಾನವನ್ನು ಲೆಕ್ಕಿಸದೆ, ಸ್ಥಿರವಾದ ಗುಣಾತ್ಮಕ ಮತ್ತು ಪರಿಮಾಣಾತ್ಮಕ ಸಂಯೋಜನೆಯನ್ನು ಹೊಂದಿರುತ್ತದೆ.
ವೇಲೆನ್ಸ್
ವೇಲೆನ್ಸಿ ಎನ್ನುವುದು ರಾಸಾಯನಿಕ ಅಂಶದ ಪರಮಾಣುವಿನ ಆಸ್ತಿಯಾಗಿದ್ದು ಅದು ಮತ್ತೊಂದು ಅಂಶದ ನಿರ್ದಿಷ್ಟ ಸಂಖ್ಯೆಯ ಪರಮಾಣುಗಳನ್ನು ಲಗತ್ತಿಸಲು ಅಥವಾ ಬದಲಾಯಿಸಲು.

ರಾಸಾಯನಿಕ ಕ್ರಿಯೆ
ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಯು ಒಂದು ವಿದ್ಯಮಾನವಾಗಿದೆ, ಇದರ ಪರಿಣಾಮವಾಗಿ ಒಂದು ವಸ್ತುವಿನಿಂದ ಇತರ ವಸ್ತುಗಳು ರೂಪುಗೊಳ್ಳುತ್ತವೆ. ಪ್ರತಿಕ್ರಿಯಾಕಾರಿಗಳು ರಾಸಾಯನಿಕ ಕ್ರಿಯೆಗೆ ಪ್ರವೇಶಿಸುವ ವಸ್ತುಗಳು. ಪ್ರತಿಕ್ರಿಯೆ ಉತ್ಪನ್ನಗಳು ಕ್ರಿಯೆಯ ಪರಿಣಾಮವಾಗಿ ರೂಪುಗೊಂಡ ಪದಾರ್ಥಗಳಾಗಿವೆ.
ರಾಸಾಯನಿಕ ಪ್ರತಿಕ್ರಿಯೆಗಳ ಚಿಹ್ನೆಗಳು:
1. ಶಾಖದ ಬಿಡುಗಡೆ (ಬೆಳಕು).
2. ಬಣ್ಣದಲ್ಲಿ ಬದಲಾವಣೆ.
3. ವಾಸನೆ ಕಾಣಿಸಿಕೊಳ್ಳುತ್ತದೆ.
4. ಕೆಸರು ರಚನೆ.
5. ಅನಿಲ ಬಿಡುಗಡೆ.




 ವಿ ಮೀ= 22.4 l/mol (n.s.)
ವಿ ಮೀ= 22.4 l/mol (n.s.)